Neumología
La especialidadArtículos especializados
Enfermedades
Síntomas
Otros contenidos

Enfermedad
Edema Pulmonar
¿Qué es un edema pulmonar?
El edema pulmonar, edema agudo de pulmón o congestión del pulmón, es una enfermedad producida por la acumulación de líquido en los pulmones afectando al sistema respiratorio y disminuyendo la capacidad de respiración. El líquido se acumula en los sacos de aire de los pulmones (alvéolos).
El edema pulmonar puede aparecer de repente. Es una urgencia médica que precisa de atención rápida porque puede llegar a ser mortal si no recibe tratamiento.
Tipos de edemas
Los tipos de edema son:
Edema pulmonar cardiogénico : el corazón recibe sangre del sistema respiratorio por el ventrículo derecho y de ahí pasa a los pulmones. Cuando existen problemas aparece la insuficiencia cardiaca, donde el corazón no consigue evacuar de manera eficaz la sangre que recibe del sistema sanguíneo. Esto provoca un aumento de presión en los pulmones haciendo que el líquido pase de los vasos sanguíneos a los alvéolos.
Edema pulmonar no cardiogénico: cuando el causante no es el mal funcionamiento del corazón sino del sistema sanguíneo. La sangre no es capaz de mantenerse dentro de los vasos sanguíneos invadiendo el interior de los alvéolos de líquido.
Causas del edema pulmonar
La causa del edema pulmonar es cualquier situación que eleve la presión capilar de los pulmones.También puede ser entre otras por:
Infarto agudo de miocardio.
Arritmia cardiaca.
Aumento de la presión arterial.
Hipoxemia (disminución de oxígeno en sangre) por altura.
Sobrecarga de líquidos administrados necesidades terapéuticas unidas a un mal funcionamiento renal.
Traumatismos graves.
Problemas cardiacos.
Tabaco y drogas.
Altitudes superiores a 2500 m.
Síntomas del edema pulmonar
El síntoma principal es la disnea , dificultad para respirar sensación de asfixia bien en reposo o al realizar alguna actividad física. Otros síntomas son:
Dificultades para hablar.
Sensación de sangre o espuma con sangre en la boca.
Ruido de tipo ronquera al respirar.
Sudoración.
Ansiedad.
Palidez en la piel o coloración azulada.
Inflamación de piernas y abdomen.
Respiración rápida.
Taquicardia.
No tolerar estar tumbado
Disminución de orina.
Malestar general.
Molestias en el pecho.
Fiebre.
Tratamiento del edema pulmonar
El tratamiento depende de la gravedad, pero en cualquier caso tiene tres objetivos fundamentales que son:
Administración de oxígeno para mejorar la función pulmonar con una mascarilla o con un respirador en casos más graves.
Administración de diuréticos que permiten eliminar líquidos a través de la orina para disminuir la presión pulmonar (venocapilar).
Medicación para dilatar las venas y por tanto disminuir la cantidad de sangre que llega al corazón.
Si la causa es por alguna enfermedad el tratamiento será específico de esa patología.
Pruebas complementarias del edema pulmonar
Las principales pruebas complementarias del edema pulmonar son:
Exploración física, auscultación pulmonar, saturación de oxígeno, toma de tensión arterial y frecuencia cardiaca.
Radiografía de tórax.
Electrocardiograma.
Ecocardiograma.
Análisis de orina y sangre.
Factores desencadenantes del edema pulmonar
Cuando el corazón no es capaz de bombear la sangre de los pulmones al resto del organismo. Esto produce un aumento de la presión de los vasos sanguíneos haciendo que el líquido pase a los sacos de aire (alvéolos) en los pulmones. Por lo tanto, el intercambio de oxígeno entre los vasos sanguíneos y los alvéolos se reduce y causa dificultad para respirar. El factor desencadenante se debe a cualquier situación que eleve la presión pulmonar.
Factores de riesgo del edema pulmonar
Entre los principales factores de riesgo destacamos:
Tensión arterial elevada.
Fumar en exceso.
Consumo de drogas.
Dieta rica en grasa y exceso de sal.
Estrés.
Antecedentes familiares de cardiopatías.
Padecer enfermedades que comprometan las funciones respiratorias, cardiacas y renales.
Abandono de medicación habitual de determinadas patologías que puedan provocar edema pulmonar.
Sobrecarga de líquidos administrados de manera terapéutica.
Anemias graves.
Deportes de altitud.
Enfermedades de las válvulas del corazón.
Complicaciones del edema pulmonar
La complicación del edema pulmonar es la muerte por paro cardiorrespiratorio.
Prevención del edema pulmonar
Hacer una dieta cardiosaludable, baja en grasa y sal.
Tomar la medicación adecuadamente en caso de padecer alguna enfermedad con riesgo de provocar un edema pulmonar o problemas cardiacos. Hacer ejercicio físico regularmente.
Especialidades a las que pertenece
La especialidad médica para tratar el edema pulmonar son los neumólogos y cardiólogos.
Preguntas frecuentes
¿Qué puede producir un edema pulmonar?
El edema pulmonar lo puede producir cualquier enfermedad o situación que produzca un aumento de la presión pulmonar. Los vasos sanguíneos y los alvéolos no hacen de manera eficaz el intercambio de oxígeno, llenándose, estos últimos, de líquido.
¿Qué es tener líquido en los pulmones?
Tener líquido en los pulmones significa que los alvéolos están llenos de líquido.
¿Qué es la trombosis pulmonar?
La trombosis pulmonar es la obstrucción, de manera súbita, de una arteria de los pulmones. Generalmente es causado por un coágulo de la pierna que emigra y circula por el torrente sanguíneo hasta el pulmón. Provoca bajos niveles de oxígeno en sangre y por tanto lesiones en algunos los órganos por falta de oxígeno. También puede causar daños permanentes en el pulmón afectado.
¿Qué es un enfisema pulmonar?
El enfisema pulmonar es una enfermedad pulmonar obstructiva donde los alvéolos están dañados y no pueden coger el oxígeno necesario. Esto hace que sea más difícil recuperar la respiración tras el ejercicio y que se tenga tos crónica. El causante principal es el tabaco .
¿Qué es un infarto pulmonar?
El infarto pulmonar llamada también embolia pulmonar, es la obstrucción de uno o más vasos grandes pulmonares que impide que la zona afectada tenga riego sanguíneo . Puede manifestarse con sensación de ahogo, dolor torácico, mareo, coloración azulada de la piel, tos con esputos de sangre, fiebre. Es una enfermedad grave que puede provocar la muerte súbita del paciente.

Enfermedad
Hiperreactividad Bronquial
¿Qué es la hiperreactividad bronquial?
La hipersensibilidad o hiperreactividad bronquial (HRB) es la respuesta anormal y exagerada de la vía respiratoria y la mucosa bronquial y responsable del origen de broncoespasmo. No es una enfermedad por sí misma. Se refiere a que los bronquios reaccionan más de lo habitual frente a muchos estímulos, como infecciones, alergias, aire frío, contaminación, ejercicio, tabaco, etc. La hiperreactividad bronquial es una característica, un rasgo del asma. Puede ser debida a alguna alergia y también puede aparecer como resultado de infecciones de los bronquios y persistir durante mucho tiempo. Suele ser más frecuente en niños y adolescentes, aunque puede ocurrir a cualquier edad, también en personas que realizan alguna actividad física frecuente. Es una afección muy común, la gravedad va a depender de las causas que la provocan, ya que, si no se trata adecuadamente, puede derivar a complicaciones más serias.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tipos de hiperactividades
No se conocen variantes de esta enfermedad.
Causas de la hiperreactividad bronquial
No está claro por qué algunas personas contraen hiperreactividad bronquial y otras no, sin embargo, es probable que se deba a una combinación de factores ambientales y genéticos (hereditarios). La hiperreactividad bronquial puede también presentarse en algunos pacientes (aunque no todos) con la fiebre del heno , fibrosis quística, bronquitis crónica e incluso puede detectarse en algunas personas sin enfermedad respiratoria. También puede aparecer de forma transitoria tras infecciones respiratorias o exposiciones a irritantes. La causa que produce la hiperreactividad bronquial en los pacientes con asma se desconoce, aunque parece que, en parte, puede ser debida a una ruptura de la integridad de la mucosa bronquial ocasionada por una inflamación persistente, principalmente a base de eosinófilos, que se detecta en todos los pacientes asmáticos, incluso en los más leves.
Síntomas de la hiperreactividad bronquial
Los síntomas pueden incluir:
Falta de aire.
Dolor u opresión en el pecho.
Tos con o sin producción de esputo (flema).
Problemas para dormir causados por falta de aire, tos o silbido al respirar.
Retracción o tiraje de la piel entre las costillas al respirar.
Dificultad para respirar que empeora con el ejercicio o la actividad.
Un pitido o silbido al respirar que puede oírse al exhalar.
Tos o silbido al respirar que empeora con un virus respiratorio, como un resfrío o influenza, presión torácica y sensación de tirantez, entre otros síntomas.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tratamiento de la hiperreactividad bronquial
El tratamiento para la hiperreactividad bronquial puede ser el mismo que para el asma. El tratamiento, generalmente, implica aprender a reconocer los desencadenantes, tomar medidas para evitarlos y controlar la respiración para garantizar que los medicamentos diarios para el asma mantengan los síntomas bajo control.
Los medicamentos adecuados dependen de una serie de cuestiones, como la edad, los síntomas, los desencadenantes de la hiperreactividad bronquial y lo que sea más efectivo para mantener los síntomas bajo control.
Los medicamentos preventivos de control a largo plazo reducen la inflamación de las vías respiratorias que produce los síntomas . Los inhaladores de alivio rápido (broncodilatadores) abren rápidamente las vías respiratorias inflamadas que restringen la respiración.
En algunos casos, es necesario tomar medicamentos contra la alergia. Existen diversos medicamentos que tienen efecto antiinflamatorio en la mucosa bronquial, pero los más potentes y eficaces son los corticoides (cortisona) inhalados. Para el tratamiento inmediato, se utilizan broncodilatadores, que normalmente se administran por vía inhalatoria.
Pruebas complementarias de la hiperreactividad bronquial
Las pruebas complementarias para el diagnóstico de la hiperreactividad bronquial pueden incluir : pruebas de alergias, examen de sangre o piel para ver si una persona es alérgica a ciertas sustancias, gasometría arterial (normalmente se lleva a cabo sólo con pacientes que están sufriendo un ataque de asma grave), radiografía de tórax y pruebas de la función pulmonar, entre otras pruebas.
Factores desencadenantes de la hiperreactividad bronquial
En las personas con vías respiratorias sensibles, los síntomas pueden desencadenarse por la inhalación de sustancias llamadas alérgenos o desencadenantes . Los más comunes incluyen: animales (caspa o pelaje de mascotas), ácaros del polvo, ciertos medicamentos (ácido acetilsalicílico o aspirina y otros AINE), cambios en el clima (con mayor frecuencia el clima frío), químicos en el aire o en los alimentos, moho, polen y humo del tabaco, entre otros desencadenantes.
Factores de riesgo de la hiperreactividad bronquial
Entre los factores que aumentan el riesgo de padecer hiperreactividad bronquial están: tener un pariente consanguíneo (como padre o hermano) con asma, tener una afección alérgica, como dermatitis atópica o rinitis alérgica (fiebre del heno), ser fumador, exposición al tabaquismo pasivo, y exposición a desencadenantes en el ámbito laboral, como los productos químicos utilizados en las industrias de la agricultura, la peluquería y la fabricación, entre otros factores.
Complicaciones de la hiperreactividad bronquial
Las complicaciones de la hiperreactividad bronquial pueden incluir:
Signos y síntomas que interfieren en el sueño , el trabajo o las actividades recreativas.
Estrechamiento permanente de los tubos bronquiales que afecta la forma en que se puede respirar.
Efectos secundarios del consumo a largo plazo de algunos medicamentos que se utilizan para estabilizar el asma grave.
Prevención de la hiperreactividad bronquial
La mejor forma de prevenir la hiperreactividad bronquial es evitar los factores que puedan desencadenar los síntomas.
Especialidades a las que pertenece
La hiperreactividad bronquial pertenece a la especialidad de neumología, está es la rama de la medicina que está dedicada a la evaluación, prevención, diagnóstico y tratamiento de las patologías del aparato respiratorio.
Preguntas frecuentes:
¿Qué es el asma?
El asma es una afección en la que se estrechan y se hinchan las vías respiratorias, lo cual produce mayor mucosidad. Esto podría dificultar la respiración y provocar tos, silbido al respirar y falta de aire.
¿Es lo mismo hiperreactividad bronquial que asma?
La hiperreactividad bronquial es una característica, un rasgo del asma. Por lo que podría ser lo mismo.
¿Qué es la hiperreactividad bronquial por frío?
Se refiere a que los bronquios reaccionan más de lo habitual frente a los estímulos del frío.
¿Qué remedios naturales hay para la hiperreactividad bronquial?
El té de jengibre es una gran alternativa para aliviar la hiperreactividad bronquial de manera natural. La cebolla también contiene un flavonoide llamado quercetina que ayuda a relajar los bronquios y disminuir la constricción de las vías respiratorias. El belcho (efedra) contiene efedrina y seudoefedrina, sustancias broncodilatadoras que expanden las vías respiratorias para ayudar a respirar más fácilmente. Pero se recomienda que si el paciente tiene algún síntoma respiratorio acuda al médico.
¿Qué remedios caseros hay para el asma?
El ajo era usado como un medicamento natural mucho antes de ser usado como condimento. Gracias a sus propiedades antiinflamatorias, ha sido considerado como uno de los remedios caseros más eficaces contra el asma. Tomar jugo de limón mezclado con agua ayuda a evitar que la mucosidad se acumule en los bronquios, mejora la respiración y limpia el aparato respiratorio de bacterias y gérmenes que podrían dificultar el paso del aire. La cúrcuma es una especia con propiedades antiinflamatorias y expectorantes, lo que la convierte en una gran opción para curar el asma naturalmente. El té de jengibre es una gran alternativa para aliviar el asma de manera natural. Aunque existen estos remedios naturales, lo más recomendable es acudir al médico.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Enfermedad
Enfermedad Pulmonar Onstructiva Crónica
¿Qué es la enfermedad pulmonar obstructiva crónica?
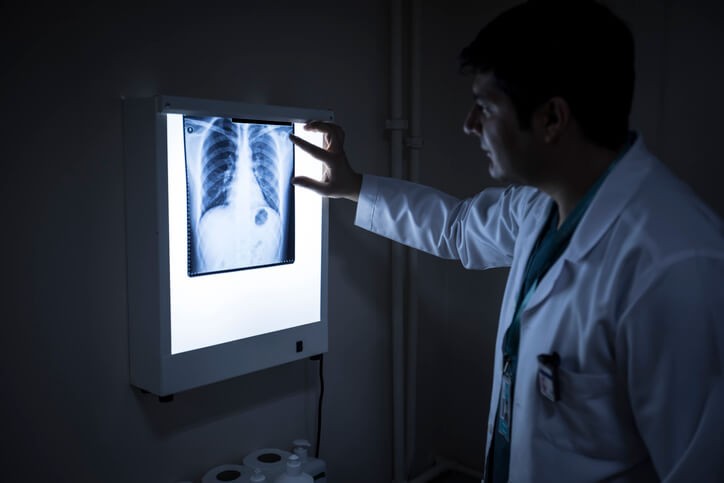
La enfermedad pulmonar obstructiva crónica, bronquitis crónica o EPOC es la enfermedad pulmonar que se produce por alteración inflamatoria de los bronquios . Los casos de enfermedad obstructiva en mayores de 40 años en España es de 10,2 por ciento, siendo en varones de 15,1 por ciento. Es una enfermedad que va desde leve a grave y que puede dar lugar a episodios de hipoventilación , con descenso del oxígeno en sangre a niveles que pueden poner en peligro la vida del enfermo.
Tipos de enfermedades pulmonares
Las enfermedades pulmonares se pueden dividir en enfermedades infecciosas, asma, bronquitis crónica y enfisema pulmonar.
Enfermedades infecciosas neumonías y tuberculosis son las enfermedades pulmonares infecciosas más frecuentes y precisan de tratamiento antibiótico para su mejoría.
Asma , es una enfermedad que produce inflamación de los bronquios y se caracteriza por dificultad en la espiración (cuando sale el aire del pulmón) produciendo un ruido conocido como sibilancias. Puede ser intrinseca o extrinseca, el asma extrínseca está relacionada con procesos alérgicos.
Bronquitis crónica es la enfermedad que produce inflamación bronquial, relacionada sobre todo con el humo del tabaco.
Enfisema pulmonar es la destrucción o dilatación de los alvéolos pulmonares, alterando el intercambio gaseoso en los mismos.
Causas de la enfermedad pulmonar obstructiva crónica
La causa principal de la enfermedad pulmonar obstructiva crónica es el humo del tabaco en los países desarrollados, en las zonas en vía de desarrollo será la contaminación y la combustión en zonas mal ventiladas de cocinas de carbón y calefacciones. El 1 por ciento de la enfermedad obstructiva crónica se debe al déficit genético de alfa 1 antitripsina.
Síntomas de la enfermedad pulmonar obstructiva crónica
Los síntomas principales de la enfermedad obstructiva crónica son la tos, dificultad para respirar, ruido de mucosidad en el pecho, fatiga y sensación de falta de aire . En los estadios más avanzados aparecen labios y uñas azules y se puede producir hinchazón en las piernas debido al daño cardíaco que se produce en el avance de la enfermedad.
Tratamiento de la enfermedad pulmonar obstructiva crónica
El tratamiento de la enfermedad pulmonar obstructiva crónica se va a realizar con:
Broncodilatadores inhalados , cuya función será disminuir la inflamación del bronquio, aumentando la capacidad respiratoria del paciente. Entre los inhaladores tendremos broncodilatadores de acción rápida como el salbutamol o la terbutalina, broncodilatadores de acción prolongada como el tiotropio, el salmeterol o el formoterol, esteroides inhalados como la budesonida y la fluticasona. Combinaciones de estos fármacos pueden también usarse como inhalador único.
Los esteroides orales tipo prednisona o deflazacort pueden usarse en casos de recidivas, con grave compromiso bronquial, en pautas cortas de entre 3 y 5 días.
Teofilinas son fármacos antiguos con poco uso en el momento actual.
Será necesaria la vacunación preventiva tanto de su gripe como del neumococo .
La oxigenoterapia podrá usarse en caso avanzados, cuando el nivel de oxígeno que se encuentra en el aire no es suficiente para garantizar una correcta oxigenación de la sangre del paciente.
La rehabilitación pulmonar pretende enseñar al enfermo a expulsar las flemas de forma correcta usando tanto el diafragma como los músculos intercostales para una correcta respiración.
Pruebas complementarias de la enfermedad pulmonar obstructiva crónica
Las pruebas complementarias para llegar al diagnóstico y controlar el tratamiento serán:
Análisis de sangre con medición del oxígeno en sangre arterial y hemograma ya que la falta de oxígeno puede dar lugar a un aumento de los glóbulos rojos.
Radiografía de tórax que permite conocer la situación pulmonar.
TAC puede ser necesario en los casos de sospecha de un enfisema, para valorar qué parte del pulmón puede estar dañada por este proceso.
Electrocardiograma que permite conocer si existe una sobrecarga cardíaca, secundaria al proceso pulmonar.
Espirometría valorando tanto la capacidad vital, esto es la cantidad de aire que entra en los pulmones, como la capacidad espiratoria a través del volumen espiratorio forzado en el primer segundo. En muchos casos se realiza una espirometría tras administrar broncodilatadores, esto permite conocer cuánto va a mejorar un paciente con un tratamiento correcto.
Factores desencadenantes de la enfermedad pulmonar obstructiva crónica
La causa desencadenante de la enfermedad pulmonar obstructiva crónica será principalmente la exposición al humo del tabaco , que se asocia a otros modos de exposición a contaminantes ambientales y lugares de trabajo con sustancias químicas o humos.
También existen causas genéticas como es la falta de alfa 1 antitripsina.
Factores de riesgo de la enfermedad pulmonar obstructiva crónica
Son factores de riesgo:
Humo del tabaco , cuantos más cigarrillos se fuman y durante más años en la vida de una persona, es más probable que se tenga una enfermedad pulmonar obstructiva crónica. También se da en personas que fuman en pipa o marihuana, y en personas que soportan el llamado tabaquismo pasivo.
Exposición a sustancias químicas y polvos en suspensión. Está relacionado con ciertos tipos de trabajo como mineros, personas que trabajan con piedra, con polvo de madera, vapores de pinturas y barnices pueden sufrir con más facilidad esta enfermedad.
Personas que se ven sometidas a humos de calefacciones o de cocinas con carbón o maderas.
Edad , siendo más frecuente a partir de los 40 años.
Genetica , personas con déficit de alfa 1 antitripsina.
Complicaciones de la enfermedad pulmonar obstructiva crónica
Las complicaciones de la enfermedad pulmonar obstructiva crónica son:
Infecciones pulmonares de repetición.
Daño cardiaco.
Insuficiencia cardiaca.
Fibrilación auricular.
Hipertensión pulmonar.
Cancer de pulmon.
Prevención de la enfermedad pulmonar obstructiva crónica
La prevención de la enfermedad pulmonar obstructiva crónica requiere:
Dejar de fumar.
No exponerse a vapores de sustancias químicas.
No exponerse a combustión en lugares mal ventilados.
Especialidades a las que pertenece
La bronquitis crónica o enfermedad obstructiva crónica va a ser controlada en sus fases más precoces por el médico de familia , que también deberá de encargarse de la vacunación de la gripe y la neumonía, y de ayudar al enfermo a dejar de fumar. En las fases más avanzadas de la enfermedad se deberán de controlar por el neumólogo .
Preguntas frecuentes:
¿Qué es la EPOC?
El EPOC es la enfermedad pulmonar obstructiva crónica, también conocida como bronquitis crónica , es una enfermedad pulmonar en la cual se va a producir una inflamación y constricción de los bronquios que origina dificultad para poder inhalar, exhalar y hacer un intercambio gaseoso correcto en los pulmones.
¿Qué es la bronquitis crónica?
La bronquitis crónica o enfermedad pulmonar obstructiva crónica será la inflamación crónica de los bronquios , dando lugar a una alteración del intercambio gaseoso en los mismos lo que da lugar a una menor cantidad de oxígeno en sangre a nivel arterial, de la que es necesaria para una correcta oxigenación de los tejidos.
¿Qué es la fibrosis pulmonar?
Los pulmones están formados por un tejido elástico , que se distiende al llenarse de aire , cuando se produce la fibrosis pulmonar. Este tejido se endurece y como consecuencia no se puede distender de forma adecuada
¿A qué órganos afecta la EPOC?
La bronquitis crónica afecta primero a los pulmones que se encuentran inflamados, esto hace que se aumente la tensión pulmonar y posteriormente se dañe el corazón. No obstante, otros muchos órganos sufren con esta enfermedad ya que en algunas ocasiones no llega bastante oxígeno a órganos vitales, como puede ser el cerebro y los riñones , que van sufriendo daños a lo largo de la enfermedad.
¿Qué es un enfisema pulmonar?
El enfisema es la enfermedad pulmonar que provoca la rotura de los alvéolos pulmonares , que es la parte más pequeña del pulmón donde tiene lugar el intercambio gaseoso, entre la sangre y el aire. Cuando esto ocurre la sangre se oxigena de forma más pobre. Se trata de una forma de enfermedad pulmonar obstructiva crónica.

Enfermedad
Insuficiencia Respiratoria
¿Qué es una insuficiencia respiratoria?
La insuficiencia respiratoria es un tra storno en el que no se produce una correcta oxigenación de la sangre debido a alguna patología o afectación pulmonar, de forma aguda, de forma crónica, o progresiva. Es una alteración que se da bastante que puede llegar a ser muy grave, ya que compromete la vida del paciente y que de forma más frecuente se da en paciente mayores con patologías de base.
Tipos de insuficiencias respiratorias
Insuficiencia respiratoria hipercápnica : se produce por retención aguda de dióxido de carbono (CO2).
Insuficiencia respiratoria hipóxica : se produce cuando el intercambio gaseoso de oxígeno y dióxido de carbono se altera, lo que lleva a la hipoxemia o disminución de oxígeno en la sangre (saturación de sangre arterial de oxígeno menor a 90%). Dentro de este tipo se engloba el síndrome de insuficiencia respiratoria aguda (SIRA), producida por una lesión pulmonar aguda.
Causas de una insuficiencia respiratoria
Las causas que producen una insuficiencia respiratoria son aquellas alteraciones que afectan al normal funcionamiento del pulmón como aparición de edema en su tejido, obstrucción de las vías respiratorias, inflamación de sus tejidos, obstrucciones vasculares, infecciones, alteraciones anatómicas torácicas o pulmonares, alteraciones neurológicas…etc. De esta forma, se pueden enumerar una gran cantidad de enfermedades, alteraciones y situaciones que pueden determinar la aparición de una insuficiencia respiratoria: E nfermedad pulmonar obstructiva crónica, asma, sarcoidosis, neumonía, embolia pulmonar, insuficiencia cardiaca , infarto de miocardio, sepsis, permanencia en regiones de gran altitud, ahogamiento, politraumatismos, aspiración de un cuerpo extraño, apnea del sueño, escoliosis, intoxicaciones por drogas o alcohol, inhalación de gases y humos, fibrosis pulmonar…etc.
Síntomas de una insuficiencia respiratoria
Se produce una d ificultad respiratoria, sensación de falta de aire, respiración agitada, acelerada, debilidad, incapacidad para realizar grandes esfuerzos , coloración azulada de la piel, confusión, somnolencia, mareo, puede haber hasta pérdida de conocimiento. También aceleración del ritmo del corazón con sensación de palpitaciones por taquicardia, y, en ocasiones, aparición de arritmias. A veces, según la causa de la insuficiencia respiratoria se puede realizar una autoescucha de ruidos respiratorios anormales (sibilantes, etc).
Tratamiento para la insuficiencia respiratoria
Los pacientes que presentan una insuficiencia respiratoria aguda reciben tratamiento en la urgencia hospitalaria o, si su gravedad así lo determina, en los servicios de cuidados intensivos.
El tratamiento fundamental es el aporte de oxígeno que, en casos de gravedad extrema, se realiza mediante una ventilación mecánica no invasiva (mediante CPAP, máquinas que por medio de una mascarilla amplia aportan una presión positiva al final de la espiración al paciente) o por ventilación invasiva con intubación.
Además, debe tratarse la enfermedad de base que produce la insuficiencia respiratoria de forma específica.
Pruebas complementarias del tratamiento de la insuficiencia respiratoria
Además de la exploración física y la anamnesis (interrogatorio clínico), que se le realiza al paciente, se puede realizar una prueba inicial básica e inocua que es la toma de la saturación de oxígeno en sangre con ayuda de un pulsioxímetro.
La prueba diagnóstica fundamental es la realización de una gasometría arterial , que ayuda a determinar a los médicos el tipo de insuficiencia respiratoria que sufre el paciente (hipóxica, hipercápnica o mixta), y la asociación con desequilibrios ácido-básicos de la sangre derivados.
Se puede acompañar para llegar al origen de la insuficiencia respiratoria con otras exploraciones como analítica de sangre, electrocardiograma , pruebas de imagen como radiografía de tórax, TAC torácico, ecocardiograma, angio-TAC pulmonar, determinación de tóxicos en orina…etc.
Factores desencadenantes de una insuficiencia respiratoria
Presencia de cortocircuitos en el corazón o en el sistema vascular periférico, que determinan que una fracción de sangre venosa (con dióxido de carbono), pasa a la circulación arterial oxigenada, bajando la oxigenación global de la sangre en mayor o menor medida.
Aparición de un desequilibrio entre la ventilación del pulmón y la perfusión sanguínea de su tejido.
Existencia de un bajo oxígeno inspirado , por ejemplo, si se inhalan tóxicos.
Lesiones neurológicas que disminuyan el mecanismo de la respiración y con ello la ventilación del pulmón por minuto.
Factores de riesgo de una insuficiencia respiratoria
Edad : la capacidad respiratoria, la pérdida de masa muscular, la disminución de la elasticidad de la caja torácica…etc, que se producen con el envejecimiento, pueden favorecer la aparición de una insuficiencia respiratoria en ciertas circunstancias.
Abuso de drogas o alcohol.
Tabaquismo .
Padecer traumatismos : caídas que afecten a la caja torácica.
Padecer enfermedades neurodegenerativas .
Padecimiento de enfermedades pulmonares y cardíacas .
Complicaciones de una insuficiencia respiratoria
Hipertensión pulmonar.
Enfermedad tromboembólica venosa.
Insuficiencia cardíaca.
Arritmias cardíacas.
Insuficiencia renal.
Alteraciones neurológicas.
Fallo multiorgánico.
Muerte.
Prevención de la insuficiencia respiratoria
No fumar, no tomar drogas.
Evitar inhalar humos y otros tóxicos.
Mantener medidas generales de higiene para prevenir la transmisión de infecciones (lavado de manos…etc).
Vacunarse.
Mantener una vida activa y una alimentación equilibrada.
Especialidades a las que pertenece la insuficiencia respiratoria
La insuficiencia respiratoria es un trastorno tratado por los médicos que trabajan en los servicios de urgencias (especialistas en medicina familiar, internistas…etc), por médicos intensivistas o por neumólogos.
Preguntas frecuentes:
¿Qué es la disnea respiratoria?
La disnea es un síntoma físico que describe la sensación de falta de aire , fatiga, de no poder respirar adecuadamente que tiene el paciente.
¿Qué es el asma?
El asma es una enfermedad crónica respiratoria producida por una hiperreactividad bronquial que deriva en la aparición de “ataques” de disnea o sensación de no respirar bien de duración variable, acompañada de tos, ruidos respiratorios como silbidos (sibilancias) y sensación de constricción debida al espasmo que se produce en los bronquios y cuyos precipitantes pueden ser varios.
¿Qué es la disnea de esfuerzo?
La disnea de esfuerzo es la sensación de dificultad respiratoria cuando se realiza algún esfuerzo como subir escaleras, hacer ejercicio físico, etc.
¿Qué es la disnea paroxística?
La disnea paroxística es una sensación de dificultad respiratoria abrupta que aparece en el paciente cuando este está acostado, tumbado en horizontal, y que le obliga a incorporarse y sentarse para poder volver a respirar bien.
¿Qué es la apnea?
Es una pausa o suspensión transitoria de la respiración a la que habitualmente le sigue una respiración forzada y más profunda.

Enfermedad
Hipotermia
¿Qué es la hipotermia?
Se denomina hipotermia a la disminución de la temperatura corporal por debajo de 35 grados centígrados. Aparece sobre todo en personas mayores o niños, en pacientes con patologías crónicas, personas que consumen drogas, o personas malnutridas, siendo frecuente también en personas que realizan deportes en zonas de altura (escalada, senderismo, etc). La gravedad del proceso depende de la severidad de la bajada de la temperatura corporal, llegando a ser una causa de muerte en su extremo.
Tipos de hipotermia
Según el mecanismo de producción de la hipotermia se define:
Hipotermia primaria : cuando un individuo sano es sometido a temperaturas ambientales muy bajas.
Hipotermia secundaria : aquella producida como consecuencia del proceso de afectación de una enfermedad, traumatismo o toma de sustancias.
Según la severidad de la hipotermia, se divide en:
Hipotermia leve : 35ºC a 32ºC.
Hipotermia moderada : 32ºC a 28ºC.
Hipotermia profunda: 20ºC a 14ºC.
Hipotermia extrema : menos de 14ºC.
Asimismo, también se puede clasificar según la rapidez de instauración de la hipotermia en:
Hipotermia aguda : cuando existe una exposición al frío grande y repentina, no dándole al cuerpo tiempo a compensarlo a pesar de que la producción del calor sea o esté casi al máximo.
Hipotermia subaguda : cuando se instaura de forma progresiva y el cuerpo lo compensa pero aparece agotamiento y disminución de las reservas energéticas y aparece la hipotermia.
Hipotermia crónica : cuando existe una exposición prolongada no muy severa al frío y las medidas corporales de control de temperatura son insuficientes o deficitarias (por ejemplo, en ancianos), por lo que después de días o semanas aparece una hipotermia.
Causas de hipotermia
El frío ambiental es la causa fundamental de la hipotermia con factores que influyen como el viento, la humedad, el tiempo de exposición a él y su intensidad. Otra causa física de la disminución de la temperatura es sumergirse en agua fría o mantenerse con ropas húmedas o mojadas en ambientes fríos.
Otras posibles causas son la exposición a métodos médicos como tratamientos quirúrgicos en quirófanos con mal control de la temperatura, sobre todo en cirugías con mayor exposición del interior corporal. También la administración de sueros y otros líquidos endovenosos con una temperatura baja.
Patologías como el hipotiroidismo mal controlado, la encefalopatía de Wernicke, la sepsis, o sufrir un traumatismo severo con lesiones graves, son factores causales. Igualmente la intoxicación por drogas y la desnutrición graven pueden producir una hipotermia.
Síntomas de hipotermia
Los primeros síntomas que presenta el paciente son los desencadenados como mecanismo compensador del organismo para aumentar la temperatura corporal: temblores, vasoconstricción cutánea, disminución del flujo de sangre que va a las zonas periféricas del cuerpo, aumento del flujo sanguíneo cerebral, aumento de la cantidad de orina (diuresis), aumento de la frecuencia cardíaca teniendo sensación de palpitaciones de la frecuencia respiratoria y de la tensión arterial.
Existen también alteraciones cardiovasculares que se presentan después del periodo de activación inicial, cuando progresa la hipotermia. En ese momento se inicia una disminución progresiva de la tensión arterial y la frecuencia cardíaca, así como de la cantidad de sangre que bombea el corazón. Además, aparecen alteraciones del ritmo del mismo, es decir, arritmias , que en algunos casos son muy graves y llevan a la asistolia del corazón (falta de latido).
De forma progresiva la hipotermia también provoca una disminución del estado de consciencia, con confusión, alteración del pensamiento, debilidad, falta de coordinación , etc, hasta poder sumir a la persona en una situación de coma profundo de forma progresiva, debido a la disminución del consumo de oxígeno (la hipotermia reduce el consumo de O2 del organismo al 50% aproximadamente cuando la temperatura corporal central llega a los 31ºC). Este mecanismo puede ser utilizado en determinadas circunstancias, para inducir una hipotermia controlada en pacientes en los que se quiere preservar la recuperación neurológica, que puede darse posteriormente cuando se restablece la temperatura corporal normal.
De forma progresiva también el ritmo respiratorio va disminuyendo (bradipnea), lo que finalmente puede producir un estado final de apnea (falta de respiración) y fallo respiratorio. Pueden aparecer otras alteraciones como la disminución del azúcar en sangre (hipoglucemia), alteración de la función del riñón, con un inicial aumento de la frecuencia miccional para posteriormente pasar a un estado de insuficiencia renal. Además, es posible que aparezcan alteraciones a nivel de las células de la sangre y una mayor predisposición a poder sufrir infecciones.
Cuando la hipotermia es leve, el cuerpo reacciona produciendo un aumento de contracciones musculares que producen la típica tiritona, cuyo fin es preservar y aumentar el calor corporal. Cuando la disminución de la temperatura es mayor, debido a la afectación neurológica, los músculos dejan de realizar este movimiento y la persona pasa a un estado de relajación muscular extrema no reactiva.
Tratamiento para la hipotermia
Cuando los pacientes con hipotermia se encuentran en un sitio con peligro lo primero que se debe hacer es poner a la persona en un sitio seguro, así como seco y caliente en la medida de lo posible y retirarle las ropas húmedas o mojadas, etc. En los pacientes con pérdida de consciencia, se realizan siempre las maniobras de reanimación cardiopulmonar (RCP).
Se debe iniciar un tratamiento de recalentamiento progresivo pudiendo aplicar medidas mecánicas externas como uso de mantas, toallas, ambiente con temperaturas altas (calefacción…etc), agua caliente, aparatos eléctricos, y bolsas de calor químico, entre otros. Además, se aplican tratamientos de fluidoterapia con administración de sueros y otros líquidos precalentados, y oxigenoterapia con administración de oxígeno humidificado caliente y, si es preciso, intubación y administración de respiración mecánica.
Así mismo, se deben tratar las enfermedades o alteraciones que hayan sido causantes o desencadenantes de la hipotermia, como el hipotiroidismo, el tratamiento de traumatismos, así como todas aquellas complicaciones que puedan surgir derivadas de la hipotermia (arritmias cardíacas, alteraciones del equilibrio ácido-básico interno…etc).
Pruebas complementarias del tratamiento de hipotermia
Ante la sospecha diagnóstica por los síntomas y signos que presenta el paciente, se debe objetivar la temperatura corporal central (determinada a nivel rectal, esofágica o timpánica).
Además, se registran otros signos vitales como ritmo cardíaco, tensión arterial, frecuencia respiratoria, entre otros.
Según el estado de evolución de la hipotermia, en ocasiones es preciso realizar pruebas diagnósticas como:
Analítica de sangre : con determinación de hemograma, coagulación, electrolitos, creatinina y glucosa. Además se realiza una gasometría arterial
Pruebas de imagen : como radiografía de tórax para detectar alteraciones pulmonares secundarias a la hipotermia.
También se realiza un electrocardiograma para detectar las alteraciones del ritmo del corazón.
Factores desencadenantes de la hipotermia
El factor desencadenante es una disminución de la temperatura ambiental o el padecimiento de enfermedades que afectan a la regulación de la temperatura corporal.
Factores de riesgo de hipotermia
La edad : los grupos de los extremos de la vida (niños y ancianos), tienen mayor riesgo.
Consumo de tóxicos : como el alcohol y otras drogas.
Padecer enfermedades : como el hipotiroidismo, lesiones de la médula espinal, anorexia…etc.
Realizar actividades deportivas sin adecuado vestuario, planificación y reservas de alimentos.
Toma de fármacos que pueden interferir en el mecanismo de control y regulación de la temperatura corporal (antidepresivos, antipsicóticos, analgésicos narcóticos y sedantes).
Estar en temporada invernal .
Complicaciones de la hipotermia
Muerte.
Congelación de tejidos del organismo.
Amputaciones de los tejidos muertos por congelación, sobre todo aquellos más distales como los dedos de los pies y de las manos etc.
Aparición de infecciones respiratorias y alteraciones anatómicas pulmonares secundarias al proceso de hipotermia y recuperación de la temperatura corporal.
Alteraciones cardíacas.
Prevención de hipotermia
Vestir siempre ropas adecuadas a la temperatura y el clima en cada época del año.
Evitar los ambientes fríos.
Cubrir la cabeza para prevenir la pérdida de calor a través de ella, usando gorras, sombreros, pañuelos, etc.
Realizar una adecuada alimentación variada y una correcta hidratación.
Durante el sueño, mantener caliente la temperatura ambiente de la habitación, sobre todo en niños y personas mayores.
Mantener la ropa seca.
Evitar bañarse en agua fría.
No consumir alcohol ni otros tóxicos.
Especialidades a las que pertenece la hipotermia
La hipotermia en muchos de los casos es tratada por médicos que trabajan en los servicios de emergencias y urgencias médicas, pudiendo ser estos médicos de familia, intensivistas, especialistas en medicina interna…etc.
Preguntas frecuentes:
¿Qué hacer si entras en estado de hipotermia?
Es fundamental conocer los síntomas que pueden aparecer en una persona con hipotermia para así ser conscientes, cuando nos hayamos en esa situación, de lo que está pasando. Siendo así, debemos, en ese momento, retirar ropas húmedas y protegernos del frío, intentando cubrirnos y arroparnos , aproximar las extremidades al cuerpo, beber líquidos y consumir alimentos ricos en azúcar y, ante todo, si se está en una circunstancia de riesgo, llamar a los servicios de emergencias (112).
¿En qué temperatura se considera que entras en hipotermia?
Con la disminución de la temperatura corporal por debajo de 35ºC.
¿Qué es la hipotermia en niños?
La hipotermia en niños es el descenso de su temperatura central tomada a nivel rectal por debajo de 35ºC.
¿Qué es la hipertermia?
Se define hipertermia como la elevación de la temperatura corporal por encima de 37.5ºC.
¿Qué produce una lipotimia?
La lipotimia es un desmayo o pérdida de conocimiento producido por una disminución del flujo de sangre al cerebro y con ello, la cantidad de oxígeno que precisa para funcionar adecuadamente.

Enfermedad
Bradipnea
¿Qué es la bradipnea?
La bradipnea es el término médico utilizado para referirse a la disminución de la frecuencia respiratoria por debajo de 12 respiraciones por minuto en adultos y de 30 respiraciones por minuto en niños . La bradipnea es un signo que puede aparecer de forma frecuente con el padecimiento de patologías graves, consumo de sustancias tóxicas, o ser inducida de forma controlada por fármacos en procesos de tratamiento médico. Es un signo que puede determinar la gravedad de un proceso patológico en el paciente.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tipos de bradipnea
Bradipnea en adultos : frecuencia respiratoria anormalmente lenta, por debajo de 10-12 respiraciones por minuto.
Bradipnea en niños : en menores lactantes se considera bradipnea aquella disminución de la frecuencia respiratoria por debajo de 30-40 respiraciones por minuto, y en niños escolares por debajo de 20 respiraciones por minuto.
Causas de la bradipnea
De una manera fisiológica sin riesgo vital para el paciente, en momentos de descanso y sueño, las personas pueden presentar periodos episódicos de bradipnea revertidos con normalidad en el momento de activación corporal. Esto igualmente le puede pasar a una persona que haga ejercicio físico intenso de forma habitual.
El consumo de ciertos fármacos como sedantes, opioides, analgésicos , etc, puede provocar la disminución de la frecuencia respiratoria. Asimismo, el consumo excesivo de alcohol puede producir una inhibición del centro respiratorio, y con ello la aparición de bradipnea, lo que ocurre también con otros tóxicos y drogas.
Además, toda enfermedad que produzca alteraciones neurológicas, como accidentes cerebrovasculares, tumores, etc, así como enfermedades degenerativas neuromusculares que llegan a paralizar los músculos que participan en los movimientos respiratorios, la pueden producir. Otras posibles causas son las alteraciones del sistema respiratorio , como infecciones, síndrome de apnea obstructiva del sueño y otras enfermedades crónicas que producen una obstrucción al paso adecuado del aire en los pulmones. También eventos traumáticos que dañen la caja torácica (fracturas de costillas, por ejemplo), o la disminución de la frecuencia cardíaca y otras alteraciones del corazón . Así mismo, otras patologías como las alteraciones de iones, hipotiroidismo, enfermedades hepáticas, alteraciones de la presión arterial entre otras, pueden producir este signo.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Síntomas de la bradipnea
La bradipnea puede ir asociada a la aparición de mareo, confusión, aturdimiento, o pérdida de conciencia, sensación de fatiga o falta de aire (disnea), coloración azulada de la piel, sobre todo de labios, manos y otras zonas distales del organismo, y sensación de cansancio o abatimiento.
Tratamiento para la bradipnea
El soporte fundamental del tratamiento de la bradipnea es el aporte de oxígeno cuando existe una disminución de su concentración en sangre. Si es preciso, se procede a la utilización de una respiración asistida con intubación.
Además, se debe tratar la base de la causa de la bradipnea, que será diferente dependiendo de su orígen (tratamiento del hipotiroidismo, de las enfermedades neurológicas, respiratorias, cardiológicas, etc).
Pruebas complementarias del tratamiento de la bradipnea
El diagnóstico de la bradipnea se obtiene mediante la exploración física , determinando cuántas inspiraciones y expiraciones (ciclo respiratorio completo), realiza el paciente.
Asimismo, se pueden realizar otras exploraciones complementarias para ver la repercusión en cuanto a la disminución de oxígeno en sangre que puede producir la bradipnea, o en búsqueda de la patología que está provocando la disminución de la frecuencia respiratoria. Para ello, muy frecuentemente es preciso realizar analítica de sangre, gasometría arterial y pruebas de imagen como radiografía de tórax, TAC o resonancia magnética. También puede precisarse la realización de una ecografía cardíaca o de un electrocardiograma.
Factores desencadenantes de la bradipnea
El factor desencadenante es la producción de un estímulo respiratorio neurológico disminuido por el padecimiento de una alteración o el consumo de una sustancia .
Factores de riesgo de la bradipnea
Realizar de forma habitual ejercicio de forma intensa.
Consumo de medicamentos y tóxicos que puedan afectar al centro respiratorio.
La edad avanzada.
La hipotermia (descenso de temperatura corporal).
El tabaquismo.
Padecimiento de patologías cardíacas.
Estados críticos como el shock.
Alteraciones iónicas de la sangre.
Traumatismos craneales.
Enfermedades neurológicas.
Consumo de tóxicos y drogas.
Enfermedades respiratorias.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Complicaciones de la bradipnea
Hipoxemia: déficit de oxígeno en sangre.
Pérdida de conocimiento.
Alteraciones del equilibrio ácido-base en el organismo.
Insuficiencia cardíaca.
Parada cardiorespiratoria.
Prevención de la bradipnea
Evitar el consumo de alcohol y drogas.
Realizar ejercicio físico adecuadamente.
Comer una dieta equilibrada con abundancia de frutas y verduras.
No fumar.
Vigilancia de tratamientos ansiolíticos y analgésicos puros.
Especialidades a las que pertenece la bradipnea
La bradipnea es una alteración que puede ser valorada y tratada en los servicios de urgencia hospitalaria, por médicos internistas, intensivistas, neumólogos, neurólogos…etc. según sea la circunstancia y la estabilidad del paciente que presenta este síntoma y la causa que lo produce.
Preguntas frecuentes:
¿Qué es la taquipnea?
Nos referimos a taquipnea cuando la frecuencia respiratoria es mayor a 20 respiraciones por minuto , asociada a movimientos respiratorios de gran amplitud.
¿Qué es la hipopnea?
Es la limitación parcial del paso del aire a los pulmones durante el sueño.
¿Qué es el SAOS grave?
El síndrome de apnea obstructiva del sueño es una alteración que produce un obstrucción momentánea y persistente de la vía aérea durante el descanso nocturno, lo que produce despertares frecuentes y mala recuperación y descanso que desencadena a alteraciones neurológicas, psiquiátricas, cardíacas y respiratorias con gran afectación de las funciones orgánicas en su extremo más grave.
¿Qué es el SAHS severo?
El síndrome de apnea-hipopnea del sueño grave es un término que, de la misma forma que el anterior, se utiliza para describir un cuadro clínico de somnolencia y trastornos neuropsiquiátricos y cardiorrespiratorios graves , secundarios a episodios repetidos de obstrucción de la vía aérea, que provocan que baje la concentración de oxígeno en sangre de forma transitoria desencadenando sucesivos despertares a lo largo del periodo de sueño, lo que desencadena un descanso no reparador. Cuantas más interrupciones en la respiración y descanso del paciente, más severa es la afectación orgánica y psíquica que posteriormente desarrolla este.
¿Qué es la apnea del sueño?
La apnea del sueño es un trastorno en el cual la respiración se detiene para reiniciarse posteriormente en repetidas ocasiones mientras la persona duerme.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Enfermedad
Tos Ferina
¿Qué es la tos ferina?
La tos ferina es una infección de las vías respiratorias que provoca tos intensa acompañada de un sonido agudo al respirar (es el llamado “gallo” de la tos ferina), también conocida como tosferina, tos convulsa, pertussis o coqueluche. Se trata de una enfermedad muy contagiosa que afecta al ser humano a nivel mundial, aunque es más frecuente en niños no vacunados. La posibilidad de contagio aumenta durante las dos primeras semanas de aparecer los primeros síntomas. En España, es una enfermedad de declaración obligatoria individualizada que se presenta frecuentemente y considerada grave, y muy grave en bebés menores de seis meses.
Tipos de tos ferina
No existen tipos diferentes de tos ferina
Causas de la tos ferina
La tos ferina está causada por la bacteria Bordetella Pertussis , se contagia al inhalar secreciones de saliva con gérmenes, expulsadas al hablar o toser, y que se adhieren a las vías respiratorias.
Síntomas de la tos ferina
Los síntomas de la tos ferina son muy parecidos a los de un resfriado común y pueden permanecer hasta siete semanas (la tos incluso puede continuar meses después). Los primeros síntomas pueden durar hasta dos semanas y suelen consistir en m oqueo, tos leve, apnea en bebés, fiebre baja y lagrimeo. Posteriormente, la tos empeora y se vuelve convulsiva, dificultando la respiración y provocando un sonido ruidoso al inspirar llamado comúnmente, “gallo”. También pueden aparecer vómitos, esputos mucosos, ojos y cara enrojecida, angustia y fatiga . Inclusive, es posible perder el conocimiento durante los ataques de tos.
En recién nacidos no suele existir el “gallo” y es habitual padecer crisis graves de apnea que pueden llegar a provocar la muerte del bebé u otras complicaciones respiratorias y neurológicas.
Lo síntomas acaban desapareciendo de forma lenta y gradual.
Tratamiento para la tos ferina
El tratamiento de la tos ferina se lleva a cabo en casa mediante el mantenimiento de reposo y el suministro de antibióticos para acabar con la bacteria. En el caso de bebés es común la hospitalización para recibir el tratamiento y vigilar al menor, ya que es más habitual que existan complicaciones.
Se desaconseja el uso de medicamentos contra la tos.
El uso de humidificadores o vaporizadores de vapor frío y soluciones salinas nasales son útiles para despejar la mucosidad de las vías respiratorias.
Se recomienda beber abundante líquido , incluso puede ser necesario administrarlos por vía venosa en el caso de niños muy pequeños.
En ocasiones se emplea la oxigenoterapia complementaria , sobre todo en los pacientes más pequeños a quienes la tos les provoca apnea.
Pruebas complementarias del tratamiento de la tos ferina
La tos ferina suele ser fácil de diagnosticar, pero en ocasiones puede ser necesario acudir a pruebas complementarias como un cultivo nasofaríngeo para buscar evidencias de la bacteria, un análisis de sangre para comprobar la cantidad de glóbulos blancos o una radiografía de tórax para confirmar si existen complicaciones o infecciones respiratorias.
Factores desencadenantes de la tos ferina
Cualquier alteración del medio ambiente puede desencadenar los ataques paroxísticos o bruscos típicos de la tos ferina; tales como el humo, polvo, ruidos o cambios de temperatura. Si se sufre tos ferina, se deben evitar los ambientes contaminados.
Factores de riesgo de la tos ferina
El principal factor de riesgo para contraer la tos ferina es no estar vacunado y exponerse a personas ya infectadas.
Se tiene mayor riesgo en edades tempranas (sobre todo antes del primer año de vida), durante el embarazo y si se vive en condiciones poco higiénicas.
Complicaciones de la tos ferina
La tos ferina puede derivar en ciertas complicaciones, sobre todo debidas al gran esfuerzo realizado continuamente al toser o provocados por la falta de oxígeno:
Problemas respiratorios: bronquitis, neumonía, otitis…
Enfermedades neurológicas: encefalopatía tosferinosa, hipoxia y daño cerebral, etc.
Hemorragias: nasales, cerebrales….
Hernia inguinal o abdominal.
Prolapso rectal.
Deshidratación en bebés.
Apnea.
Convulsiones.
Muerte.
Prevención de la tos ferina
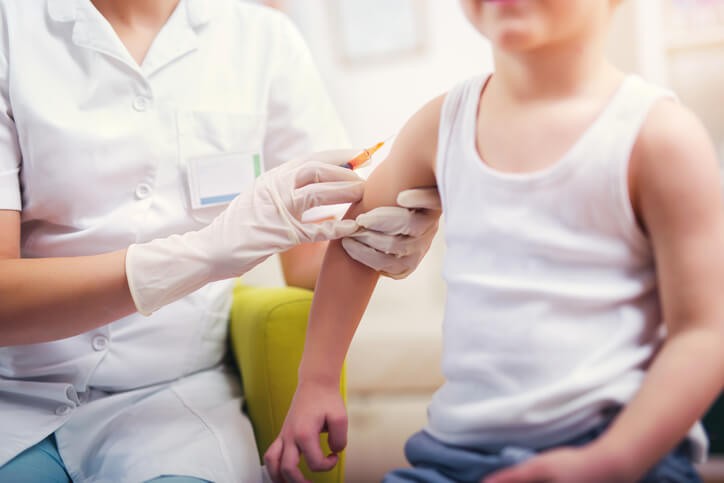
La prevención de esta enfermedad se lleva a cabo mediante la inmunización con la vacuna de la tos ferina ; la vacuna DTPa en niños y la Tdap en adolescentes y adultos según el siguiente esquema de administración:
3 dosis de vacuna DTPa a los 2, 4 y 6 meses.
2 dosis de recuerdo, una a los 15-18 meses y otra a los 6 años.
Posteriormente, una dosis de recuerdo de la vacuna Tdap cada 10 años.
Mujeres gestantes entre la semana 27 y 36 del embarazo.
Especialidades a las que pertenece la tos ferina
La tos ferina pertenece a la especialidad médica de otorrinolaringología o bien la neumología.
Preguntas frecuentes:
¿Cuándo se pone la vacuna de la tos ferina?
La vacuna de la tos ferina se recomienda ser administrada en cinco dosis antes de cumplir los 6 años (una dosis a los 2, 4 y a los 6 meses, la de refuerzo a los 15-18 meses y otra a los 6 años), posteriormente se debe administrar una vacuna recordatoria cada 10 años.
También se aconseja vacunarse a mujeres embarazadas (a partir de la semana 27 de gestación) y a toda persona que vaya a tener contacto directo y continuado con niños.
¿Cuánto tiempo puede durar la tos ferina?
La enfermedad de la tos ferina puede durar hasta 7 semanas o incluso meses . Durante las dos primeras semanas se desarrolla el proceso de incubación, generalmente sin síntomas. Después, la fase catarral dura unas 2 semanas y la fase paroxística (repentina) con los prolongados ataques de tos se extiende de 4 a 8 semanas para llegar al período de convalecencia, donde hay un declive de la tos, y puede continuar 2 o 4 semanas más, incluso prolongarse durante meses.
¿Cómo se puede contagiar la tos ferina?
La bacteria de la tos ferina se contagia manteniendo contacto directo con otra persona afectada. El proceso de contagio se lleva a cabo a través de diminutas gotas de fluido de la boca o nariz que son expulsadas al toser o hablar y se inhalan al respirar, adhiriéndose a las vías respiratorias.
Es más fácil contagiarse durante las primeras semanas de la enfermedad.
¿Qué es la vacuna Tdpa?
La vacuna Tdpa es la vacuna que protege a personas adolescentes y adultas de enfermedades como la difteria, el tétanos y la tos ferina. Es una vacuna de recuerdo y es de menor carga que la vacuna DTPa que se administra a niños y bebés para protegerlos de las mismas afecciones.
Si estoy embarazada… ¿Cuándo tengo que vacunarme de la tosferina?
El comité Asesor de Vacunas de la AEP recomienda vacunarse de la tos ferina a mujeres embarazadas para proteger al bebé en los primeros meses de vida. Debe administrarse durante el tercer trimestre de la gestación (entre las semanas 27 y 36) y debe repetirse en cada embarazo.

Enfermedad
Tromboembolismo Pulmonar
¿Qué es el tromboembolismo pulmonar?
El tromboembolismo pulmonar es la obstrucción de una arteria pulmonar, que se produce por la situación de un coágulo en la arteria o por la migración de un coágulo que, formado en una vena, llega hasta la arteria pulmonar a través del torrente sanguíneo. En un 95% de los casos es una vena de los miembros inferiores. Se producen unos 145 casos por cien mil habitantes con una mortalidad que llega a ser de entre el 2 y el 10%. Es una enfermedad grave que supone una urgencia médica, necesitando en muchos casos el ingreso en UVI.
Tipos de tromboembolismos
Tromboembolismo pulmonar agudo : es el que se produce en un momento dado, que se trata de modo adecuado con anticoagulantes revirtiendo el coágulo o émbolo
Tromboembolismo pulmonar crónico : es el que se mantiene la obstrucción arterial, a pesar del tratamiento adecuado con anticoagulantes, durante más de tres meses.
Causas del tromboembolismo pulmonar
El tromboembolismo pulmonar en un 95% es secundario a un proceso de trombosis venosa profunda. También puede ser causado por un émbolo graso en caso de fracturas de huesos largos como el fémur, o por embolismos gaseosos.
Síntomas de de tromboembolismo pulmonar
Los síntomas del tromboembolismo pulmonar serán disnea, taquipnea ( aumento de la frecuencia respiratoria), ansiedad, dolor torácico agudo, mareos , desvanecimientos, tos con sangre, y además puede observarse cianosis y disminución de oxígeno en la sangre.
Tratamiento para el tromboembolismo pulmonar
El tratamiento del embolismo pulmonar es con anticoagulantes , primero con inyección intravenosa de Heparina durante unos 10 días. Posteriormente se puede pasar a inyecciones de Heparina subcutánea, y más tarde se deberá mantener tratamiento con anticoagulantes orales durante al menos seis meses.
En casos más graves o en enfermos que no pueden recibir tratamiento anticoagulante se procederá a la fibrinolisis , que es la disolución del coágulo. Pacientes que tienen episodios de repetición, pueden necesitar de la colocación de un filtro en la vena cava inferior, que impida la llegada del coágulo hacia los pulmones, dicho filtro se coloca a través de la vena femoral, llegando con el catéter hasta la vena cava inferior, donde se sitúa el filtro.
Pruebas complementarias del tratamiento de tromboembolismo pulmonar
Las pruebas complementarias serán, en primer lugar, una analítica de sangre con dímero D y niveles de oxígeno.
Se realizará también un electrocardiograma de control, que permitirá descartar el origen cardíaco de la disnea.
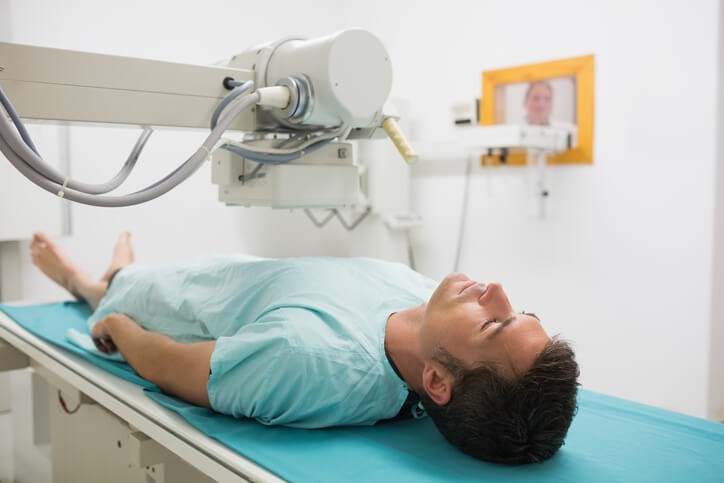
Las pruebas de imagen serán una radiología de tórax y más tarde la angiografía por medio de TAC ( ANGIO-TAC). La gammagrafía de ventilación/perfusión prácticamente se realiza solo en casos especiales en los que no se puede usar medio de contraste por alergias o embarazo.
Factores desencadenantes del tromboembolismo pulmonar
El factor de desencadenante es la hipercoagulabilidad de la sangre.
Factores de riesgo de tromboembolismo pulmonar
Los factores de riesgo para un tromboembolismo pulmonar serán los traumatismos graves, la cirugía abdominal o pélvica, las varices en miembros inferiores y/o las fracturas en los miembros inferiores.
El cáncer predispone al tromboembolismo pulmonar, en especial los linfomas y las leucemias, el cáncer de pulmón, los cánceres gastrointestinales, el cáncer de páncreas y los tumores del sistema nervioso central.
Se puede producir por problemas en la coagulación de origen genético , como es la alteración del factor V de Leiden y la alteración del gen de la protrombina.
En pacientes con lupus, los anticuerpos antifosfolípidos y el anticuerpo lúpico pueden favorecer también este proceso.
En mujeres en edad fértil serán los anticonceptivos hormonales y el embarazo las dos causas principales
Complicaciones del tromboembolismo pulmonar
Infarto pulmonar.
Alteración del intercambio gaseoso pulmonar.
Hipertensión pulmonar.
Trombo mantenido.
Prevención de tromboembolismo pulmonar
Uso de anticoagulantes orales o inyectables en pacientes de riesgo.
Uso de medias de compresión en pacientes con varices en miembros inferiores.
Control de tratamiento anticonceptivo.
Control del embarazo.
Especialidades a las que pertenece el tromboembolismo pulmonar
El tromboembolismo pulmonar se deberá controlar por parte de médicos intensivistas o bien por neumólogos y hematólogos.
Preguntas frecuentes:
¿Qué es un coágulo pulmonar?
Un coágulo pulmonar es la formación de un coágulo que normalmente se produce ante la rotura de una vénula o una arteria para taponar y evitar el sangrado, en una situación anómala, dando lugar a la obstrucción de una arteria o una vena pulmonar.
¿Qué es una embolia y cómo se produce?
La embolia se da cuando un coágulo, ya sea sanguíneo, de grasa, o de gas, viaja a través del sistema venoso o arterial y obstruye una arteria o vena de menor calibre de la arteria o vena donde se originó.
¿Cuál es la diferencia entre trombosis y embolia?
La diferencia es en el inicio de su formación, pero la clínica y por tanto los síntomas son los mismos y el tratamiento es similar. El trombo se forma directamente en el territorio afectado , en tanto que la embolia se formó en otro territorio, pero llega un punto en que obstruye un determinado territorio arterial o venoso.
Un trombo se puede convertir en un émbolo, cuando no se queda fijo, sino que se traslada hacia otro territorio.
¿Cómo se forman los coágulos en la sangre?
Los coágulos en la sangre se forman a través de un sistema complejo conocido como cascada de coagulación . En un inicio lo que se produce es la unión de las plaquetas entre sí, que da lugar a una secreción de sustancias químicas, que da lugar a que acudan más plaquetas, y así posteriormente la sustancia de la cascada de la coagulación da lugar a la llegada de la fibrina, haciendo una estructura que sella la zona de sangrado, cuando el punto de sangrado sana el organismo pone en funcionamiento otras sustancias, que dan lugar a la disolución del coágulo.
¿Qué es la embolia en las piernas?
La embolia en las piernas es la obstrucción arterial o venosa, que se produce por la llegada de un coágulo que se ha formado en otro lugar, si la embolia es arterial, se produce una situación grave, de falta de aporte de sangre y por tanto de nutrientes y oxígeno, que puede dar lugar a la pérdida de la extremidad.
Enfermedad
Neumotórax
¿Qué es un neumotórax?
El neumotórax también conocido como colapso pulmonar, se define como la presencia de aire en el espacio pleural. Se produce cuando el aire se filtra dentro del espacio que se encuentra entre los pulmones y la pared torácica (espacio pleural). El aire hace presión en la parte externa del pulmón y lo hace colapsar. Es común que se presente en pacientes sin enfermedad pulmonar anterior. Es más frecuente en hombres que en mujeres, entre los 20 y 40 años y el riesgo puede aumentar si la persona es fumadora. Es una condición que puede ser grave y si no se trata a tiempo puede ocasionar la muerte.
Tipos de neumotórax
El tipo de neumotórax depende de la causa que lo produzca. Estos pueden ser:
Neumotórax espontáneo: es aquel que ocurre en ausencia de antecedente traumático o iatrogénico que lo justifique, es decir que se produce cuando no se da ningún motivo aparente de que ocurra. Este se clasifica en neumotórax espontáneo primario y secundario.
Neumotórax espontáneo primario : Ocurre en individuos aparentemente sanos, sin enfermedades pulmonares conocidas. Neumotórax espontáneo secundario: afecta a paciente con una enfermedad pulmonar previa o preexistente, como la enfermedad pulmonar obstructiva crónica (EPOC), neumonías, fibrosis quística, asma bronquial, infección etc.
Neumotórax adquirido o espontáneo que se divide en neumotórax traumático y neumotórax yatrogénico.
Neumotórax traumático: se produce por causas externas al propio organismo, ya sea por ataque con armas blancas o accidentes de tránsitos. Suele producirse conjuntamente con un hemotórax. es decir, la acumulación de sangre entre los pulmones y la pared torácica. Se produce como consecuencia de un traumatismo torácico abierto o cerrado. Neumotórax traumático abierto: es consecuencia de una herida penetrante en el tórax que pone en comunicación el espacio pleural y la atmósfera exterior (entrada de aire atmosférico), y a su vez suele lesionar también el pulmón (salida de aire alveolar). Neumotórax traumático cerrado : está causado habitualmente por una fractura costal, rotura bronquial, o lesión esofágica.
Neumotórax yatrógeno: se produce como consecuencia de una maniobra diagnóstico-terapéutica, es decir, durante una intervención médica para tratar al paciente. Como la punción transparietal (biopsia de la pleura), la toracoscopia (exploración en el interior del pulmón) o pacientes con respirador artificial.
Causas del neumotórax
El neumotórax puede causarse por cualquier lesión o contusión penetrante en el pecho, dichas lesiones pueden presentarse en accidentes automovilísticos, agresiones físicas, o accidentes durante intervenciones médicas . En algunos casos el neumotórax puede ser causado por ampollas de aire o bullas , que se rompen enviando el aire al espacio que rodea el pulmón.
Las personas altas y delgadas y los fumadores tienen mayores probabilidades de sufrir un neumotórax. También algunas enfermedades pulmonares pueden causar un colapso pulmonar, como son, el asma, fibrosis quística, neumonía, enfermedad pulmonar obstructiva crónica.
Síntomas del neumotórax
Los síntomas del neumotórax pueden incluir:
Dolor en el área torácica.
Dificultad para respirar.
Tos.
Dolor de hombro.
Taquicardia. Hipotensión.
Coloración azulada debido a la falta de oxígeno.
Shock y colapso. Entre otros síntomas.
Tratamiento para el neumotórax
El objetivo para el tratamiento del neumotórax consiste en extraer el aire de la cavidad pleural, aliviar la presión en el pulmón y permitir que se vuelva a expandir. Si una zona más grande del pulmón ha colapsado, es posible que se utilice una aguja o una sonda pleural para eliminar el exceso de aire , llamado toracentesis por aspiración con aguja. La sonda o aguja se inserta entre las costillas para llegar al espacio de aire que está presionando el pulmón colapsado.
Toracostomía cerrada , que consiste en introducir un tubo en la cavidad pleural a través de un espacio intercostal de la pared torácica y conectarlo a una máquina de aspiración con succión pleural permanente.
Si la sonda pleural no funciona, es necesario realizar una cirugía para cerrar la fuga de aire. La cirugía puede realizarse a través de pequeñas incisiones, usando una pequeña cámara de fibra óptica, y herramientas quirúrgicas estrechas de mango largo, llamada toracoscopia.
Pleurodesis química : se realiza para tratar el colapso pulmonar y evitar episodios futuros, se hace mediante la aplicación de sustancias irritantes en la cavidad pleural para lograr una adhesión permanente de las pleuras parietal y visceral. Esta técnica está indicada en pacientes con el escape de aire ya esté controlado.
Pruebas complementarias del tratamiento del neumotórax
Para el diagnóstico y tratamiento del neumotórax es necesario realizar pruebas como, una radiografía de tórax o una tomografía computarizada.
Factores desencadenantes del neumotórax
No existen factores desencadenantes del neumotórax.
Factores de riesgo del neumotórax
Los factores de riesgo van a depender del tipo de neumotórax, como son:
El consumo de tabaco: el riesgo aumenta por la cantidad de tiempo que tiene fumando y de cuántos cigarrillos se fuma.
El sexo: los hombres tienen mayor probabilidad de tener neumotórax que las mujeres.
La edad: el tipo de neumotórax espontáneo, provocado por ampollas de aire rotas tiene más probabilidad de ocurrir en personas entre los 20 y los 40 años, en especial, si la persona es muy alta y tiene bajo peso.
Enfermedad pulmonar: tener una enfermedad de base, como fibrosis quística, enfermedad pulmonar obstructiva crónica, asma etc.
Neumotórax anterior: cualquier persona que haya tenido un neumotórax anterior tiene mayor probabilidad de tener otro.
Ventilación mecánica: las personas que necesitan ventilación mecánica para asistir su respiración, por la presión de aire que este produce en el pecho el pulmón puede colapsar, como es el caso del neumotórax iatrogénico
Complicaciones del neumotórax
Aparición de otros neumotórax en el futuro, son poco frecuente pero potencialmente grave.
Shock hemodinámico (si existen lesiones o infecciones graves, inflamación grave o si presenta líquidos en los pulmones).
Insuficiencia respiratoria.
Prevención del neumotórax
No existe una forma de cómo prevenir el neumotórax, pero si se puede ayudar a prevenir los factores de riesgo para la aparición del neumotórax como son:
Dejar de fumar, puede ayudar a disminuir la aparición del neumotórax.
Tratar las formas secundarias del neumotórax se pueden prevenir con un tratamiento adecuado de las enfermedades pulmonares.
Especialidades a las que pertenece el neumotórax
La especialidad médica que trata el neumotórax en la neumología, es la que se encarga del estudio de las enfermedades del aparato respiratorio, tanto de los pulmones como de las vías respiratoria.
Preguntas frecuentes
¿Cuáles pueden ser las secuelas de un neumotórax?
Por lo general no suelen quedar secuelas de un neumotórax. Pero no se crean adherencia pleurales e insuficiencias cardio-respiratoria.
¿Qué es la fibrosis quística?
La fibrosis quística es una enfermedad crónica y hereditaria, también degenerativa que afecta a los pulmones y al sistema digestivo. Se caracteriza por congestión pulmonar, así como la infección y mala absorción de nutrientes por parte del páncreas. Es más común en niños y adultos jóvenes y es una enfermedad potencialmente mortal.
¿Qué es un colapso de pulmón?
Un colapso de pulmón, también conocido como neumotórax, es una condición que ocurre cuando aire entra en el espacio pleural (espacio entre la pared del pecho y el pulmón). A medida que el aire aumenta, la presión dentro del espacio pleural aumenta y causa el colapso del pulmón . La presión también impide que el pulmón se expanda cuando intentas inhalar, causando dolor en el pecho y falta de aliento.
¿Qué es un neumotórax yatrógeno?
Un neumotórax yatrógeno, se produce como consecuencia de una maniobra diagnóstico-terapéutica, es decir, que es provocado por una complicación durante una intervención médica para tratar al paciente. Como la punción transparietal (biopsia de la pleura), la toracoscopia (exploración en el interior del pulmón) o pacientes con respirador artificial.
Enfermedad
Lepra
¿Qué es la lepra?
La lepra o enfermedad de Hansen (el médico noruego Gerhard Armauer Hansen en 1873 descubrió el microorganismo que la produce), es una enfermedad crónica producida por la bacteria Mycobacterium leprae, que afecta en su expresión primaria a los nervios periféricos y de forma secundaria a la piel y a otros tejidos. Es una enfermedad de distribución mundial que afecta de forma endémica en regiones de Asia y Sudamérica. Se trata de una patología grave por sus posibles repercusiones y complicaciones.
Tipos de lepra
La lepra se divide según su estado de presentación y el estado de las defensas del paciente en:
Lepra indeterminada : estadío precoz y transitorio.
Lepra tuberculoide : ocurre en pacientes con inmunidad o defensas activas.
Lepra borderline tuberculoide .
Lepra borderline lepromatosa .
Lepra lepromatosa : la que ocurre en pacientes con inmunidad alterada. En las lesiones dérmicas se encuentran muchas bacterias.
Causas de la lepra
La causa de la enfermedad es la infección por la bacteria Mycobacterium leprae, cuyo reservorio es el ser humano. La transmisión se produce por el contacto entre personas a través de gotas nasales infecciosas. La transmisión a través de las lesiones cutáneas es más rara.
Síntomas de la lepra
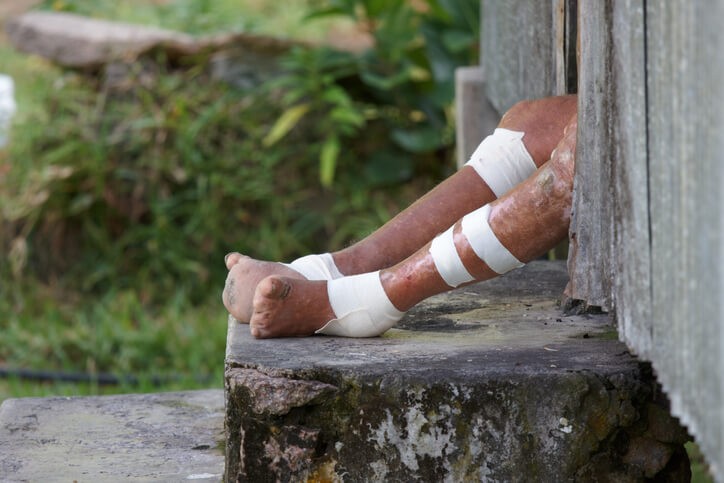
La forma de inicio es la Lepra indeterminada, afectando más a niños. Aparecen lesiones dérmicas a modo de manchas rojizas o con disminución del color (hipocrómicas), redondeadas y con bordes mal definidos. Se localizan en la espalda, en la parte superior de los brazos, en los muslos y en las nalgas. En las lesiones existe una alteración de la sensibilidad al calor y al dolor . Un 75% de los pacientes evoluciona a la curación tras meses o años.
La lepra tuberculoide es la más frecuente. Aparecen un número escaso de lesiones en la piel, ovaladas de color rojizo parduzco, con bordes bien definidos y con la región central más clara, que surgen en nalgas, tronco, hombros muslos y cara. En las lesiones no existe sensibilidad en esa piel, ya que existe un engrosamiento de los troncos nerviosos periféricos que además produce parálisis de la musculatura .
La lepra lepromatosa es la forma más grave y contagiosa. Las lesiones que aparecen de forma simétrica son pequeñas manchas (máculas) rojizas con bordes difusos y superficie brillante. Otra de las lesiones son nódulos o leproma, que son las lesiones más características. Son pequeñas tumoraciones de hasta 3-4 cm, duras y recubiertas por una piel alterada (atrófica, rojiza o roja parduzca). En estas lesiones también está comprometida la sensibilidad de la piel. Además, es frecuente que estas lesiones se ulceren. Es típica la afectación del tracto respiratorio superior, los ojos y la pérdida del vello corpora l, incluyendo las cejas y pestañas, y la deformación del tabique nasal.
Tratamiento para la lepra
El tratamiento de la lepra comprende medidas generales para proteger las áreas en las que el paciente no tiene sensibilidad. Se le explican al paciente los cuidados y prevenciones que debe llevar a cabo para evitar contagios, así como se atiende a las alteraciones psicológicas y sociales que puede padecer de forma crónica.
La pauta del tratamiento farmacológico según el tipo de presentación clínica es:
En la lepra tuberculoide (y la borderline tuberculoide), se pautan dos antibióticos por vía oral , Dapsona y Rifampicina , en distintas pautas de dosificación, manteniendo este tratamiento durante 6-9 meses.
En la lepra lepromatosa (y la borderline lepromatosa), se indica la toma de Clofazimina , Dapsona y Rifampicina , en distintas pautas de dosificación manteniendo este tratamiento durante 24-36 meses.
Pruebas complementarias del tratamiento de la lepra
A parte de la entrevista clínica y la exploración física, se procede a la toma de muestras para su estudio. Así, se coge una muestra del borde de las lesiones para la visualización directa mediante el uso de un colorante de la bacteria presente en el tejido. Además, se pueden realizar biopsias cutáneas (toma de un pequeña porción de tejido alterado), para su estudio por el laboratorio de anatomía patológica y la detección de bacterias. En ocasiones, para diferenciar en qué estadío de la enfermedad está el paciente, se realiza una prueba llamada prueba de la lepromina , con la inyección cutánea de una suspensión de la bacteria de forma inactiva, desencadenando una reacción en la piel característica de cada fase.
Factores desencadenantes de la lepra
El factor desencadenante es el contacto con las secreciones del aparato respiratorio de un paciente enfermo, cuando se establece un contacto cercano y prolongado.
Factores de riesgo de la lepra
Condiciones socioeconómicas bajas.
Hacinamiento.
Bajo grado de escolarización.
Mala higiene e insalubridad.
Desnutrición.
Inmunidad alterada (disfunción de las defensas).
Convivencia con un enfermo de lepra.
Alteraciones metabólicas.
Complicaciones de la lepra
Leprorreacciones : cambios bruscos en la estabilidad clínica del enfermo producidas como consecuencia de una alteración del estado de las defensas del paciente. Existen dos tipos:
Tipo I: aparecen edemas en las lesiones cutáneas y hay mayor afectación neurológica.
Tipo II: aparecen edemas en las lesiones cutáneas y hay mayor afectación neurológica. En la II existen alteraciones cutáneas importantes con aparición de múltiples placas y nódulos, que pueden sufrir grandes ulceraciones, además de surgir mayor inflamación de los nervios periféricos y dolor, acompañado de fiebre y malestar general. Pueden verse afectados los músculos, el hígado, lo ganglios linfáticos, los testículos…etc.
Alteración psiquiátrica: depresión, ansiedad…etc.
Pérdida de visión por la afectación ocular.
Obstrucción nasal, sinusitis crónica y epistaxis (sangrado nasal).
Aislamiento social.
Pérdida de piezas dentales.
Afectación renal.
Prevención de la lepra
Tratamiento o quimioprofilaxis de las personas que conviven con enfermos en la forma más contagiosa, la lepra lepromatosa, administrando un antibiótico , la Sulfona , durante un tiempo prolongado.
Realizar un tratamiento precoz de aquellas personas infectadas para disminuir el riesgo de contacto.
Especialidades a las que pertenece la lepra
La lepra es una enfermedad que puede ser valorada y tratada por el dermatólogo, por el médico de enfermedades infecciosas, el neumólogo, el oftalmólogo, o el neurólogo, en muchas ocasiones de forma conjunta, según la afectación del paciente.
Preguntas frecuentes:
En la actualidad… ¿Sigue existiendo la lepra?
Sí, aparece sobre todo en regiones tropicales y subtropicales. En Europa su aparición está limitada a los países de la cuenca mediterránea.
¿Cómo se contagia la lepra?
La lepra se contagia a través del contacto persona a persona, por medio del contacto con las secreciones respiratorias (mucosidad, goteo nasal, o al estornudar).
En la actualidad… ¿Tiene cura la lepra?
Sí, se utilizan varios antibióticos de forma conjunta (sinérgica) para evitar la aparición de resistencias. El tratamiento se debe mantener hasta que se objetiva mediante análisis que las lesiones cutáneas no presentan bacterias.
¿En qué países es más propensa la gente a contraer la lepra?
Las zonas donde la lepra aparece de forma endémica sobre todo son Asia y América del sur. En Europa, su mayor incidencia aparece en España y Portugal.
¿Qué es la enfermedad de Hansen?
La enfermedad de Hansen es otra forma de denominar a la lepra . Hace referencia al nombre de este médico noruego que descubrió a la bacteria que produce la lepra, el médico noruego Gerhard Armauer Hansen.

Enfermedad
Linfoma
¿Qué es un linfoma?
El linfoma es una tumoración maligna que parte de los linfocitos T o B. El linfoma no Hodgkin se da en 12,3 varones cada 100.000 y en 10,8 cada 100.000 mujeres. En cuanto al linfoma de Hodgkin, este se da en 2.5 varones de cada 100.000 y en 2,1 mujeres de cada 100.000. El aumento de los ganglios linfáticos puede dar lugar a la compresión de estructuras produciendo tos o dolor. Es una enfermedad grave.
Tipos de linfomas
Linfoma no Hodgkin : es el más frecuente y se suele dar más en adultos.
Linfoma Hodgkin : es más raro y tiene dos picos de edad entre los 15 y 40 años y a partir de los 55 años.
Causas de un linfoma
En el linfoma de Hodgkin no se ha encontrado una causa del mismo, puede tener relación con infecciones como pueden ser el virus de Epstein Barr , pero no se ha podido demostrar una relación directa.
En el linfoma de no Hodgkin tampoco hay una causa clara, si bien aumenta con la edad y enfermedades como VIH, hepatitis C y enfermedades del tejido conectivo.
Síntomas de un linfoma
Los síntomas suelen ser pocos, hay aumento de uno o varios ganglios linfáticos, fiebre, pérdida de peso y sudoración profusa . Estos síntomas pueden aparecer hasta en la mitad de los pacientes, y hasta un 10% de ellos puede sentir malestar general y picor.
Tratamiento para el linfoma
Los tratamientos para los linfomas serán diferentes según el tipo de linfoma y el estadio en que este se encuentre, pero serán necesarias quimioterapia y radioterapia , y, en muchos casos, también un transplante de médula posterior.
La radioterapia de campo afectado en la que se irradia la zona ganglionar afectada, con los nuevos sistemas de radiación se puede dar sobre la zona afectada con poca repercusión en las células sanas de alrededor.
la quimioterapia utiliza los fármacos Adriamicina, Bleomicina, Vinblastina, Dacarbazina (ABVD): es el tratamiento estándar en casi todos los estadios.
En los linfomas progresivos o recurrentes se va a realizar un trasplante de células madres con células autólogas, esto es, del mismo individuo, se adquieren desde su médula ósea, tras tratamiento con altas dosis de quimioterapia y radioterapia.
Pruebas complementarias del tratamiento del linfoma
Las pruebas complementarias de linfoma serán la biopsia ganglionar con aguja fina o aguja gruesa, para poder observar las células en el laboratorio, analítica de sangre completa y biopsia de médula ósea. Pruebas de imagen como radiología de tórax, escáner toraco-abdominal y pélvico, y un estudio del sistema nervioso central con escaner y con estudio del líquido cefalorraquídeo puede ser necesario para ver la extensión de la enfermedad.
Factores de riesgo del linfoma
Los factores de riesgo son: tratamientos con radioterapia, quimioterapia, pacientes trasplantados, infecciones por virus de Epstein Barr , hepatitis C, enfermedades del tejido conectivo como lupus, o enfermedad mixta del tejido conectivo.
Complicaciones del linfoma
Infecciones.
Anemia.
Problemas respiratorios.
Dolor en abdomen o espalda.
Prevención del linfoma
Ya que no hay causas ni factores claros de riesgo, podemos decir que no se puede prevenir.
Especialidades a las que pertenece el linfoma
El linfoma estará en control tanto bajo del hematólogo como del oncólogo
Preguntas frecuentes:
¿Qué es un linfoma en el cuello?
Un linfoma en el cuello es el linfoma que afecta los ganglios linfáticos del cuello. Esto produce como sintomatología que el paciente presenta áreas del mismo claramente inflamadas e induradas a la palpación.
¿Qué es el cáncer linfático?
El cáncer linfático es el que afecta a los órganos linfáticos , son los linfomas, y se llaman así porque pueden afectar a los ganglios, pero también a otras zonas del sistema linfático como son amígdalas, bazo o timo, e incluso zonas como estómago, intestino, donde también se hallan células de defensa del organismo.
¿Qué es un linfoma no Hodgkin en adultos?
El linfoma no Hodgkin es un linfoma que afecta preferentemente a adultos , y que es el más frecuente de todos. Ocupa el séptimo lugar en incidencia de cáncer en población total y es la novena causa de muerte por cáncer
¿Cuál es el linfoma más frecuente?
El linfoma más frecuente es el linfoma no hodgkin , que se relaciona con la edad siendo más frecuente a partir de los 50 años.
¿Qué es un linfoma de MALT?
El linfoma MALT es el linfoma de tejido linfoide asociado a mucosas . Es un linfoma no hodgkin raro que se desarrolla en la mucosa de ciertos órganos como puede ser el sistema intestinal, siendo el más común el linfoma de estómago, también se puede producir en mucosas del pulmón y de glándulas lagrimales y mamarias.

Enfermedad
Paro Cardiorrespiratorio
¿Qué es un paro cardiorrespiratorio?
El paro cardiorespiratorio es el cese de la función cardíaca y de la función respiratoria del individuo. Es más frecuente en los hombres y la edad de presentación suele ser alrededor de los 69 años . Tanto en hombres como en mujeres, la causa más frecuente es la asistolia . Es una urgencia vital, de forma que hay que iniciar la resucitación cardiopulmonar cuanto antes, lo cual es vital para la vida del paciente. Es una enfermedad grave.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tipos de paros cardiorrespiratorios
Asistolia : no hay latido cardíaco, se asocia a ahogamiento , intoxicación medicamentosa y bradicardia extrema .
Fibrilación ventricular o taquicardia ventricular sin pulso : hay latido cardíaco, pero este no es efectivo, si no se revierte mediante un desfibrilador , el paciente llegará a asistolia. Es el más frecuente cuando hay un infarto cardíaco previo.
Actividad eléctrica sin pulso : hay actividad eléctrica que no da lugar a actividad mecánica del corazón, hipovolemia , neumotórax a tensión , hipoxia y taponamiento cardíaco , son algunas de sus causas.
Causas de un paro cardiorrespiratorio
Las causas de paro cardiorespiratorio pueden ser:
Causas cardíacas : como el infarto , las arritmias o el taponamiento cardíaco .
Causas respiratorias : como el embolismo pulmonar , la obstrucción de las vías aéreas, el broncoespasmo severo , ahogamiento , neumotórax a tensión, insuficiencia respiratoria , depresión del centro respiratorio.
Causas metabólicas : hiperpotasemia e hipopotasemia .
Otras causas : traumatismos craneales o torácicos , lesiones de grandes vasos e hipovolemia, shock séptico e hipotermia.
Síntomas de un paro cardiorrespiratorio
Los síntomas principales de un paro cardiorespiratorio son la pérdida de conciencia , que se asocia a una ausencia de pulso, y la pérdida de respiración.
Tratamiento para un paro cardiorrespiratorio
El tratamiento de un paro cardíaco respiratorio es la resucitación cardiopulmonar básica por medio de masaje cardíaco y ventilación boca a boca que se puede asociar a la resucitación con desfibrilador automático o semi-automática. En el momento actual existen muchos lugares públicos que tienen desfibriladores, en caso de paro cardiorespiratorio, su uso, lo más rápidamente posible, mejora el pronóstico de la parada.
Los desfibriladores automáticos presentes en lugares públicos permiten el manejo por personal no cualificado , ya que el propio aparato guía el proceso a seguir. Esto permite que cualquier persona pueda realizar una resucitación cardiopulmonar, mejorando el pronóstico de vida de estos pacientes.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Pruebas complementarias del tratamiento de un paro cardiorrespiratorio
En un paro cardíaco la única prueba complementaria consiste en comprobar que el paciente respira y tiene pulso . Ante la ausencia de los mismos se deberá proceder a realizar un masaje cardíaco y ventilación boca a boca o poner un desfibrilador automático si es posible. La rapidez en estas acciones, y no las pruebas diagnósticas, son las que suponen la diferencia en la vida del paciente.
Posteriormente, cuando el paciente esté estable, se deberá diagnosticar la causa del paro cardíaco para revertir la causa.
Las pruebas serán: analíticas de sangre, radiología de tórax y zona abdominal, y electrocardiograma.
Factores desencadenantes de un paro cardiorrespiratorio
Los factores desencadenantes puede ser arritmias , infarto de miocardio , insuficiencias respiratorias , broncoespasmo , traumatismos , heridas inciso-contusas en zonas torácicas o abdominales, y sepsis .
Factores de riesgo de un paro cardiorrespiratorio
Son factores de riesgo las enfermedades cardiovasculares como hipercolesterolemia e hipertensión, las enfermedades respiratorias como la bronquitis crónica y el asma, la alteración iónica en el potasio , los neumotórax a tensión herida, las heridas inciso-contusas que puedan afectar al corazón o el tórax, y los traumatismos severos torácicos.
Complicaciones de un paro cardiorrespiratorio
La complicación de un paro cardiorespiratorio es la muerte .
Si se recupera del paro:
Insuficiencia respiratoria.
Insuficiencia cardíaca.
Alteraciones neurológicas por el daño cerebral padecido por hipoxia.
Prevención de un paro cardiorrespiratorio
Control del colesterol.
Control de la tensión.
Ejercicio acorde a la edad del paciente.
Dieta cardiosaludable.
Control de asma y bronquitis crónica de forma adecuada.
Especialidades a las que pertenece un paro cardiorrespiratorio
El paro cardiorrespiratorio se debe controlar tras su recuperación en la UVI por parte de un médico intensivista , pero todo el mundo puede ayudar a una persona que presenta un paro cardiorrespiratorio delante de él por medio de los medios de resucitación cardiorrespiratoria básicos y la localización de desfibriladores automáticos en los sitios de gran afluencia de público.
Preguntas frecuentes
¿Cómo empieza un paro cardíaco?
El paro cardíaco puede empezar de muy diferente forma dependiendo de la causa que lo produzca. Se puede iniciar por una arritmia o una bradicardia con alteración en el latido cardíaco, por disminución del mismo, o por el contrario por el aumento del ritmo cardíaco. Puede iniciarse con dolor torácico opresivo irradiado a brazo izquierdo, cuello o garganta, si la causa es un infarto . En los casos de problemas respiratorios comenzará con un aumento de la disnea , que el paciente no podrá tratar de modo adecuado por falta de conocimiento de la progresión del proceso. Se puede producir también por alteraciones en iones como el potasio, que darán lugar a arritmias cardíacas . En algunos casos no hay síntomas previos, es lo que se conoce como muerte súbita .
¿Cuáles son los primeros auxilios en caso de paro cardíaco?
Los primeros auxilios en un paro cardíaco serán:
En primer lugar, avisar al 112.
Seguidamente, si usted sabe, deberá comenzar con el masaje cardíaco , que se realiza por compresiones (el tórax debe bajar 5 cm. aproximadamente) en el centro del tórax, con los brazos de la persona estirados, se darán 15 compresiones torácicas seguidas de 2 respiraciones boca a boca.
Si hay un desfibrilador será necesario conectarlo al paciente y seguir las instrucciones que el sistema nos vaya indicando.
¿Qué es un preinfarto?
El término preinfarto es el término vulgar conocido como angina de pecho . En la angina de pecho se produce una isquemia menor por falta de aporte sanguíneo en las arterias coronarias , que no dejan daño a nivel del músculo cardíaco. Cuando un paciente presenta una angina de pecho de reciente comienzo, debe acudir a un servicio de urgencia, donde será valorado. En muchas ocasiones, tras realizar una coronariografía , se puede ver si el paciente tiene una arteria obstruida y ser intervenido de forma adecuada.
¿Cómo saber si tengo un preinfarto?
Cuando un paciente presenta dolor centrotorácico opresivo que se relaciona con el ejercicio, o aparece en reposo de forma mantenida, deberemos acudir a un médico, que nos hará el diagnóstico acertado y propondrá el tratamiento más adecuado.
¿Qué hacer si tengo un preinfarto?
Si se tiene un preinfarto o angina de pecho se deberá acudir a una urgencia hospitalaria, donde el paciente será diagnosticado y tratado de forma adecuada. No se deberá ir conduciendo y, si es posible, habrá que pedir ayuda al 112, cuyo personal capacitado para ello trasladará y atenderá al paciente en el mínimo tiempo posible.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.

Enfermedad
Tuberculosis
¿Qué es la tuberculosis?
La tuberculosis, antiguamente conocida en Europa como “gran peste blanca” y anteriormente por los griegos denominada “tisis”, es una infección infectocontagiosa de larga duración producida por agentes de la especie mycobacterium tuberculosis complex, en España sobre todo por la mycobacterium tuberculosis o bacilo de Koch (BK). Esta infección puede afectar a cualquier órgano.
Se trata de la infección crónica más importante del mundo , con una incidencia de 8 millones de casos nuevos al año. El 90-95% de casos se producen en países en vías de desarrollo, siendo una de las mayores causas de muerte de origen infeccioso.
Tipos de tuberculosis
Se puede dividir la tuberculosis en dos maneras según la presentación en el paciente:
La infección tuberculosa latente: Se produce cuando la persona entra en contacto con mycobacterium tuberculosis desencadenandose, en su organismo, una respuesta del sistema de defensa (llamado chancro de inoculación) en el lugar donde se asienta (habitualmente el pulmón ). Esta respuesta inmune consigue controlar la multiplicación de la mycobacteria y con ello frenar la infección y eliminar cualquier síntoma. Pero el paciente tiene el riesgo de poder desarrollar la enfermedad en el futuro.
La enfermedad tuberculosa activa: Se define por la presencia de síntomas y alteraciones en la exploración física y en la realización de pruebas complementarias. El desarrollo de la enfermedad puede darse en una gran variedad de localizaciones: pulmonar, pleura (membrana que recubre los pulmones), ganglionar (estaciones del sistema de defensa), meníngea (membranas que recubren el cerebro y la médula), osteoarticular, gastrointestinal, genitourinaria, etc. Se presenta de forma más frecuente (85%) en los pulmones .
Causas de la tuberculosis
La causa de la infección es el contagio por especies del complejo mycobacterium tuberculosis. En nuestro país sobre todo por la mycobacterium tuberculosis , con algún brote esporádico por Mycobacterium bovis. La vía de contagio habitual es la respiratoria y por secreciones respiratorias (esputo) emitidas por un adulto con enfermedad tuberculosa pulmonar. En el caso del origen bovino (infección producida por la m. bovis) , se transmite tras la ingestión de leche contaminada.
Síntomas de la tuberculosis
Los síntomas son variables dependiendo de la zona de afectación del organismo, la edad del paciente, la situación de su sistema de defensas, la coexistencia de otras enfermedades y la virulencia de la mycobacteria.
Pueden presentarse síntomas generales como fiebre, sudoración nocturna profusa, pérdida de apetito (anorexia) y disminución de peso, cansancio (astenia), y malestar general.
Cuando afecta al pulmón , que es lo más frecuente, aparece tos que inicialmente no arranca flemas y después es productiva arrastrando un esputo purulento (infeccioso, con aspecto de pus), en ocasiones va acompañado por la expulsión de sangre (hemoptisis), dolor torácico y sensación de falta de aire (disnea).
La tuberculosis extrapulmonar es menos común . Puede aparecer por ejemplo en: los ganglios linfáticos que se inflaman y pueden fistulizar la piel (tener comunicaciones anómalas hacia la piel).
Tuberculosis pleural: Aparece una acumulación de líquido en el espacio pleural (espacio virtual entre las dos membranas que cubren los pulmones), con dolor torácico agudo y sensación de falta de aire.
Si existe afectación del sistema nervioso central con meningitis , aparecerán síntomas como dolor de cabeza, disminución del nivel de conciencia y rigidez en la nuca.
Cuando la infección se da en el aparato genitourinario , el paciente suele tener molestias al orinar, sangre en la orina, dolor lumbar, febrícula e ir de forma frecuente a orinar. En las mujeres , además, aparece dolor en la pelvis, alteraciones de la menstruación e infertilidad. Y en los varones , aparece prostatitis y orquitis (inflamación de la próstata y/o el testículo). Puede darse también la infección en el tubo digestivo desde la boca hasta el ano, cursando con síntomas como diarrea, dolor abdominal, fístulas a la piel, hemorragia digestiva, aparición de una masa palpable en el abdomen, etc.
En el corazón , concretamente en el pericardio que es la membrana que lo recubre, el paciente puede presentar dolor torácico que se modifica con la inspiración o la posición y otros síntomas de todo el organismo (malestar, fiebre, etc). Si existe un derrame puede comprometer la función del corazón.
Tratamiento para la tuberculosis
En la infección latente está indicado tratar a todos los pacientes menores de 35 años. Los médicos ofrecen tratamiento a todos los pacientes de entre 35-65 años con infección tuberculosa latente y riesgo de desarrollar una tuberculosis activa (salvo riesgo elevado de toxicidad en el hígado por los fármacos). Este tratamiento se denomina quimioprofilaxis y en él se indica la toma de antibióticos en distintas pautas (isoniazida durante 6 meses o Isoniazida + rifampicina durante 3 meses).
En la enfermedad tuberculosa activa incluye la administración de 4 tipos de antibióticos, dos de ellos con actividad bactericida (mata a las mycobacterias que se están multiplicando), otro con buena actividad esterilizante (mata a las que están en situación latente), y otro que se denomina acompañante (sirven para disminuir las resistencias de los microorganismos).
Es fundamental el cumplimiento terapéutico dado que su incumplimiento o el cumplimiento irregular compromete la eficacia y es el principal mecanismo de inducción de resistencias.
La pauta principal suele ser de 2 meses con administración de isoniazida + rifampicina + pirazinamida + etambutol, seguido durante otros 4 meses de la toma de isoniazida + rifampicina. Existen otros tipos de pautas que se indican dependiendo de las características del paciente y de la presentación de la enfermedad.
El paciente con enfermedad activa debe ser aislado respiratoriamente para el control de contagio.
Pruebas complementarias del tratamiento de tuberculosis
La infección tuberculosa latente se diagnostica mediante la denominada prueba de la tuberculina o mantoux en la que se detecta una hipersensibilidad del organismo frente a las proteínas de la mycobacteria como memoria del sistema de defensa al haber tenido contacto previo con el microorganismo cuando se infectó. Para ello, se inyecta a nivel subcutáneo un líquido y a las 48 – 72 horas se objetiva si el organismo ha presentado una reacción en la piel, en el sitio donde se inyectó. Se considera que la prueba es positiva si hay un enrojecimiento e inflamación por encima de 10mm.
En la enfermedad tuberculosa activa se realiza una recogida de muestras de esputo , orina, jugos gástricos, sangre, líquido cefalorraquídeo, aparato genital, etc, según la localización de la infección y se visualiza de forma directa el microorganismo mediante el uso de una tinción que colorea de forma específica la bacteria. Además, se realizan cultivos para detectar la presencia de microorganismos, una analítica de sangre y técnicas de imagen fundamentalmente radiografía de tórax y TAC, donde se objetivan las lesiones en el pulmón, en el caso de la radiografía, y de forma más ampliada al resto de zonas del organismo según la afectación que presente el paciente .
Factores desencadenantes de la tuberculosis
El principal factor desencadenante de la tuberculosis es el contagio a través de los fluidos .
Factores de riesgo de la tuberculosis
Convivencia con una persona enferma de tuberculosis.
Vivir en situaciones de hacinamiento.
Ventilación pobre.
Riesgo laboral (personal de instituciones sanitarias, etc.).
Inmigración.
Nivel socioeconómico bajo.
Personas adictas a drogas por vía parenteral, alcohol, etc.
Padecer una situación de inmunosupresión (alteración del sistema de defensa): pacientes con VIH (virus de la inmunodeficiencia humana), ingesta crónica de corticoides, pacientes transplantados, etc.
Complicaciones de la tuberculosis
Lesión del tejido pulmonar con su destrucción y cavitación .
Desarrollo de un tipo de tumor pulmonar que se asocia frecuentemente al padecimiento de tuberculosis (carcinoma broncogénico).
Lesiones de la vía aérea (bronquiectasias), estenosis (estrechamiento traqueobronquial), etc.
Alteraciones vasculares (vasculitis, trombosis,etc.)
Calcificaciones de los ganglios linfáticos.
Neumotórax (entrada de aire en la cavidad pleural).
Prevención de la tuberculosis
La principal medida de prevención es actuar sobre el paciente enfermo que es el reservorio para transmitir la enfermedad . Para ello es fundamental realizar un diagnóstico precoz y un tratamiento idóneo con aislamiento respiratorio del paciente .
Controlar los animales enfermos y garantizar una adecuada higiene de la leche de vaca.
Uso de la vacuna , que está reservada a casos seleccionados (niños con prueba de tuberculina negativa con exposición crónica a los esputos de un familiar con la enfermedad, trabajadores de instituciones sanitarias con prueba de la tuberculina negativa en contacto frecuente con enfermos o muestras biológicas, etc.)
Especialidades a las que pertenece la tuberculosis
Según la forma de presentación de la enfermedad puede ser tratada y evaluada por el especialista en enfermedades infecciosas , por el neumólogo , el médico internista , y todos aquellos especialistas según el tipo de afectación desarrollada.
Preguntas frecuentes
¿Cómo se transmite la tuberculosis?
La tuberculosis se transmite por vía respiratoria a través de las secreciones y las pequeñas gotas de saliva expulsadas por la tos de un paciente con la enfermedad activa. Además, otra de las micobacterias que pueden desencadenar la infección se transmite por el consumo de leche bovina sin control higiénico sanitario.
¿Cuál es la vacuna contra la tuberculosis?
La vacuna contra la tuberculosis o BCG, constituida por la bacteria modificada viva , no patógena (no produce la infección), que se administra por vía intradérmica. En Europa occidental no se recomienda la vacunación masiva de la población, salvo en casos específicos de mayor riesgo de infección. En los países de bajo nivel socioeconómico, donde la enfermedad es más frecuente, sí se aplica de forma habitual.
¿Cuál es la bacteria de la tuberculosis?
La bacteria que habitualmente en nuestro medio produce la tuberculosis es el mycobacterium tuberculosis (bacilo de la familia mycobacteriaceae , género mycobacterium y especie mycobacterium complex ).
¿Cuánto tiempo dura viva la bacteria de la tuberculosis?
Una vez infectado el cuerpo por la bacteria, esta puede vivir en el organismo de forma latente sin dividirse y sin producir infección con síntomas , encapsulada por una reacción del sistema de defensa del organismo en lo que se denomina granuloma.
Otras veces el cuerpo es capaz de eliminarla de forma completa . En pacientes con alteración del sistema inmune, meses o años después puede reactivarse la enfermedad y producir síntomas típicos.
¿Cuánto dura el tratamiento de la tuberculosis?
El tratamiento de la infección activa de tuberculosis se establece como mínimo en unos 6 meses .

Enfermedad
Hipertensión Pulmonar
¿Qué es la hipertensión pulmonar?
La hipertensión pulmonar se define como la elevación de la presión en la arteria pulmonar por encima de 25 mmHg (milímetros de mercurio), estando el paciente en reposo. Es una alteración infrecuente que afecta sobre todo a personas jóvenes, habitualmente mujeres, dándose en 1-2 personas por millón de habitantes. Es una enfermedad grave de curso progresivo.
Tipos de hipertensión pulmonar
Hipertensión pulmonar primaria : es aquella que produce una elevación mantenida de la presión arterial pulmonar sin una causa demostrable.
Hipertensión pulmonar secundaria : es la presión arterial pulmonar elevada debido al padecimiento de enfermedades pulmonares.
Hipertensión pulmonar hereditaria : de influencia genética, apareciendo en un 6% de los casos debido a una alteración genética.
Causas de la hipertensión pulmonar
El 80% de las hipertensiones pulmonares secundarias son debidas al padecimiento de la Enfermedad Pulmonar Obstructiva Crónica (EPOC). Otras patologías que pueden ser motivo de la aparición de la hipertensión son el tromboembolismo pulmonar, fibrosis pulmonares, hipertensión portal, bronquiectasias, asma bronquial, síndrome de apnea del sueño, enfermedades cardiovasculares como valvulopatías, cardiopatías congénitas, o miocardiopatías. No obstante, la causa de la hipertensión pulmonar primaria es desconocida.
Síntomas de hipertensión pulmonar
La instauración de los síntomas suele ser muy progresiva. Aparece sensación de falta de aire de aparición gradual (disnea), con limitación de la actividad física, fatiga, debilidad, dolor torácico en la zona del esternón producido por la aparición de una angina de pecho. Puede haber un síncope o pérdida de conciencia que en ocasiones es la primera manifestación. A veces puede producirse hemoptisis (expulsión de sangre con la tos). Se pueden manifestar síntomas de fallo cardíaco con insuficiencia cardíaca derecha.
Tratamiento para la hipertensión pulmonar
En los casos de hipertensión pulmonar secundaria el tratamiento debe basarse en aquel que corrige la enfermedad que lo produce.
En los casos de hipertensión pulmonar primaria el tratamiento se basa en:
Medidas generales : evitar realizar un ejercicio intenso, la exposición constante a grandes alturas, los anticonceptivos orales y el embarazo. También evitar la toma de fármacos como antiinflamatorios no esteroideos y betabloqueantes
Tratamiento de base con oxigenoterapia : sirve para mantener la oxigenación de la sangre por encima del 90%, administración de fármacos como diuréticos , Digoxina o anticoagulantes orales para evitar la producción de tromboembolismos pulmonares (coágulos en el pulmón)
Otro de los fármacos utilizados para el control de la enfermedad son los fármacos vasodilatadores como calcioantagonistas , Nifedipino o Diltiazem, y otros más selectivos sobre la circulación pulmonar como prostaglandinas, Epoprostenol, Iloprost, Treprostil, Beraprost, antagonistas de los receptores de endotelina, como Bosentan , e inhibidores de fosfodiesterasa tipo 5 como el Sildenafilo.
Trasplante pulmonar : se reserva como tratamiento de aquellos pacientes en los que las medidas farmacológicas no producen mejoría, manteniendo una insuficiencia cardíaca derecha.
Pruebas complementarias del tratamiento de hipertensión pulmonar
Las pruebas complementarias que se realizan para llegar al diagnóstico de la hipertensión pulmonar son:
Radiografía de tórax : se puede detectar una anomalía en la silueta de la arteria pulmonar y el corazón. También se detecta alteración en la vascularización pulmonar que se manifiesta en la imágen radiográfica.
Electrocardiograma : se produce una alteración del registro del ritmo del corazón.
Ecocardiograma : detecta la presencia de hipertensión pulmonar y alteraciones del corazón producidas por esta.
Gammagrafía pulmonar de perfusión : determina el flujo de las arterias pulmonares.
Arteriografía pulmonar : prueba de rayos X para la visualización de las arterias pulmonares.
Cateterismo cardíaco : ayuda al diagnóstico y evalúa la función del corazón.
Realización de análisis genéticos : para detección de aquellas alteraciones heredadas que producen hipertensión pulmonar.
Factores desencadenantes de hipertensión pulmonar
El factor desencadenante de la producción de la hipertensión pulmonar es la producción de una contracción de las paredes arteriales pulmonares , una remodelación y proliferación de las células de esas paredes y la producción de trombos en las arterias.
Factores de riesgo de hipertensión pulmonar
Padecimiento de enfermedades como sarcoidosis, histiocitosis, colagenosis, enfermedades mieloproliferativas, esplenectomía, etc.
Toma de fármacos y tóxicos como anorexígenos, inhalación de cocaína, anfetaminas y/o aceite de colza.
Exposición crónica a grandes alturas.
Padecimiento de insuficiencia cardíaca.
Tener alteraciones anatómicas del corazón de nacimiento.
Enfermedad hepática.
Complicaciones de la hipertensión pulmonar
Aparición de arritmias cardíacas.
Desarrollo de insuficiencia cardíaca derecha.
Hipertrofia del ventrículo derecho (aumento del tamaño de su pared muscular).
Aparición de cianosis o coloración azulada de la piel por déficit de sangre y oxigenación de los tejidos.
Hemorragias, sagrados pulmonares o de alteraciones arteriales (aneurismas).
Insuficiencia respiratoria.
Pérdida de conocimiento.
Muerte.
Prevención de la hipertensión pulmonar
Realizar una alimentación equilibrada , rica en frutas y verduras.
Realizar ejercicio moderado de forma regular.
Evitar permanecer tiempos prolongados en regiones de gran altitud.
Vacunación contra enfermedades que pueden afectar al pulmón como vacunación contra el Neumococo y la gripe.
En las pacientes con factores de riesgo se recomienda no quedarse embarazadas.
No fumar.
Tomar anticoagulantes orales en pacientes con riesgo de alteraciones de la coagulación de la sangre (pacientes encamados, que sufren fracturas óseas, con tumores…etc.)
Tratamiento específico de las enfermedades de base que pueden desencadenar o provocar la hipertensión arterial.
Especialidades a las que pertenece la hipertensión pulmonar
La hipertensión arterial es una patología cuyo diagnóstico y manejo se realiza por especialistas en neumología.
Preguntas frecuentes:
¿Qué es la hipertensión pulmonar en recién nacidos?
La hipertensión pulmonar en los recién nacidos se define como en los adultos, como la elevación de la presión en la arteria pulmonar por encima de 25 mmHg. La hipertensión pulmonar persistente del recién nacido es un síndrome donde aparece cianosis (coloración azulada de la piel) por la presencia de una anomalía anatómica de comunicación de cavidades en el corazón del recién nacido, en ausencia de cardiopatía congénita subyacente
¿Cuál es la presión arterial pulmonar normal?
Se encuentra entre 18 y 25 mmHg para la presión sistólica (la más alta), entre 6 a 10 mmHg para la diastólica (la más baja), y 12 a 16 mmHg para la presión arterial pulmonar media.
¿Qué mide la presión venosa central?
La de presión venosa central (PVC) consiste en la medición de la presión que existe en la aurícula derecha del corazón para valorar el flujo de sangre que llega al corazón y el tono vascular del paciente, que se mide en cm de agua.
¿Qué es la presión en cuña?
Es la presión determinada en la arteria pulmonar que refleja la presión de la aurícula izquierda y la presión diastólica final del ventrículo izquierdo (cuando este se llena de sangre).
¿Qué es un cateterismo pulmonar?
El cateterismo pulmonar o cateterismo de la arteria pulmonar, es un procedimiento en el que se pasa una sonda delgada (pequeño tubo flexible), hasta el lado derecho del corazón para medir el paso de sangre a través del corazón y vigilar la función cardíaca en pacientes muy enfermos. Este catéter permite realizar medidas de las presiones en la aurícula derecha, el ventrículo derecho así como en la arteria pulmonar.

Enfermedad
Hemoptisis
¿Qué es la hemoptisis ?
La hemoptisis es la expulsión de sangre por la boca procedente de los pulmones o de los bronquios , que habitualmente se acompaña de tos. Puede ser la primera manifestación de un gran número de enfermedades con afectación pulmonar, con una frecuencia de afectación diferente. La cantidad de sangre expulsada puede ser variable y con ello la gravedad del cuadro que, en el caso más importante, puede comprometer la vida del paciente.
Tipos de hemoptisis
Según la cantidad de sangre que se expulsa en la hemoptisis, esta se clasifica en:
Esputos hemoptoicos o hemoptisis leve : escasa cantidad de sangre mezclada con la expectoración, como hilos de sangre (máximo 15-30 ml/día).
Hemoptisis moderada o franca : emisión de sangre pura (menos de 200 ml/día).
Hemoptisis grave o masiva : expulsión de sangre de forma abundante (de 200-600 ml/día o mayor de 150 ml/hora) que amenaza la vida del paciente.
Causas de la hemoptisis
La hemoptisis es un signo inespecífico asociado a muchas patologías producidas en el pulmón:
Tumores : carcinoma broncogénico (25-30% de los casos), adenomas y tumores metastásicos endobronquiales.
Bronquitis crónica : de origen tabáquico (20-30% de los casos).
Enfermedades infecciosas (10%) : neumonías, absceso pulmonar o micosis (infecciones por hongos), infecciones por parásitos, producidas así mismo por bacterias como el Staphylococcus aureus , Mycobacterium tuberculosis , hongos como el Aspergillus , o parásitos como el responsable de la hidatidosis, el Echinococcus granulosus .
Trastornos vasculares : infarto pulmonar, estenosis mitral, ruptura de aneurisma aórtico, insuficiencia cardíaca…etc.
Vasculitis : lupus eritematoso sistémico, granulomatosis de Wegener, enfermedad de BehÇet…etc.
Coagulopatías : alteraciones de la coagulación de la sangre congénitas o adquiridas.
Alteraciones producidas por acciones médicas : tratamientos farmacológicos anticoagulantes o antiagregantes (alteran la coagulación de la sangre), biopsia bronquial (toma de muestras de tejidos)…etc.
Otras causas raras : hemoptisis catamenial (endometriosis en la mucosa (revestimiento) respiratoria) y hemoptisis coital (en enfermos con patología cardíaca por el esfuerzo realizado que aumenta el edema de la mucosa).
Hemoptisis por la aspiración de cuerpos extraños .
Hemoptisis de origen desconocido o idiopática : 5 – 30% de los casos.
Síntomas de la hemoptisis
La hemoptisis se caracteriza por la expectoración de sangre en mayor o menor cantidad, de color rojo brillante, aspecto espumoso y consistencia líquida, acompañada de saliva. En ocasiones pueden expulsarse coágulos.
Según la causa de la hemoptisis, se podrá acompañar de otro tipo de síntomas muy variables como sensación de falta de aire (disnea), dolor torácico, fiebre, malestar general, pérdida de peso, etc.
Tratamiento para la hemoptisis
El tratamiento de la hemoptisis leve es aquel específicamente dirigido a la causa que la produce. Se mantiene al paciente en observación durante 12 hora s hasta confirmar la desaparición del sangrado. Frecuentemente se indica tratamiento con fármacos antitusivos como Codeína .
Cuando hay un sangrado masivo, el tratamiento va dirigido además de a la causa, de forma urgente e inicial, a mantener la supervivencia del paciente:
Medidas de soporte : ingreso del paciente con vigilancia intensiva. Aporte de oxigenoterapia y control de la saturación de oxígeno e intubación si es preciso. Control de la tensión arterial y realización de un electrocardiograma. Se mantiene al paciente en reposo absoluto en la cama y, si se sospecha el lado del origen del sangrado, se coloca al paciente de dicho lado. Se mantiene al paciente en dieta absoluta y se le administran fármacos antitusivos.
Realización de broncoscopia : además de ser útil para el diagnóstico, puede ser la vía de realización de un tratamiento tópico con fármacos para favorecer la coagulación, tratamientos antibióticos o antifúngicos, instilación de suero frío que favorece la vasoconstricción, y reducción del sangrado o aplicación de láser para cauterizar el punto del mismo. Además, con este procedimiento se puede llevar a cabo la intubación de pulmón no sangrante que permita ventilar y preservar la oxigenación de la sangre.
Embolización de las arterias bronquiales : ocluir o cerrar los vasos sanguíneos para evitar el flujo se sangre y la continuación del sangrado.
Cirugía : cuando el resto de medidas fallan en pacientes con hemorragia unilateral o con compromiso respiratorio, o la cantidad de flujo sanguíneo en el cuerpo esté comprometido, siempre y cuando no haya contraindicaciones en el paciente.
Pruebas complementarias del tratamiento de hemoptisis
Es fundamental para el diagnóstico de la hemoptisis y la determinación de su posible causa, el interrogatorio clínico al paciente para saber sus antecedentes en cuanto a patologías que pueden afectar al pulmón, presencia de síntomas acompañantes, etc, así como una minuciosa exploración física para diferenciar si el sangrado proviene de la vía digestiva o confirmar que es de la vía respiratoria inferior.
Además, se solicitan pruebas complementarias como:
Analítica de sangre : con determinación de hemograma sabiendo con ello si existe anemia, algo que solo ocurre si existe una hemorragia grave, función hepática, renal, bioquímica, determinaciones específicas si se sospecha de enfermedades específicas (ANCA, ANA, anti DNA, Ac. antimembrana basal…etc.), y también se puede solicitar una gasometría arterial.
Radiografía de tórax : en un porcentaje elevado de casos orienta a la posible causa del sangrado con las alteraciones que se observan en los pulmones, aunque, en algunas ocasiones, no se ven claras alteraciones, lo que no excluye la presencia de una entidad potencialmente grave causante de la hemoptisis.
TAC torácico : detecta lesiones no visibles en la radiografía de tórax.
Broncoscopia : ayuda a la identificación de la posible causa, sobre todo en aquellos casos de sospecha tumoral. También se utiliza en el tratamiento de hemoptisis con abundante hemorragia para localizar y poder tratar el punto de sangrado.
Otras pruebas : citología de esputo (examinar el esputo para determinar la presencia de células anómalas), cultivo o tinciones de esputo para la determinación de la presencia de microorganismos causantes de las infecciones, gammagrafía de ventilación perfusión (si se sospecha de un tromboembolismo pulmonar), y angiografía (permite realizar una embolización o taponamiento del vaso que sangra).
Factores desencadenantes de la hemoptisis
Según la causa que puede producir la hemoptisis, esta se puede desencadenar por la presencia de inflamación y necrosis , (muerte) de los vasos sanguíneos presentes en un tumor pulmonar, un aumento de la vascularización de la mucosa, (revestimiento) de los bronquios en procesos inflamatorios crónicos como bronquitis, la aparición de trombos (coágulos) en vasos sanguíneos, y la muerte de los tejidos en procesos infecciosos , entre otros.
Factores de riesgo de la hemoptisis
Someterse a pruebas médicas invasivas: complicaciones de la broncoscopia, implante de prótesis endobronquiales, intubación traqueal…etc.
Tomar fármacos como anticoagulantes , Amiodarona, Vinblastina …etc.
Consumo de tabaco y/o de cocaína.
Padecer tumores con tendencia a metastatizar al pulmón.
Exposición a elementos como el níquel , el cromo, o el asbesto.
Antecedente de enfermedad pulmonar obstructiva crónica, infecciones a repetición de vía aérea inferior y tos con esputo purulento recurrente.
Contacto continuado con pacientes que presentan infecciones respiratorias.
Complicaciones de la hemoptisis
Anemia.
Colapso pulmonar por hemorragia masiva.
Insuficiencia respiratoria y asfixia.
Shock hipovolémico: fallo multiorgánico por falta de riego sanguíneo suficiente en los órganos y tejidos.
Muerte.
Prevención de la hemoptisis
Promover en la población con campañas de información y la consulta inmediata una vez se presente el síntoma, para el estudio e identificación
Estudio de contactos y aislamiento respiratorio del paciente con TBC para prevenir la infección. Tratamiento del paciente con afectación tuberculosa.
No fumar . Con ello se previene la aparición del cáncer de pulmón y la enfermedad pulmonar obstructiva crónica (EPOC).
Vacunación antigripal y antineumocócica.
Medidas de prevención específica para cada patología que sea posible productora de hemoptisis.
Especialidades a las que pertenece la hemoptisis
La hemoptisis es una alteración que puede ser estudiada y tratada por el neumólogo o el cirujano torácico. Según la causa que la produce, pueden intervenir en su manejo otros especialistas como médicos internistas, cardiólogos…etc.
Preguntas frecuentes:
¿Qué es hemoptoico?
El término hemoptóico o hemoptísico es un adjetivo que se utiliza para referirse a las características del esputo de un paciente cuando presenta sangre o también para hacer referencia al enfermo aquejado de hemoptisis.
¿Qué pasa cuando toses sangre?
El toser sangre puede ser sinónimo de tener una hemoptisis . La persona que tiene ese síntoma debe consultar siempre con su médico, inicialmente al médico de atención primaria, para que se pueda iniciar la exploración física y las pruebas complementarias necesarias para encontrar la causa de la hemoptisis y realizar, así mismo, un diagnóstico diferencial para descartar que la sangre no tiene un origen digestivo u orofaríngeo. Si hay un sangrado abundante, el paciente debe acudir a un servicio de urgencias hospitalarias para su estudio y tratamiento, ya que presenta un riesgo vital importante.
¿Qué significa el color de la flema?
El color de la flema puede orientar hacia la presencia de determinadas enfermedades , por ejemplo, una flema líquida transparente puede estar presente en procesos alérgicos con rinitis, una flema blanquecina, puede presentarse al inicio de una infección respiratoria y una flema espesa amarillo-verdosa sugiere la presencia de una infección respiratoria evolucionada, una coloración rosada o roja informa de la presencia de sangre, la flema marronácea puede presentarse por inhalación de humos
¿Cuáles son los síntomas del cáncer de pulmón?
La forma de presentación de los tumores en el pulmón puede ser variada. Son frecuentes síntomas como dolor torácico, tos, sensación de falta de aire (disnea), hemoptisis, infecciones respiratorias, cansancio, pérdida de peso, dificultad para deglutir por compresión del esófago por el tumor, parálisis de las cuerdas vocales o el diafragma por afectación de los distintos nervios que llevan la información a estas estructuras…etc.
¿Qué significa tener sabor a sangre en la boca?
El sabor a sangre en la boca puede indicar que el paciente presenta un sangrado real en la misma boca o faringe , en la nariz, procedente del aparato digestivo o los pulmones. Además, algunos tratamientos pueden producir esta sensación gustativa sin que realmente exista sangrando.

Enfermedad
Gripe A
¿Qué es la gripe A?
La gripe A es también conocida como gripe influenza A, gripe, gripe porcina y/o nueva gripe es una enfermedad vírica que puede afectar a toda la población, independientemente de la edad y el sexo. Tiene una gran capacidad de difusión, pertenece a la especialidad de medicina general y es considerada una enfermedad de tipo leve.
Tipos de gripe
La gripe puede ser ocasionada por tres tipos diferentes de virus:
Gripe del tipo A : es el tipo de gripe más grave, ya que tras cada contagio la cepa muta (cambia su secuencia genética).
Gripe del tipo B : este tipo de virus de la gripe también muta, pero de una forma más lenta y como mucho hasta tres veces.
Gripe del tipo C : es el tipo de gripe más leve, los síntomas apenas se notan en la mayoría de los casos y es muy común en niños.
Causas de la gripe A
La gripe A es una enfermedad vírica ocasionada por el virus de la llamada gripe porcina A/H1N1.
Este virus es muy contagioso y se transmite de una persona contagiada a una sana mediante vía aérea al toser, estornudar o besarse , es decir, al entrar en contacto gotitas de los fluidos del paciente contagiado con una persona sana.
Síntomas de la gripe A
La gripe A presenta unos síntomas similares a los de cualquier gripe genérica, con la diferencia que en la gripe A son de mayor gravedad . Algunos de estos síntomas son:
Fiebre muy elevada.
Dolor de cabeza.
Irritación y dolor de garganta.
Dolor corporal, sobre todo en articulaciones.
Tos.
Congestión nasal.
Problemas respiratorios.
Tratamiento para la gripe A
La gripe A es un virus, por lo que normalmente si los síntomas no son muy graves el tratamiento es similar al de una gripe común.
El paciente debe permanecer en cuarentena hasta que se recupere, tomando analgésicos y medicamentos para la descongestión nasal.
Sin embargo, en casos de mayor gravedad se suelen emplear medicamentos antivirales que bloquean la enzima de la neuraminidasa, la cual se encarga de propagar el virus por el cuerpo del paciente.
El uso de antivirales debe estar indicado bajo prescripción médica y hay que emplearlos con cautela, ya que sino el virus puede volverse inmune.
Pruebas complementarias del tratamiento de gripe A
Para diagnosticar si el paciente padece gripe A, el médico evaluará los síntomas que estén presentes y tomará una muestra de la nariz o de la faringe para enviarla al laboratorio y someterla a la prueba del PCR (reacción en cadena de la polimerasa), un proceso por el cual se duplica el ADN del paciente mediante la enzima de la Taq Polimerasa para ver si existe el virus de la gripe A.
Factores desencadenantes de la gripe A
La gripe A es una enfermedad vírica que se transmite por vía aérea, por tanto, el principal factor desencadenante se da al entrar en contacto con una persona que padezca la gripe A.
De manera que, si una persona sana entra en contacto con una que padezca gripe A, al toser, estornudar, darle la mano o besarse, entre otras acciones, el paciente sano suele quedar contagiado.
También puede transmitirse por el aire sin entrar en contacto físico con el paciente infectado.
Factores de riesgo de la gripe A
Los factores de riesgo que pueden propiciar que una persona padezca gripe A con mayor probabilidad son:
Edad : las personas mayores de 65 años tienen mayor facilidad de contraerla, del mismo modo que de padecer los síntomas son más graves.
Mujeres embarazadas : los síntomas en este tipo de pacientes pueden complicar el embarazo.
Antecedentes clínicos : los pacientes que padezcan otras enfermedades crónicas relacionadas con los pulmones, riñones, hígado, diabetes, o con un sistema inmunitario débil, tienen mayor riesgo de que los síntomas agraven sus enfermedades.
Complicaciones de la gripe A
Pulmonía.
Fallo hepático.
Otitis.
Miocarditis.
Neumonía.
Prevención de la gripe A
Evitar mantener contacto con personas con gripe A.
Lavarse las manos antes de comer.
Acudir a lugares con buena ventilación y evitar aquellos muy concurridos.
Evitar los cambios de temperatura rápidos y bruscos.
Usar ropa adecuada al tiempo, abrigándose bien para el frío.
Especialidades a las que pertenece la gripe A
Ante la presencia de síntomas de la gripe A el paciente debe acudir a su médico de cabecera, que será el encargado de tramitar las pruebas para el diagnóstico.
Preguntas frecuentes:
¿Cuáles son las diferencias entre la gripe A y la gripe común?
La gripe A y la gripe común son ocasionadas por el mismo virus, pero de distinta apariencia , de forma que el sistema inmunitario del organismo no reconoce a la gripe A como una gripe común y por ello afecta a más población.
¿Cómo se contagia el virus de la gripe A?
La gripe A se contagia mediante vía aérea, esto es, al entrar en contacto con alguien que la padezca o por el aire.
¿Cuáles es el periodo de contagio de la gripe A?
El paciente infectado de gripe A puede contagiar al resto de personas incluso un día antes de que presente los primeros síntomas y hasta 7 días después del inicio de la enfermedad.
¿Cuánto duran los síntomas de la gripe?
Los síntomas de la gripe suelen desaparecer por completo a las dos semanas.
¿Cuánto tiempo puede durar la fiebre?
La fiebre es uno de los síntomas que remite antes, aproximadamente a los 5 días.

Enfermedad
Fibrosis Quística
¿Qué es la fibrosis quística?
Enfermedad autosómica recesiva (ambos padres deben tener el gen) que se da tanto en hombres como en mujeres, siendo mayor el índice de supervivencia en los hombres. Es más común en niños y adultos jóvenes. Es una enfermedad de tipo grave.
Tipos de fibrosis
Existen numerosos tipos de fibrosis, siendo las más habituales:
Fibrosis quística: afecta a los pulmones y al páncreas, por un exceso de producción de mocos las cuales se acumulan en las vías respiratorias y produce alteraciones en las mismas.
Fibrosis pulmonar: afecta al tejido de los pulmones, el cual se cicatriza y se vuelve grueso, provocando alteraciones en la respiración y la oxigenación de los órganos.
Fibrosis endomiocárdica: en este caso la fibrosis se produce en el endocardio al inflamarse por engrosarse las paredes del corazón.
Causas de la fibrosis quística
La fibrosis quística es una enfermedad hereditaria que se ocasiona por una anomalía en uno de los genes del individuo.
Esta alteración del gen provoca que el organismo genere moco excesivo el cual se acumula en las vías respiratorias, los pulmones y el páncreas generando problemas graves en el cuerpo del paciente.
Síntomas de fibrosis quística
Al ser una enfermedad que sobre todo afecta a los pulmones los principales síntomas se manifiesta en las vías respiratorias, pero también en otras partes del cuerpo. Los síntomas más frecuentes son:
Pólipos nasales.
Congestión nasal.
Neumonías.
Tos.
Fiebre.
Infección.
Tratamiento para la fibrosis quística
La finalidad del tratamiento es controlar los síntomas de la enfermedad ya que no tiene una cura a día de hoy.
El tratamiento suele basarse en medicamentos a ntiinflamatorios, antibióticos y broncodilatadores, entre otros.
También existen terapias adicionales como fisioterapia o la terapia del chaleco para reducir la acumulación de mucosa en el pecho. En algunos casos el paciente puede necesitar una intervención quirúrgica para eliminar pólipos nasales o incluso realizar un trasplante del pulmón.
Cada tratamiento es diferente según el paciente y la gravedad de su enfermedad.
Pruebas complementarias del tratamiento de fibrosis quística
Al tratarse de una enfermedad hereditaria las pruebas se suelen hacer en la primeras horas de vida de los bebés, de manera que en una analítica se observan los niveles del tripsinógeno inmunorreactivo (sustancia química que libera el páncreas que indica fibrosis quística), aunque tras un parto prematuro o complicado pueden estar alterados por lo que se suelen realizar otras pruebas como el test del sudor.
También, puede realizarse un estudio genético de los padres para ver si son portadores del gen anómalo y la posibilidad de que el bebé padezca la FQ.
Factores desencadenantes de la fibrosis quística
El factor desencadenante de la fibrosis quística es la mutación de un gen.
Factores de riesgo de fibrosis quística
Al tratarse de una mutación en los cromosomas uno de los factores de riesgo es la herencia genética , transmitiendo la enfermedad de padres a hijos.
Otro factor de riesgo es la raza , ya que es más habitual en personas blancas del norte de europa.
Complicaciones de la fibrosis quística
Insuficiencia respiratoria.
Neumotórax.
Hemoptisis (tos con sangrado).
Reagudizaciones (agravamiento de los síntomas de la FQ).
Aparición de infecciones crónicas.
Prevención de la fibrosis quística
La fibrosis quística no se puede prevenir ya que es hereditaria fruto de una alteración del cromosoma 7.
La única medida preventiva es analizar los cromosomas de los padres para evaluar la posibilidad de que se transfiera a los hijos.
Especialidades a las que pertenece la fibrosis quística
La fibrosis quística es tratada por la rama médica de neumología y si se precisa intervención quirúrgica sería tratada por el cirujano torácico.
Preguntas frecuentes:
¿Es la fibrosis quística hereditaria?
Si. Su origen está en la mutación de un gen del cromosoma 7 lo que genera una excesiva cantidad de moco que se acumula en las vías respiratorias y páncreas.
¿Qué esperanza de vida tiene alguien con fibrosis quística?
La esperanza de vida en pacientes con fibrosis quística cada vez es mayor, siendo a día de hoy de casi 40 años en muchos casos.
¿Cómo se hace el test del sudor?
Mediante el test del sudor se mide la cantidad de cloruro sódico presente en el organismo, el cual es indicador de fibrosis quística.
La prueba se realiza colocando un par de electrodos en la zona delantera del brazo y se suministra un medicamento a través de ellos, de manera que se estimulan las glándulas sudoríparas.Justo después se coloca otro dispositivo que recogerá la muestra de sudor.
¿Es contagiosa la fibrosis quística?
No. Es una enfermedad congénita que se origina por la mutación de un gen.
¿A quién afecta la fibrosis quística?
Al ser una enfermedad congénita que se transmite de manera autosómica recesiva, es decir, que se transmite de padres sanos a hijos , es a estos a quienes afecta. Esta enfermedad además es más frecuente en personas de raza blanca.

Enfermedad
Pectus Excavatum
¿Qué es el pectus excavatum?
El pectus excavatum, también conocido como pecho en embudo o pecho hundido, es una malformación congénita de la pared torácica, que se produce por el crecimiento anormal del esternón y de las costillas que se articulan sobre él, produciendo un hundimiento del tórax. Aparece en forma leve en 1 de cada 1.000 nacimientos y 1 de cada 10.000 en forma más grave. Presenta una problema de insuficiencia respiratoria o problemas cardíacos en sus casos más graves. Es una enfermedad que puede ser desde leve hasta grave.
Tipos de pectus excavatum
Los tipos de pectus excavatum son:
Pectus excavatum leve : muy poco perceptible en la infancia, aumenta en la adolescencia pero no afecta a otros órganos torácicos.
Pectus excavatum grave : crea una profunda hendidura en el tórax, que ejerce presión sobre los pulmones y el corazón.
Causas del pectus excavatum
No se conoce claramente la causa de esta malformación, si bien puede aparecer con frecuencia en una misma familia, lo cual podría indicar un origen genético .
Síntomas de pectus excavatum
El síntoma principal del pectus excavatum es la anomalía del tórax que aparece hendido y con un aspecto de metido hacia dentro.
Puede dar lugar a fatiga al hacer ejercicio, disnea (dificultad para respirar), dolor en el pecho, aumento de la frecuencia cardíaca y palpitaciones, infecciones respiratorias frecuentes, tos y opresión del pecho.
Tratamiento para el pectus excavatum
En los casos leves en los cuales no hay compromiso respiratorio ni defecto físico, se puede no realizar tratamiento. En los más marcados se suele realizar tratamiento quirúrgico utilizando diferentes técnicas.
Procedimiento de Ravitch : en el cual el cirujano extrae el cartílago anómalo, reconstruye el esternón, y fija todo mediante barras metálicas. Cuando la estructura está fijada se extraerán las barras en un segundo acto quirúrgico que se realiza unos seis meses después. Se realiza en pacientes de entre 13 y 22 años.
Procedimiento de Nuss : se sitúa una barra metálica colocando el esternón en su lugar, para introducirlas, se hace una pequeña hendidura, a la que se añadirá una barra estabilizadora para mantenerlo en su sitio. El pecho se va a ir remodelando de forma constante durante unos 4 años. Esta técnica se realiza en niños de unos 9 años y es menos agresiva y es la que se suele usar en el momento actual.
Sistema de ventosas : desde hace unos años se está usando un método a base de ventosas que produce un vacío. El sistema logra la alineación del esternón mediante este vacío, y puede usarse en niños desde los cinco años hasta la edad adulta. Se comienza a usar poco a poco y se va a ir usando mayor tiempo hasta hacerse su uso prácticamente constante, una vez que se consigue la corrección, se va a proceder a mantener el uso del sistema de modo intermitente durante un año más, para conseguir la estabilidad de la mejoría conseguida.
Pruebas complementarias del tratamiento de pectus excavatum
El examen físico será necesario para el diagnóstico, seguido de pruebas radiológicas como la radiografía de tórax o de esternón, el TAC torácico, un electrocardiograma, pruebas de función respiratoria y, en caso necesario, se realizarán pruebas genéticas que permitan descartar los síndromes genéticos que pueden tener el pectus excavatum como uno de sus síntomas, como ocurre con el síndrome de Marfan o el síndrome de Poland.
Factores desencadenantes del pectus excavatum
Se desconocen los factores desencadenantes del pectus excavatum, salvo en los casos de síndromes asociados como síndrome de Marfan, síndrome de Poland, síndrome de Ehlers-Danlos, síndrome de Turner, síndrome de Noonan y la osteogénesis imperfecta, todos ellos síndrome genéticos que se asocian a esta malformación .
Factores de riesgo del pectus excavatum
Casos de pectus excavatum en la familia.
Complicaciones del pectus excavatum
Infecciones respiratorias de repetición.
Problemas cardíacos.
Taquicardia.
Palpitaciones.
Dificultad para expandir los pulmones.
Insuficiencia respiratoria.
Prevención del pectus excavatum
No se conocen medidas preventivas para evitar el pectus excavatum.
Especialidades a las que pertenece el pectus excavatum
El pectus excavatum será operado por el cirujano torácico , pero precisará de controles médicos por parte del neumólogo y el cardiólogo en los casos más graves.
Preguntas frecuentes
¿Qué ejercicios son recomendables para el pectus excavatum?
Los ejercicios de fisioterapia en el pectus excavatum serán los necesarios para el control de la postura. Se trata de establecer tensiones en la partes hundidas del tórax para lograr su tensión. Se enseñará al paciente a relajar el diafragma, lo que hará que se expanda mejor la caja torácica. Los principales ejercicios son:
Ejercicio de relajación del diafragma : se tumba el paciente boca arriba con la espalda apoyada en el suelo y las piernas en flexión. Se procederá a realizar un masaje debajo de las costillas, desde la zona central y hacia el lateral. El masaje será en forma de círculos y se deberá realizar con la espiración , tras ello, con el dedo índice y el corazón se procede a realizar movimientos rectos hacia el exterior del tórax. El tercer ejercicio se realiza en movimiento vertical o paralelo al ombligo con los mismos dos dedos anteriores.
Ejercicio de movilización costal : se tratará de abrazar los omóplatos a la vez que se gira hacia ambos lados de modo alternativo, las manos se irán bajando hacia abajo mientras se realiza el mismo movimiento de balanceo.
Ejercicio de estiramiento : el paciente tumbado situará sus manos sobre la pelvis , con los codos apoyados en el suelo para proceder entonces a contraer la musculatura abdominal, el ejercicio de estiramiento se realiza al espirar.
¿Cómo se llama la operación para reducir el pectus excavatum?
Existen dos técnicas quirúrgicas para reducir el pectus excavatum, la operación de Ravitch , en la cual se extirpan los cartílagos dañados y se ponen de barras de sujeción, es una operación que hoy casi no se realiza, y la operación de Nuss , en ella, se realiza una incisión mínima, se mete a través de ella un fijador que levanta el esternón, y luego una barra más que lo fija; es menos cruenta, y es la que se suele hacer en el momento actual.
¿Cuáles son los cuidados tras la operación de pecho hundido?
El paciente deberá controlar los movimientos de tórax evitando realizar grandes esfuerzos. La herida deberá seguir curas según las instrucciones prescritas por el cirujano, quien indicará cómo cuidar la misma. En general se deberá lavar con agua y jabón y posteriormente secar de forma adecuada, dando Betadine o Clorhexidina . No se deberá realizar actividades deportivas hasta seis meses después de la cirugía, y no se deben realizar deportes de alto riesgo o que exijan el movimiento del torso hasta pasado un año de la cirugía.
¿Cuánto cuesta la operacion de pectus excavatum?
Aunque el precio puede ser variable dependiendo de las características de cada paciente y su situación personal, el precio suele ser unos 5.000 euros .

Enfermedad
Difteria
¿Qué es la difteria?
La difteria es una enfermedad infecciosa producida por una bacteria , la corynebacterium diphtheriae , en la antigüedad conocida con el nombre vulgar de garrotillo. En España no se dan casos de difteria desde el año 1986, pero sí se producen en otras zonas del este de Europa. Tiene una tasa de mortalidad en la difteria no cutánea de entre 5 y 10% , suele aparecer en los meses fríos y es más frecuente en menores de 15 años no inmunizados y en adultos que perdieron la inmunidad. Puede dar lugar a obstrucción de las vías aéreas, también puede producir miocarditis (inflamación del miocardio) y en algunos casos puede dar lugar a una neuropatía (enfermedad del sistema nervioso). Es una enfermedad grave dada su tasa de mortalidad.
Tipos de difteria
Los tipos de difteria son:
Difteria nasal : puede ser leve y cronificarse, da lugar a ulceraciones en el interior de la nariz.
Difteria faringoamigdalina: cursa con dolor de garganta y aumento de los ganglios del cuello, en casos graves pueden crearse membranas traqueales que pueden obstruir las vías respiratorias
Difteria cutánea : la mayoría de las lesiones se producen en los miembros, en ocasiones son superficiales y en el tórax lesiones más profundas a modo de úlceras que se recubren de una membrana grisácea.
Causas de la difteria
La causa de la difteria es la infección por parte del corynebacterium diphtheriae .
Síntomas de la difteria
En la difteria faríngea, se produce dolor de garganta, fiebre, dificultad para tragar, aumento del ritmo cardíaco, náuseas, vómitos y escalofríos . Posteriormente se va a observar la presencia de una membrana sobre las amígdalas, puede haber ronquera, cuello hinchado y ruido al respirar.
En la piel se pueden producir úlceras que no curan y que presentan una membrana gris que la recubre.
En la nariz se suele producir un cuadro más leve en el cual se producen secreciones.
En casos más graves puede haber postración (decaimiento), palidez e incluso llegar al coma.
Tratamiento para la difteria
Se debe administrar la antitoxina diftérica tan pronto como se sospeche la enfermedad, aunque no se tengan pruebas de laboratorio que lo confirmen.
El tratamiento de la difteria es con antibióticos como la Penicilina G Procaina en vía intramuscular en dosis de 300.000 unidades internacionales en pacientes menores de 10 kg y de 600.000 unidades internacionales en pacientes de más de 10 kg durante 14 días o la Eritromicina a dosis de 40 mg/kg/día en dosis cada 6 horas durante 14 días para eliminar la bacteria.
Pruebas complementarias del tratamiento de la difteria
Las pruebas complementarias serán el cultivo de las membranas y la tinción de gram que colorea las bacterias.
Se realiza una prueba de producción de la toxina difteria o bien se busca en la bacteria el gen productor de la misma.
Deben realizarse pruebas de electrocardiograma que permitirán descartar lesiones del corazón llamadas miocarditis.
Factores desencadenantes de la difteria
No hay factores desencadenantes de la difteria salvo el contagio con la bacteria corynebacterium diphtheriae .
Factores de riesgo de la difteria
El factor de riesgo principal es no presentar inmunidad para la bacteria, esta inmunidad solo se adquiere mediante la vacunación.
Complicaciones de la difteria
Obstrucción respiratoria.
Miocarditis.
Coma
Prevención de la difteria
Vacunación de la difteria mediante la vacuna con tétanos-difteria-tosferina y vacunación en adultos con la vacuna de tétanos-difteria con una periodicidad de cada diez años. La eficacia de la vacuna es del 97%.
Especialidades a las que pertenece la difteria
La difteria es una enfermedad que se controla por los servicios de medicina infecciosa de los hospitales que están formados por médicos de medicina interna.
Las difterias amigdalinas serán ingresadas en UCI y por tanto serán controladas por médicos intensivistas.
Preguntas frecuentes:
¿Cómo se contagia la difteria?
La difteria se contagia a partir de personas infectadas, que mediante las gotitas emitidas en estornudos y/o toses , dejan las bacterias en el aire, desde donde serán adquiridas por otras personas sensibles al germen.
¿Cuál es el nombre de la vacuna contra la difteria?
La vacuna contra la difteria es la vacuna DPT en niños, ya que lleva también inmunidad contra las tosferina y el tétanos. En los adultos es la Td, que lleva tambien la inmunidad para la tosferina.
¿Qué es el DTP?
La DTP es la vacuna contra el tétanos corresponde a la letra T, la tosferina corresponde a la letra P, ya que la bacteria que la produce es la bordetella pertussi , y la difteria que corresponde a la letra D.
Esta es la vacuna que se administra a los niños a los 2-4-6 meses con un recuerdo a los 18 meses y otro a los 4 años.
¿En qué países es más probable coger la difteria?
En Asia, países como India, Nepal y Bangladesh, Irán y Afganistán. En el sudeste asiático, países como Filipinas, Indonesia, Vietnam, Laos y Papua Nueva Guinea. En África en Nigeria. En Sudamérica en Brasil. Y en Europa en Albania, Armenia, Azerbaiyán, Bielorrusia, Estonia, Georgia, Kazajistán, Latvia, Lituania, Moldavia, Rusia, Tayikistán, Turkmenistán, Ucrania y Uzbekistán
¿Qué es la poliomielitis?
La poliomielitis es una enfermedad infecciosa, producida por el virus de la polio , que da lugar a daño en el tejido nervioso pudiendo causar parálisis.
Los síntomas son fiebre, cansancio, cefalea, vómitos, rigidez de cuello y dolor en los miembros, y puede causar una parálisis permanente. Es una enfermedad sin cura pero que se previene de modo eficaz mediante la vacunación.

Enfermedad
Apnea del Sueño
¿Qué es la apnea del sueño?
La apnea del sueño es un trastorno en el cual la respiración se detiene y recomienza repetidas veces mientras se duerme . Es posible que se tenga apnea del sueño si se ronca sonoramente y si la persona se siente cansada, inclusive después de una noche completa de sueño. La apnea del sueño ocurre con mucha más frecuencia en adultos mayores. Los hombres son dos veces más propensos a tener apnea del sueño que las mujeres, sin embargo, el riesgo aumenta en las mujeres con sobrepeso y también después de la menopausia, raramente, pero también puede ocurrir en niños. Es común y en ocasiones puede ser grave.
Tipos de apnea del sueño
Existen 3 tipos de apnea del sueño estas son:
Apnea obstructiva del sueño : la forma más común, que ocurre cuando los músculos de la garganta se relajan. En ella, la interrupción del flujo aéreo se debe a una oclusión de la vía respiratoria. Sucede mientras el paciente duerme porque, al encontrarse tumbado, las partes blandas de la garganta se desplazan hacia atrás y ocluyen la vía. Esto puede provocar que el paciente se despierte frecuentemente.
Apnea central del sueño : ocurre cuando el cerebro no envía señales correctas a los músculos que controlan la respiración. En este tipo de apnea la vía respiratoria permanece abierta, pero como los músculos respiratorios permanecen inactivos y se produce el cese del flujo respiratorio.
Apnea del sueño mixta : en estos casos se comienza como una apnea central y con el tiempo acaba teniendo un componente obstructivo.
Causas de la apnea del sueño
En condiciones normales, cuando las personas duermen, la vía aérea está permeable, es decir, pueden respirar con tranquilidad, sin embargo, en algunas fases del sueño los tejidos se cierran y bloquean la vía respiratoria causando la apnea.
Síntomas de la apnea del sueño
Los ronquidos son la manifestación más visible que puede alertar al paciente sobre la posibilidad de tener apnea del sueño. Algunos otros síntomas de la apnea del sueño son: ronquidos fuertes que, por lo general, son más prominentes en la apnea obstructiva del sueño, despertares abruptos acompañados de falta de aire, despertarse con la boca seca o con dolor de garganta , problemas de atención, dificultad para permanecer dormido, somnolencia diurna excesiva, irritabilidad, dolor de cabeza por la mañana, cansancio permanente, falta de energía , disfunción sexual, sudores nocturnos o falta de energía.
Tratamiento de la apnea del sueño
La apnea del sueño no suele resolverse por sí sola, pero sí que puede tratarse. Existen diferentes opciones terapéuticas, que deben ser seleccionadas según la gravedad del cuadro. De esta forma, en algunas ocasiones pueden indicarse simplemente medidas de autocuidado , como perder peso o dormir en determinadas posturas, realizar ejercicios, y evitar el consumo de alcohol o sedantes. Otros remedios son dispositivos bucales que puestos en la boca logran un adelantamiento de la mandíbula y disminuyen los ronquidos.
Sin embargo, la mayoría de los pacientes con apnea del sueño moderada o grave, necesitarán el empleo de una mascarilla nasal de presión positiva continua en las vías respiratorias llamada CPAP. El aire se transmite a través de un tubo hasta una mascarilla que se ajusta en la nariz y en ocasiones en la boca, evitando los trastornos respiratorios y normalizando el transcurso del sueño.
No obstante, en algunas ocasiones es necesaria la cirugía . Esta suele convertirse en una opción solamente después de que otros tratamientos han fallado. Por lo general, se recomienda probar los demás tratamientos durante al menos tres meses antes de considerar la cirugía. El objetivo de la cirugía para la apnea del sueño es agrandar las vías respiratorias a través de la nariz o la garganta, que pueden vibrar y causar los ronquidos o que pueden bloquear las vías respiratorias superiores y causar la apnea del sueño.
Pruebas complementarias de la apnea del sueño
Para el diagnóstico y tratamiento de la apnea del sueño, es necesario realizar una polisomnografía nocturna . Durante esta prueba, conectan al paciente a un equipo que controla la actividad del corazón, la de los pulmones y la del cerebro, los patrones de respiración, el movimiento de piernas y brazos y los niveles de oxígeno en sangre mientras duerme. En algunos casos se pueden realizar pruebas del sueño en casa. Por lo general, en estas pruebas se miden el pulso, el nivel de oxígeno en sangre, el flujo de aire y los patrones de respiración. Si se tiene apnea del sueño, los resultados de la prueba mostrarán una reducción en el nivel de oxígeno durante las apneas y aumentos subsiguientes con el despertar.
Factores desencadenantes y de riesgo de la apnea del sueño
Los factores desencadenantes y de riesgo de la apnea de sueño incluyen: sobrepeso, vías respiratorias estrechas, sexo masculino (las apneas del sueño predominan en los varones), la edad, antecedentes familiares, el consumo de alcohol, sedantes o tranquilizantes, fumar y padecer congestión nasal.
Complicaciones del tratamiento de la apnea del sueño
Las complicaciones de la apnea del sueño incluyen:
Fatiga diaria: las personas que sufren de apnea del sueño experimentan somnolencia diurna, fatiga e irritabilidad graves.
Presión arterial alta o problemas cardíacos: el súbito descenso de los niveles de oxígeno en la sangre que ocurre durante la apnea del sueño aumenta la presión arterial y sobrecarga el aparato cardiovascular.
Hipertensión pulmonar.
Depresión.
Accidente cerebrovascular.
Problemas hepáticos.
Privación del sueño en los compañeros de cama.
Prevención de la apnea del sueño
Para prevenir la apnea del sueño es necesario:
Evitar el sobrepeso.
No fumar.
Evitar el consumo de alcohol.
Alimentación sana y equilibrada.
Especialidades a las que pertenece la apnea del sueño
El otorrinolaringólogo es el médico especialista entrenado en el diagnóstico y tratamiento de las patologías de nariz y garganta, entre ellas la apnea del sueño.
Preguntas frecuentes:
¿Qué es la disnea?
La disnea es la dificultad respiratoria que se manifiesta como una sensación de falta de aire en los pulmones.
¿Cómo se llama la respiración lenta?
La respiración que se vuelve lenta es llamada bradipnea.
¿Qué es un broncoespasmo?
Un broncoespasmo es una contracción anormal del músculo liso de los bronquios, que puede provocar un estrechamiento u obstrucción aguda de las vías respiratorias.
¿Qué son las sibilancias?
La sibilancia es un ruido inspiratorio o espiratorio agudo que aparece en el árbol bronquial como consecuencia de una estenosis (estrechez de las vías respiratorias).
¿Puedo ahogarme por tener apnea del sueño?
Sí, pero esto solo ocurre por pequeños momentos bastante rápidos, y si se presenta este síntoma se debe consultar a un médico.
Artículos por especialidad
CertificadosAlergologíaAnatomía PatológicaAnestesiología y ReanimaciónAngiología y Cirugía VascularAnálisis ClínicosAparato DigestivoCardiologíaChequeosCirugía General y del Aparato DigestivoCirugía General y del Aparato Digestivo PediátricaCirugía Oral y MaxilofacialCirugía Ortopédica y TraumatologíaCirugía Ortopédica y Traumatología PediátricaCirugía PediátricaCirugía Plástica y ReparadoraCirugía TorácicaClínica u HospitalDermatología Médico-Quirúrgica y VenereologíaEndocrinología y NutriciónEnfermeríaFisioterapiaGenética HumanaGinecología y ObstetriciaInmunologíaLogopedia y FoniatríaMedicina Estética y Unidad LaserMedicina Física y RehabilitaciónMedicina GeneralMedicina InternaMedicina NuclearMedicina del DeporteNefrologíaNeumologíaNeurocirugíaNeurofisiología ClínicaNeurologíaNutrición y DietéticaOdontología y EstomatologíaOftalmologíaOncología MédicaOncología RadioterápicaOsteopatíaOtorrinolaringologíaPediatríaPodologíaPoliclínicasPreparación al PartoPsicologíaPsiquiatríaRadiodiagnóstico-Diagnóstico Por ImagenReumatologíaTricologíaUnidad del DolorUrgencias HospitalariasUrología
Todas las especialidades  Savia
Savia