Pediatría
La especialidadArtículos especializados
Enfermedades
Síntomas
Otros contenidos

Enfermedad
Pediculosis
¿Qué es la pediculosis?
La pediculosis, también conocidos como piojos, es un tipo de ectoparásito (parásitos externos), muy contagioso, producida por una infestación del piojo. Afecta las partes del cuerpo con vello o pelo del cuerpo o de la ropa, infectados con huevos o larvas de piojos (liendres) o piojos adultos. Las etapas larvarias de este insecto se alimentan con sangre humana, provocando gran picazón. La pediculosis se contagia fácilmente de persona a persona durante el contacto directo. Tiene distribución mundial y puede afectar a todos los niveles sociales y razas. Es más frecuente en niños de 5-15 años en edad escolar y suele ser más común en el sexo femenino. Es una enfermedad común y es leve, ya que responde muy bien al tratamiento y sobre todo no pone en riesgo la vida de la persona que la padece.
Tipos de pediculosis
La pediculosis se clasifica según el lugar donde se manifieste, esta puede ser:
Pediculus humanus capitis : son los piojos de la cabeza, están normalmente localizados sobre el cuero cabelludo. Producen picazón intensa sobre todo parte posterior de la cabeza y detrás de las orejas y afectan mayormente a niños de edad escolar. Está infestacion no tiene que ver con la falta de higiene, aunque en lugares de hacinamiento y escasas condiciones higiénicas son más frecuentes.
Pediculus humanus pubis : el piojo del pubis se conoce con el nombre científico Phthirus pubis , y se conoce comúnmente como ladilla. Son criaturas pequeñas de seis extremidades que invaden el vello de la región púbica y la infestan con sus huevos. Estos piojos también pueden infestar el vello axilar y las cejas, pero son arrastrados a la región púbica. Son frecuentes entre personas sexualmente activas.
Pediculosis del cuerpo : los piojos se encuentran o viven en las prendas de ropa y depositan sus huevos. Solo salen del cuerpo y se dirigen a la piel para alimentarse con la sangre del huésped y luego regresan a la ropa. Se pueden ver en personas que rara vez se quitan la ropa y viven en situaciones de hacinamiento donde las personas viven muy juntas y sin higiene. Se transmiten por el contacto corporal o por compartir vestimenta. Presentan pápulas pruriginosas, excoriaciones y áreas de pigmentación.
Causas de la pediculosis
La causas de la pediculosis, es principalmente la deposición de los huevos pequeños sobre el cuero cabelludo que lucen como escamas, pero en lugar de desprenderse del cuero cabelludo, permanecen firmemente adheridos. Estos pueden sobrevivir en la ropa, tapetes y en la cama hasta 10 días y sus huevos pueden vivir por más de dos semanas. También se diseminan fácilmente y se pueden pegar cuando se entra en contacto cercano con una persona infestada o toca sus ropas.
Tanto los piojos de cabeza como los corporales, pueden transmitirse mediante el contacto directo con una persona infestada. El compartir ropa, peines o cepillos también puede facilitar la transmisión de estos insectos. Mientras que otros medios son posibles, los piojos púbicos son transmitidos con mayor frecuencia a través del contacto sexual.
Síntomas de la pediculosis
Los síntomas de la pediculosis incluyen: sentir prurito intenso en el cuero cabelludo, picazón o rascarse en el área del cuerpo de la que los piojos se alimentan. Huevos de piojo o liendres en el pelo y pequeños bultitos rojos o llagas provocadas por el rascado, entre otros síntomas.
Tratamiento para la pediculosis
El tratamiento para la pediculosis consiste en matar las liendres, ninfas y piojos. Existen tratamientos con pediculicidas tópicos que suelen ser muy eficaces, como son Permetrina, Lindano, Malation, Benzoato de bencilo y medicamentos orales utilizados en caso de resistencia como son la Ivermectina , suprimen la conducción de los impulsos nerviosos de los insectos y Trimetropim sulfa . Para el prurito o picazón también se pueden administrar antihistamínicos orales o de personas con piojos en la cabeza. El uso de Lindano no se recomienda en bebés, niños pequeños y mujeres embarazadas o que estén lactando. Se recomienda repetir el tratamiento entre 7-10 días después para asegurar que no hayan sobrevivido liendres. Hay peines especiales llamados liendreras, disponibles para retirar las liendres del cabello. Se deben seguir al pie de la letra las instrucciones del medicamento utilizado con relación a la dosis y duración del tratamiento.
Pruebas complementarias del tratamiento de la pediculosis
Las pruebas diagnósticas para el tratamiento de la pediculosis, es principalmente la exploración y observación directa del piojo y las liendres en el cuero cabelludo. Frecuentemente se detecta la infestación por la visualización de liendres. También existen otras formas como son: el peine de dientes finos llamado liendrera, más más rápido y útil para encontrar los piojos y liendres principalmente en región occipital y retroauricular. Lupa con luz o lámpara de cuello de ganso, o lámpara de luz ultravioleta o de wood .
Factores desencadenantes de la pediculosis
El factor desencadenante principal de la pediculosis es tener contacto con una persona infestada de piojos .
Factores de riesgo de la pediculosis
Los factores que aumentan el riesgo de tener pediculosis incluyen:
Los niños de edad escolar primaria tienen mayor riesgo de tener pediculosis.
Los piojos de la cabeza suelen migrar de un cabello a otro, independientemente de la higiene de la persona.
Las personas que tienen relaciones sexuales sin protección y sin conocer a su pareja sexual tienen más riesgo de tener pediculosis púbica.
La personas que viven muy juntas o hacinamientos, como albergues, campos de refugiados o que vivan en la calle, que no se cambien la ropa y con poca higiene para el aseo son propensos a la pediculosis corporal.
Complicaciones de la pediculosis
La pediculosis es un tipo de enfermedad que no presenta riesgos para la vida de las personas . Se puede producir una dermatitis por el rascado continuo sobre la piel donde pica el piojo.
Prevención de la pediculosis
Para prevenir la pediculosis se debe :
Evitar el contacto físico con personas infestadas y sus pertenencias, especialmente ropa, accesorios para la cabeza y ropa de cama.
Es muy valiosa la educación de la salud con relación al ciclo vital de los piojos, el tratamiento apropiado y la importancia de lavar la ropa y la ropa de cama con agua caliente o lavarla en seco, para destruir los piojos y liendres.
Hacer una inspección directa periódica de la cabeza de los niños y, cuando sea indicado, del cuerpo y de la ropa, especialmente en colegios, instituciones, asilos y campamentos de verano.
Revisar frecuentemente la cabeza de los niños usando el peine.
Especialidades a las que pertenece la pediculosis
Las especialidades a las que pertenece la pediculosis son dermatología, medicina de familia o general y en casos de niños, pediatría.
Preguntas frecuentes
¿Qué es una liendre?
Las liendres son los huevos depositados por los piojos hembras en el pelo de las personas, donde permanecen hasta que se abren de 8-10 días aproximadamente. Tienen una forma de cápsula ovalada, de color blanco cuando son visibles y amarillentas cuando están vacías o muertas (secas), se pueden confundir muy fácilmente con la caspa. Poseen una membrana que las rodea y hace que se fijen al pelo por medio de una sustancia gomosa similar a la de un pegamento.
¿Qué es un piojo?
Los piojos, también llamados Pediculus humanos capitis , son insectos parasitarios que se encuentran en el pelo de las personas. El piojo adulto tiene un tamaño de 2 a 4 mm. de largo, tiene 6 patas y su color es de marrón a grisáceo. Las hembras son las que depositan las liendres y por lo general son más grandes que los machos, y pueden vivir hasta 30 días en la cabeza de la persona. Para sobrevivir, el piojo adulto necesita alimentarse de sangre.
¿Por qué se usa vinagre con los piojos?
El vinagre se usa para los piojos porque contiene ácido acético, que permite disolver el cemento que mantiene a las liendres pegadas al cabello. También es un antiséptico y el olor fuerte que tiene no le gusta a los piojos. El uso del vinagre puede facilitar su extracción pasando un peine fino de la raíz a la punta. Es uno de los remedios caseros más antiguos que se utiliza para tratar los piojos. Aunque en ocasiones no suele ser efectivo en todos lo casos y se debe acudir a otros tratamientos.
¿Qué son las ladillas?
La ladillas son llamadas pthirus pubis, y son piojos púbicos, los cuales son pequeños insectos parasitarios que se adhieren a la piel y el vello del área genital. Se transmiten durante el contacto sexual y sobreviven alimentándose de la sangre de la persona que lo tiene.
¿Es verdad que los piojos se hacen resistentes a los productos de erradicación?
Los piojos pueden hacerse resistentes a los productos de erradicación, sólo cuando se usan en las personas que no tienen piojos, es decir, si lo utilizan de manera preventiva, puede que algunos tratamientos ya no sean efectivos para erradicarlos porque le crean resistencia.

Enfermedad
Oxiuriasis
¿Qué es la oxiuriasis?
La oxiuriasis, también conocida como enterobiasis, es una infestación parasitaria intestinal , causada por el Oxiuro enterobius vermiculares, que es un pequeño helminto nematodo (gusano), un parásito del hombre de forma cilíndrica y color blanco que mide alrededor de 1 cm. Es la enfermedad parasitaria más común alrededor del mundo, el ser humano es el único huésped natural y su infección se produce en todos los países y grupos socioeconómicos. Es más frecuente en niños de entre 5-11 años de edad, pero puede aparecer a cualquier edad, aunque rara vez se puede ver en niños de 2 años. Tiene una prevalencia alta. Es una enfermedad leve que responde muy bien al tratamiento adecuado.
Causas de la oxiuriasis
La causa principal de las oxiuriasis es la presencia del parásito Enterobius vermicularis u oxiuro , que es un gusano nematodo, redondo, pequeño, de 1 cm. de longitud, blanco y filamentoso y que habita exclusivamente en el intestino grueso de los seres humanos. Mientras la persona afectada duerme, la hembra sale del tracto intestinal y pone los huevos en la piel que rodea al ano, tiene la capacidad de producir diariamente varios miles de huevos, los cuales tienen un periodo de incubación de 3-6 semanas.
La infestación se inicia con la ingesta de los huevos de Enterobius vermicularis, que se puede dar a través de las manos contaminadas con huevos, por medio de fomites, o por la presencia de huevos en la ropa de cama o toallas, entre otras que permitan su ingreso al tracto digestivo.
Síntomas de la oxiuriasis
La mayoría de las personas infectadas por oxiuriasis no experimentan síntomas al principio , generalmente estos se presentan a partir de la 2-4 semanas después del contagio. Los más frecuente son prurito (picazón) perineal más intenso durante la noche, así como vulvar y nasal. Falta de sueño, irritabilidad, nerviosismo, inquietud, adelgazamiento, dolor abdominal, náuseas y bruxismo. Los gusanos adultos pueden migrar a la región vaginal y producir vulvovaginitis (inflamación de la vulva y la vagina) y flujo vaginal.
Tratamiento para la oxiuriasis
El tratamiento de la oxiuriasis es simple y con una tasa de curación muy alta. Pero para que sea del todo efectivo se debe administrar tanto al paciente afectado como a los familiares que viven en la misma casa para así disminuir el riesgo de una nueva infección. El tratamiento consiste en:
Albendazol , 400 mg. en una sola dosis, vía oral. Se debe repetir la dosis en dos semanas.
Mebendazol , 100 mg, 2 veces al día durante 3 días consecutivos por vía oral . También se puede administrar 100 mg. en una sola dosis. Se repite la dosis en dos semanas. Pamoato de pirantel, 10 mg/kg, una sola dosis, hasta máximo de 1.000 mg.
Pruebas complementarias del tratamiento de la oxiuriasis
Las pruebas diagnósticas para el tratamiento de la oxiuriasis se dan a través del método de Graham , que utiliza una cinta adhesiva en la piel alrededor del ano para que los huevos que se encuentran en esta región se peguen a la cinta. Estos huevos, por lo tanto, son colocados en una lámina de vidrio y visualizados en un microscopio para detectar el Oxiuro .
Factores desencadenantes de la oxiuriasis
El factor desencadenante de la oxiuriasis es la presencia del Oxiuro o Enterobius vermicularis .
Factores de riesgo de la oxiuriasis
Los factores de riesgo de la oxiuriasis son:
La edad, son más frecuente en niños.
Mala higiene personal: hacinamiento, vivir con familias afectadas por la parasitosis.
Manos contaminadas con los huevos de Oxiuros. Si el paciente se rasca el ano con sus manos puede pasar los huevos por muchos medios y transmitirlo a otras personas.
Complicaciones de la oxiuriasis
Las compliccaiones de la oxiuriasis son:
La parasitosis puede ascender desde la vagina hacia el peritoneo, donde es englobado llegando a producir una peritonitis (inflamación del peritoneo por una infección).
El rascado del ano y sus alrededores puede causar excoriaciones e infecciones añadidas de la piel por otros gérmenes más agresivos como algunas bacterias.
Prevención de la oxiuriasis
La prevención de la oxiuriasis consiste en :
Tener una buena higiene personal adecuada.
Lavarse las manos después de ir al baño y antes de comer.
Se recomienda bañarse todos los días.
Cambiar la ropa interior con regularidad.
Aconsejar a los niños a no rascarse la zona anal.
No introducir las manos en la boca o ningún objeto como los juguetes.
La ropa de cama debe ser cambiada con regularidad y lavarse con agua caliente.
Especialidades a las que pertenece la oxiuriasis
Las especialidades medicas a las que pertenece la oxiuriasis son pediatría si afecta a los niños y en adultos medicina general o medicina interna .
Preguntas frecuentes
¿Qué son los oxiuros?
Los Oxiuros, también conocidos como lombrices intestinales, son parásitos del tubo digestivo que se parecen a los gusanos y que pueden vivir en el colon y el recto. Tienen forma de unos filamentos blancos.
¿Cómo se producen lombrices en los niños?
Las lombrices se producen en los niños por autocontagio, básicamente por la boca cuando se ingieren los huevos del parásito, al rascarse el ano con las manos y luego llevarlas a la boca o al ingerir un alimento que esté en contacto con el Oxiuro o algún objeto o juguete a la boca. Los huevos llegan hasta el intestino delgado donde salen las larvas, y cuando llegan al intestino grueso se hacen adultos. A los uno o dos meses las hembras se reproducen y ponen los huevos.
Si tengo lombrices… ¿Puedo tomar azúcar?
Si tienes lombrices puedes comer azúcar, ya que esto no está implicado con el contagio de las lombrices.

Enfermedad
Rubéola
¿Qué es la rubéola?
Conocida también como tercera enfermedad , sarampión alemán o sarampión de los tres días . La rubéola es una enfermedad infecciosa exantemática producida por un virus del género Rubivirus .
Antes de la introducción de la vacunación infantil, la rubéola afectaba más a los niños entre 5 y 9 años . Desde el desarrollo de la vacuna la prevalencia de la enfermedad, en niño, ha disminuido drásticamente y pueden verse más episodios en adulto. Es una enfermedad endémica , con presentación de casos anuales aislados y ciclos epidémicos sobre todo en primavera , existiendo mayor riesgo en aquellas regiones donde hay una baja vacunación contra la rubéola (en estos casos con afectación infantil mayoritariamente).
Suele ser un proceso benigno autolimitado , aunque siempre hay riesgo de que surja una complicación.
Tipos de rubéola
Rubéola en la infancia y adultos (postnatal): Padecimiento de las manifestaciones clásicas de la enfermedad con lesiones dérmicas en la piel (exantema).
Rubéola prenatal o síndrome de rubéola fetal: A través de la transmisión de la mujer embarazada se producen malformaciones congénitas en el feto o embrión.
Causas de la rubéola
La causa de la rubéola es la infección por el virus de la rubéola ( Rubivirus de la familia Togaviridae ), transmitido por vía respiratoria (secreciones, saliva, etc), de persona a persona por contacto prolongado con un paciente que padece la enfermedad. El virus se reproduce en la mucosa del sistema respiratorio y a través del sistema linfático llega a la sangre, desde donde se localiza posteriormente en la piel. En el caso de mujeres embarazadas, el virus llega a la placenta lo que puede dar lugar a una infección del feto.
Síntomas de la rubéola
Rubéola en la infancia y adultos: Tras un periodo de incubación de 14 – 21 días, aparece la fase prodrómica de 1 – 2 días de duración en la que se presentan síntomas catarrales , malestar general y aumento del tamaño de los ganglios linfáticos (adenopatías) cervicales y retroauriculares (detrás de las orejas). Después, aparece la fase exantemática con aparición de una erupción dérmica a modo de pequeñas manchas no confluentes (que no se unen) en la cara y después en el resto del torso, desapareciendo al tercer día con mínima descamación.
Rubéola prenatal: La rubéola durante el embarazo puede presentarse en el embrión o en el feto de múltiples maneras; desde la no afectación al aborto o muerte fetal. Las manifestaciones más frecuentes en el recién nacido son la sordera, retraso mental, afectaciones oculares, cardiopatías congénitas, lesiones hepáticas, microcefalia (desarrollo insuficiente del cráneo), fisura palatina (deformación del paladar y el labio), etc.
Tratamiento para la rubéola
El tratamiento es sintomático con administración de analgésicos como el paracetamol para el control de la fiebre y el malestar general. En el caso de complicaciones o afectación congénita en el recién nacido, dependerá del tipo de manifestación que presente el paciente se requerirá un tipo u otro de tratamiento (cirugía, rehabilitación, etc).
Pruebas complementarias del tratamiento de rubéola
El diagnóstico es fundamentalmente clínico . Puede realizarse una analítica de sangre para la determinación de serología, cultivo o detección de anticuerpos (detección del virus en sangre o de producción de sustancias de defensa específicas contra el virus).
Factores desencadenantes de la rubéola
El principal factor de riesgo que desencadena la rubéola es no estar vacunado .
Factores de riesgo de la rubéola
No haber recibido la vacuna contra la rubéola contenida en la vacuna triple vírica.
Complicaciones de la rubéola
Artralgias (dolores articulares).
Artritis (infección e inflamación de las articulaciones).
Encefalitis (infección e inflamación del cerebro).
Dolor testicular.
Hepatitis (inflamación e infección del hígado).
Púrpura trombocitopénica (enfermedad hemorrágica con destrucción de las plaquetas).
En la rubéola prenatal pueden desarrollarse sordera, cataratas, afectación cardíaca y otras malformaciones.
Prevención de la rubéola
Vacunación (con virus atenuado dentro de la vacuna llamada triple vírica).
Adecuada higiene de manos y medidas de prevención en aquellos pacientes que presenten la enfermedad para evitar su transmisión (uso de pañuelos de papel, reposo domiciliario, etc).
Especialidades a las que pertenece la rubéola
En casos de rubéola no complicada, el diagnóstico y tratamiento puede llevarse a cabo por el médico de familia o pediatra .
Si existen complicaciones dependerá del tipo de manifestación clínica . Debe realizarse una evaluación hospitalaria por el servicio médico específico que trate cada complicación (neurología, hematología, etc.)
En el caso de infecciones producidas en una mujer embarazada , el ginecólogo será el encargado de hacer el seguimiento de la paciente junto con el apoyo de otros especialistas como médico internista, etc.
Los niños con rubéola congénita serán evaluados y tratados en el servicio de pediatría hospitalaria.
Preguntas frecuentes
¿Cuál es la vacuna de la rubéola?
La vacuna de la rubéola se incluye en la vacuna triple vírica junto con la vacuna del sarampión y la de la parotiditis (paperas).
¿Cuánto tiempo dura la rubéola?
Desde los primeros síntomas hasta la desaparición de las lesiones dérmicas pueden pasar en torno a 8 días (la fase prodrómica catarral de 1-5 días y las lesiones dérmicas 2-3 días).
¿Qué efectos produce la rubéola?
La forma más frecuente de presentación es un proceso catarral de vías respiratorias altas, aumento del tamaño de los ganglios linfáticos (estaciones del sistema de defensa) detrás de las orejas y en la nuca, con aparición de un “sarpullido” rosado en la cara que se extiende por todo el tronco y desaparece en 3 días.
¿Cómo se transmite la rubéola?
La rubéola se transmite por vía respiratoria a través de las pequeñas gotas que se expulsan con los estornudos, la tos, la saliva, secreciones, etc. Y por el contacto de persona a persona (sólo se transmite entre humanos). La rubéola congénita se transmite de la madre al feto a través de la placenta .
¿Qué pasa si una mujer embarazada tiene la rubéola?
Dependiendo del momento del embarazo en el que la madre adquiera la infección, el feto puede adquirir unas malformaciones u otras, sufriendo el llamado síndrome de rubéola fetal.
Enfermedad
Sarampión
¿Qué es el sarampión?
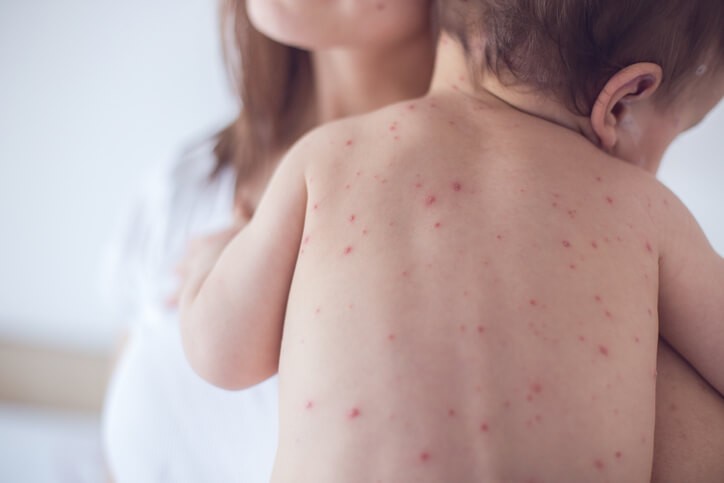
El sarampión es una enfermedad vírica altamente contagiosa , clasificada como una de las llamadas enfermedades exantemáticas , que se caracterizan por aparición de síntomas generales y que afectan a la piel con la presencia de “granitos” o “manchitas”.
Es una enfermedad que, antes de la vacunación generalizada contra el sarampión, se presentaba en niños de 5 – 9 años con epidemias recurrentes cada 2 – 5 años sobre todo en invierno y primavera . Con la introducción de la vacuna en España a partir de 1973 de forma individual, por un lado, y de forma conjunta con la vacuna triple vírica, que incluye la vacuna de la rubéola y la parotiditis, la frecuencia de aparición disminuyó de forma radical , siendo excepcional su presentación y elevándose también la edad de presentación por encima de los 10 años .
Aunque se considera una enfermedad vírica benigna en la mayoría de los casos, puede derivar en complicaciones que pueden llegar a ser graves .
Tipos de sarampión
Sarampión de presentación típica: presenta la sintomatología típica de la enfermedad .
Sarampión hemorrágico o negro: complicación del sarampión donde se producen múltiples lesiones hemorrágicas .
Sarampión modificado: se presenta en pacientes parcialmente inmunizados ( menores de 9 meses , vacunación parcial y forma raras de sarampión recurrente). Los síntomas en este caso son menos intensos .
Causas del sarampión
La causa del sarampión es el contagio del virus del sarampión (un mixovirus de la familia paramixovirus ), transmitido por la vía respiratoria de una persona infectada (a través de gotas de saliva, mocos, etc.). El periodo de transmisión de un paciente a otro se produce desde 10 días antes de la aparición de las primeras lesiones dérmicas.
Síntomas del sarampión
Inicialmente se tiene un periodo llamado prodrómico que dura aproximadamente 2 – 4 días, en el que aparece irritación de la conjuntiva del ojo (lo blanco del ojo), lagrimeo, estornudos, moqueo continuo, dificultad para tragar (disfagia), tos seca, afonía, malestar general, dolores generalizados o molestias con la luz (fotofobia). A los pocos días aparece fiebre alta.
Durante los tres y cuatro primero días del inicio de los primeros síntomas se observan unas pequeñas ”manchas” blanco-azuladas en la mucosa (revestimiento) del interior de la boca (manchas de Koplik), que son características de esta enfermedad. Posteriormente aparece un erupción o “sarpullido” en la piel , que comienza en la cabeza (detrás de las orejas) y se va extendiendo por el cuello, tronco, brazos y piernas, pudiendo afectar a las palmas de las manos y plantas de los pies. En raras ocasiones pueden verse afectados los oídos, pulmones y cerebro. Tras tres días, desaparecen en el mismo orden que aparecieron dando lugar a una descamación de la piel (excepto en palma de manos y planta de los pies).
Tratamiento para el sarampión
En los casos de sarampión típico sin complicaciones el tratamiento va destinado al control y disminución de los síntomas . Se pautan antitérmicos para disminuir la fiebre, lavados oculares con suero, adecuada hidratación bebiendo abundantes líquidos y reposo en el domicilio.
Solo en el caso de complicaciones como sobreinfecciones bacterianas se pauta un tratamiento antibiótico y, en caso de complicaciones graves y mala evolución del tratamiento, se hospitaliza al paciente.
Diagnóstico del sarampión
El diagnóstico se realiza, sobre todo, a través la exploración física y la valoración de los síntomas que presenta el paciente . Si existen dudas, se puede solicitar una analítica para detectar los anticuerpos (proteínas del sistema de defensa que reconocen al virus).
Factores desencadenantes del sarampión
Hay más riesgo de sarampión entre aquellas personas que no han sido vacunadas antes de entrar en las edades más propensas, además, las defensas bajas también pueden ser un desencadenante de la enfermedad . A continuación, vemos un listado de cuáles son los factores más potenciales para padecer el sarampión.
Factores de riesgo del sarampión
Bajo nivel socioeconómico .
Vivir en países con baja tasa de vacunación .
Padecer un estado de inmunodepresión (defensas bajas), por ejemplo, enfermos con virus de la inmunodeficiencia humana (VIH) o SIDA.
Edad menor a 2 años .
Complicaciones del sarampión
Aparición de una infección bacteriana secundaria como otitis media aguda o neumonía (infección en el pulmón)
Desarrollo de sarampión hemorrágica con sangrados nasales, orales e intestinales.
Meningoencefalitis: infección grave del cerebro y las membranas que lo recubren.
Neumonía de células gigantes (cuadros respiratorios graves poco frecuentes).
Complicaciones menos frecuentes son: la afectación del músculo cardíaco; la miocarditis o la disminución de las plaquetas o trombopenia.
Si la infección se produce en una mujer embarazada , hay una alta probabilidad de muerte fetal o aparición de malformaciones asociadas .
Prevención del sarampión
Vacunación infantil generalizada.
No estar en contacto con pacientes infectados.
Especialidades a las que pertenece el sarampión
El sarampión puede ser diagnosticado y tratado por el pediatra de atención primaria o el médico de familia . Si existen complicaciones es frecuente que se precise la hospitalización del paciente.
Preguntas frecuentes
¿Qué diferencia hay entre sarampión y varicela?
El sarampión y la varicela son dos enfermedades llamadas exantemáticas , que producen la aparición de “salpullido” en la piel, en el caso del sarampión son manchas rojas pequeñas que pueden confluir (unirse) y formar “manchas” de mayor tamaño. Después de tres o cuatro días desaparecen las “manchas” y aparece descamación de la piel. En el caso de la varicela aparecen lesiones más vesiculosas , (como ampollitas pequeñas), que se rompen y forman costras. Estas lesiones “conviven” en distinto estadio evolutivo.
En la varicela la sensación de picor aparece de manera más frecuente que en el sarampión. El periodo de contagio en el sarampión se da desde 10 días antes de la aparición de las lesiones y en la varicela es de dos días previos a la aparición de las lesiones hasta la formación de las costras . La fase prodrómica es de menor duración en la varicela.
Si he tenido la varicela… ¿Puedo tener el sarampión en el futuro?
Sí, porque son dos enfermedades originadas por dos virus diferentes .
Si me vacuno… ¿Quiere decir que ya no tendré el sarampión nunca?
Con solo la primera dosis, la vacuna evita la enfermedad durante el resto de la vida en más del 90 % de los pacientes.
¿A qué edad hay que ponerse la vacuna contra el sarampión?
En España, como en la mayoría de los países desarrollados, la vacuna forma parte del calendario de vacunación infantil : la primera dosis se recomienda entre los 12 y 15 meses de edad, aunque puede adelantarse la vacunación hasta los 6 meses si existen brotes epidémicos o si se va a realizar un viaje a zona de riesgo. La segunda dosis de vacuna es entre los 3 y los 6 años (se recomienda a los 3 – 4 años). Los lactantes vacunados antes de 1 año requerirán dos dosis adicionales más.
Si ya he tenido sarampión, ¿no lo tendré más?
Por lo general, el organismo de un paciente que padece la enfermedad se queda con un recuerdo inmunológico (en el sistema de defensa), sobre cómo reconocer al virus si toma contacto con él para poderlo eliminar. Solo podría volver a padecer Sarampión en caso de que el virus con el que toma contacto sufra una mutación (alteración de su estructura) muy importante, provocando que falle el reconocimiento del virus por parte del organismo.

Enfermedad
Síndrome Urémico Hemolítico
¿Qué es el síndrome urémico hemolítico?
El síndrome urémico hemolítico (SUH) es una enfermedad que se caracteriza por la presencia de manera simultánea de anemia hemolítica microangiopática (destrucción anormal de glóbulos rojos en su tránsito por la sangre), trombocitopeni (disminución de la cantidad de plaquetas en sangre e insuficiencia renal aguda). Los glóbulos rojos destruidos bloquean el sistema de filtración en los riñones, lo que puede provocar insuficiencia renal potencialmente mortal. Generalmente afecta a lactantes, niños entre 6 a 36 meses de edad y ancianos, se presenta frecuentemente después de una infección gastrointestinal. El síndrome urémico hemolítico es una enfermedad poco común y es grave . Sin embargo, si reciben un tratamiento adecuado a tiempo, la mayoría de las personas, especialmente los niños pequeños, se recuperan completamente .
Tipos de síndrome urémico hemolítico
El síndrome urémico se clasifica en:
Síndrome urémico hemolítico asociado a diarrea o típico: Esta forma es la causa más frecuente de SHU en niños (90%) y ocurre con un episodio previo de diarrea habitualmente con sangre , relacionado con la Escherichia coli (E. coli) productora de la toxina Shiga. El principal lugar de contagio son las guarderías e instituciones cerradas, por la transmisión de persona a persona. La ingestión de carne es la causa de brotes de origen alimentario. También son frecuentes por productos contaminados por los animales, como lechuga, coles, repollo, etc.
Síndrome hemolítico urémico no asociado a diarrea o atípico: Debido a alteraciones de factores de complemento , proteasas del factor de von Willebrand o alteraciones metabolismo de cobalamina que interviene en la adhesión y agregación plaquetaria y, dentro de este último grupo o de manera independiente, se incluye el SHU asociado a infecciones por streptococcus pneumoniae. La forma más común está asociado a la infección neumocócica debido a su mecanismo patogénico.
Causas del síndrome urémico hemolítico
El síndrome urémico hemolítico a menudo ocurre después de una infección gastrointestinal con la bacteria Escherichia coli, que hace referencia a un grupo de bacterias que normalmente se encuentran en los intestinos de seres humanos y animales sanos. La mayoría de los cientos de tipos de estas bacterias son normales e inofensivas. Pero algunas cepas específicas de Escherichia coli que generan una toxina llamada shiga, la cual inhibe la síntesis proteica, liberando el factor Von Willebrand, generando trombosis y destrucción eritrocitaria (glóbulos rojos). La ingestión de carne es la causa de brotes de origen alimentario. También son frecuentes por productos contaminados por los animales que, provocan infecciones alimentarias graves. La infección por dichas bacterias se propaga a través del contacto cercano con una persona infectada, por ejemplo, dentro de una familia o en un centro de cuidado de día o guardería infantil. Sin embargo, la afección también se ha asociado con otras infecciones gastrointestinales, como shigella y salmonella . También ha sido relacionada con infecciones que no son gastrointestinales. Otras causas pueden ser de forma hereditaria , déficit de complemento, algunas enfermedades como lupus eritematoso sistémico o tumores malignos. Aunque son causas menos frecuentes y raras.
Este síndrome es la primera causa de insuficiencia renal aguda en niños menos de 5 años. Puede causar la muerte o dejar secuelas de por vida como hipertensión arterial, insuficiencia renal crónica y alteraciones neurológicas.
Síntomas del síndrome urémico hemolítico
Los síntomas de este síndrome incluyen:
Diarrea con sangre. Dolor abdominal, vómitos y fiebre ocasional.
Disminución de la orina (oliguria), orina nula (anuria) y sangre en la orina (hematuria). Palidez. Fatiga e irritabilidad.
Pequeños hematomas sin explicación o sangrado por la nariz y la boca.
Presión arterial alta.
Confusión o convulsiones. Disminución del estado de conciencia.
Inflamación del rostro, las manos, los pies y todo el cuerpo.
Erupción cutánea que luce como pequeños puntos rojos. Entre otros síntomas.
Tratamiento para el síndrome urémico hemolítico
Las opciones de tratamiento del síndrome urémico hemolítico incluyen:
La reposición de líquidos y electrolitos perdidos (fluidoterapia), está debe realizarse con cuidado, ya que los riñones no eliminan los líquidos y los residuos con la misma eficacia que la habitual.
La transfusión de glóbulos rojos por vía intravenosa puede ayudar a revertir los signos y síntomas del síndrome urémico hemolítico, que incluyen escalofríos, fatiga, dificultad para respirar, frecuencia cardíaca acelerada, color amarillento de la piel y orina de color oscuro. Si se forman hematomas o sangrado con facilidad, la transfusión de plaquetas por vía intravenosa puede ayudar a que la sangre coagule con más normalidad.
A veces, se necesita realizar diálisis para filtrar los residuos y el exceso de líquido de la sangre (hemodiálisis). La diálisis suele ser un tratamiento provisorio que se administra hasta que los riñones vuelvan a funcionar bien, en niños la más utilizada es la diálisis peritoneal .
Pruebas complementarias del tratamiento del síndrome urémico hemolítico
Para el diagnóstico y tratamiento del síndrome urémico hemolítico se realizan pruebas como:
Análisis de sangre estos análisis pueden determinar si los glóbulos rojos están dañados.
Análisis de orina , para detectar niveles anormales de proteínas, sangre y signos de infección en la orina.
Muestra de materia fecal , para detectar Escherichia coli productora de toxinas y otras bacterias que pueden causar el síndrome urémico hemolítico.
Factores desencadenantes del síndrome urémico hemolítico
No se conoce un factor desencadenante principal para el síndrome urémico hemolítico.
Factores de riesgo del síndrome urémico hemolítico
Entre los factores que aumentan el riesgo de tener el síndrome urémico hemolítico incluyen: niños menores de 5 años . Personas mayores de más de 75 años . Personas con determinados cambios genéticos que los hacen más propensos.
Complicaciones del síndrome urémico hemolítico
Las complicaciones incluyen:
Insuficiencia renal.
Coma.
Presión arterial alta.
Accidente cerebrovascular.
Problemas cardíacos.
Problemas intestinales.
Alteraciones neurológicas.
Prevención del síndrome urémico hemolítico
Para prevenir este síndrome es necesario :
Asegurar la correcta cocción de la carne : la bacteria se destruye a los 70 °C. Esto se consigue cuando la carne tiene una cocción homogénea. Prestar especial atención al interior de preparados con carne picada.
Evitar el contacto de las carnes crudas con otros alimentos.
No consumir zumos de fruta no pasteurizados.
Lavar cuidadosamente verduras y frutas.
Asegurar la correcta higiene de las manos (deben lavarse con agua y jabón) antes de preparar los alimentos. y luego de utilizar el baño.
Especialidades a las que pertenece el síndrome urémico hemolítico
Este síndrome pertenece a las especialidades de gastroenterología y pediatría . La gastroenterología es de la medicina que se ocupa del estómago y los intestinos y sus enfermedades, así como del resto de los órganos del aparato digestivo. La pediatría es la parte de la medicina que se ocupa del estudio del crecimiento y el desarrollo de los niños hasta la adolescencia, así como del tratamiento de sus enfermedades.
Preguntas frecuentes
¿Cómo se transmite la enfermedad del síndrome urémico hemolítico?
Se propaga a través del contacto cercano con una persona infectada, por ejemplo, dentro de una familia o en un centro de cuidado de día o guardería.
¿A quién afecta el síndrome urémico hemolítico?
Afecta a personas de todas las edades . Pero mayormente a niños de entre 6 a 36 meses de edad.
¿Qué es el síndrome urémico hemolítico atípico?
Es una enfermedad crónica y potencialmente mortal que afecta fundamentalmente al riñón, en la que una deficiencia genética, debido a alteraciones de factores de complemento, proteasas del factor de Von Willebrand o alteraciones metabolismo de cobalamina que interviene en la adhesión y agregación plaquetaria y, dentro de este último grupo o de manera independiente, se incluye el SHU asociado a infecciones por streptococcus pneumoniae . La forma más común está asociado a la infección neumocócica debido a su mecanismo patogénico.

Enfermedad
Sinovitis
¿Qué es la sinovitis?
La sinovitis es la inflamación de la membrana sinovial , localizada en la parte interior de la cápsula articular, recubrimiento de las superficies articulares que engloba a modo de bolsa entre los huesos que se articulan, un líquido lubrificante llamado líquido sinovial . La alteración de esta membrana puede producir por parte de las células que la forman la sobreproducción de forma anómala de líquido sinovial que aumenta la presión en la articulación. Puede aparecer asociada a la presencia de otro tipo de enfermedades inflamatorias en las articulaciones, como la artritis reumatoide. Otras veces aparece como entidad propia, como la que se da frecuentemente en los niños en la cadera (sinovitis transitoria de la cadera). Es una alteración de gravedad moderada, dependiendo de la zona donde aparezca, el contexto clínico y la edad del paciente. Produce dolor e impotencia funcional hasta su resolución.
Tipos de sinovitis
Según el tiempo de evolución de la afectación sinovial , la sinovitis se puede dividir en aguda , de aparición más o menos brusca y corto periodo de evolución , subaguda , aquella que no da claros síntomas en la exploración, pero produce una incomodidad constante al paciente , o crónica , cuando por el proceso inflamatorio se producen lesiones permanentes en la membrana sinovial y el dolor y la incapacidad funcional más o menos presente, es constante.
Dependiendo de las características anatomopatológicas , de localización o causa se describe:
Sinovitis bursal : asociada a bursitis .
Sinovitis dendrítica : en la que aparecen vellosidades (pequeños “pliegues” a modo de pelos) en la superficie interna de la membrana hacia el saco (bolsa) sinovial.
Sinovitis fungosa : la que aparece cuando existe una infección por tuberculosis .
Sinovitis plásica : sinovitis en la que aparecen adherencias (uniones anómalas) de la membrana sinovial.
Sinovitis purulenta : asociada a la aparición de ciertas infecciones como fiebre tifoidea, escarlatina…etc, y en la cual aparece pus dentro de la bolsa sinovial.
Sinovitis seca : la que aparece asociada a otros procesos como reumatismos agudos, sífilis…etc, en la que no hay gran producción de líquidos sinoviales.
Sinovitis tendinosa : aquella asociada a la inflamación de un tendón .
Sinovitis transitoria alteración de la bolsa sinovial que aparece frecuentemente en niños y de la cual se desconoce la causa.
Sinovitis hemofílica crónica : aquella que aparece en pacientes con hemofilia asociada a sangrado intraarticulares.
Síndrome de sinovitis, acné, pustulosis, hiperostosis, osteítis (SAPHO) : en la que aparece también una afectación sinovial inflamatoria . Es una enfermedad rara de origen desconocido.
Sinovitis villonodular pigmentada focal : enfermedad benigna en la que aparece un engrosamiento de la membrana sinovial que puede llegar a formar pequeños nódulos .
Causas de la sinovitis
Las posibles causas de la producción de una sinovitis son los traumatismos en las articulaciones, la infecciones, el padecimiento de enfermedades degenerativas como la artrosis o de enfermedades reumáticas autoinmunes como la artritis reumatoide, o por depósitos de sustancia como en el caso de la gota. Otras sinovitis son de causa desconocida .
Síntomas de la sinovitis
La presentación puede variar según el tipo de sinovitis y el contexto clínico, pero por lo general aparece dolor , aumento de temperatura de la articulación , deformidad por aumento de líquido sinovial que puede llegar a salirse fuera de la membrana sinovial, y presencia de impotencia funcional (dificultad para el movimiento de la articulación).
Tratamiento para la sinovitis
El tratamiento fundamental para la sinovitis es el reposo , aplicación de frío local y toma de fármacos antiinflamatorios. Además, se pueden asociar otro tipo de medicamentos según la articulación en la que aparezca la sinovitis. En casos de sinovitis resistentes pueden utilizarse infiltraciones directas de corticoides en la articulación . En algunos casos es preciso hacer una intervención quirúrgica mínimamente invasiva con la realización de una artroscopia (introducción por pequeñas incisiones de una cámara y utensilios para poder tratar).
Pruebas complementarias del tratamiento de la sinovitis
El diagnóstico en muchos de los procedimientos en los que aparece la sinovitis debe basarse inicialmente en la exploración física y la entrevista clínica . Además, es posible que se precise de la realización de pruebas de imagen como radiografías o resonancias magnéticas nucleares o determinadas analíticas de sangre para valorar aspectos de la inflamación, infecciones (serologías), sustancias de depósito como ácido úrico, inmunodeficiencia…etc. En otras ocasiones se realiza una punción con una jeringa para realizar una extracción del líquido sinovial y realizar su análisis en laboratorio. Por último, en algunos procesos se precisa realizar una artroscopia de forma diagnóstica para ver de forma directa la alteración de la articulación.
Factores de riesgo y/o desencadenantes de la sinovitis
Sobrecarga de las articulaciones con movimientos repetitivos.
Contagio de enfermedades bacterianas.
Influencia genética para el desarrollo de enfermedades autoinmunes que afectan a las articulaciones.
Edad.
Realización de ejercicios con sobrecarga y aumento del peso que deben soportar las articulaciones.
Alimentación rica en purinas (mariscos, carne roja, tomate…etc.) que pueden aumentar el ácido úrico y con ello el riesgo de padecer gota.
Complicaciones de la sinovitis
Incapacidad funcional permanente producida por la sinovitis crónica en la que puede producirse una afectación de los cartílagos articulares.
Prevención de la sinovitis
Realizar ejercicios con adecuada protección articular.
Evitar traumatismos repetidos en ejercicios y deportes.
Prevención de infecciones con adecuada higiene.
Revisiones de salud establecidas y consulta temprana de síntomas dolorosos.
Especialidades a las que pertenece la sinovitis
La sinovitis es una alteración que puede diagnosticarse y tratarse por el especialista en traumatología o reumatología según el proceso donde aparezca.
Preguntas frecuentes
¿Qué es el engrosamiento sinovial?
El engrosamiento sinovial es un aumento patológico del grosor de la membrana sinovial que recubre a los huesos en las articulaciones.
¿Qué es la sinovitis aguda?
La sinovitis aguda es la aparición de una sinovitis de manera más o menos brusca y con un corto periodo de evolución .
¿Qué diferencia hay entre sinovitis y tenosinovitis?
La sinovitis es la inflamación de la membrana sinovial de las articulaciones. La tenosinovitis es la inflamación de la vaina que recubre a determinados tendones localizados en la muñecas-manos o en el tobillo-pie.
¿Qué es la enfermedad de Perthes?
La enfermedad de Perthes es una muerte del tejido óseo por interrupción del aporte de sangre a la parte del fémur que forma parte de la cadera (su parte más alta), cuya causa se desconoce.
¿Cuál es la sinovitis más frecuente?
La sinovitis transitoria es la causa más frecuente de sinovitis en la edad infantil y la sinovitis artrósica una de las entidades más frecuentes en edad adulta.
Enfermedad
Mastoiditis
¿Qué es la mastoiditis?
La mastoiditis es una in flamación o infección de la apófisis mastoidea o del hueso mastoideo , que es una parte del hueso temporal del cráneo, que se encuentra situado detrás del oído. El hueso mastoideo está compuesto por celdas que drenan el oído medio.
La mastoiditis es generalmente una complicación de una otitis media aguda, donde el hueso se llena de material purulento que puede llegar a destruir su estructura en panal. Es más frecuente en niños entre 2 y 5 años . Antes de la época de los antibióticos, era una de las causas principales de muerte infantil.
En la actualidad es una enfermedad poco común y mucho menos peligrosa, ya que la otitis media se trata muy bien con los antibióticos y no da lugar a que se complique con una mastoiditis, por lo que puede ser una infección leve.
Tipos de mastoiditis
Existen tres estadios en su evolución:
Mastoiditis simple: definida como inflamación de la mucosa, aparece en la mayoría de las otitis media aguda, no se acompaña de signos inflamatorios retroauriculares y no debe considerarse una complicación de la otitis media.
Mastoiditis con afectación al hueso (perióstica): por propagación venosa de la infección del oído medio suele acompañarse de signos inflamatorios retroauriculares característicos, sobre todo a la percusión y palpación del hueso.
Mastoiditis con osteítis: se considera la forma más grave y evolucionada. En este caso se produce la destrucción del hueso trabecular de las celdillas mastoideas con el riesgo de formación de un absceso subperióstico.
Causas de mastoiditis
Las causas de las mastoiditis es una infección del oído medio (otitis media aguda), que generalmente se produce por diferentes bacterias. Esto ocurre cuando la infección del oído medio se propaga hacia el hueso mastoideo. Normalmente una persona con mastoiditis tiene antecedentes de infección de oído recientes o sufre infecciones reiteradas del oído medio. La mayoría de las infecciones mastoideas son causadas por bacterias neumocócicas.
Síntomas de mastoiditis
Los síntomas de la mastoiditis incluyen:
Dolor, enrojecimiento o inflamación detrás de la oreja.
Secreción del oído.
El lóbulo de la oreja sobresale hacia afuera debido a la inflamación del hueso mastoideo. Fiebre, que puede ser alta o incrementarse súbitamente.
Dolor de cabeza.
Irritabilidad o nerviosismo.
Pérdida de audición.
Dolor a la palpación y percusión del hueso.
Borramiento del surco retroauricular.
Desplazamiento del pabellón auricular hacia delante y abajo. Entre otros síntomas.
Tratamiento para la mastoiditis
El tratamiento dependerá de los síntomas, la edad y la salud general del paciente. También variará según la gravedad de la afección. En ocasiones, la afección requiere un tratamiento repetitivo o prolongado. A la mayoría de las personas se les administra inmediatamente un antibiótico por vía intravenosa.
En cambio, a las personas que no estén gravemente enfermas puede administrarse un antibiótico por vía oral durante un periodo de 10-14 días, y administrar analgésico y/o antinflamatorios no esteroideos para el dolor y tratar la fiebre, con una hidratación adecuada. Sin embargo, a veces es necesario recurrir a una cirugía para ayudar a drenar el líquido del oído medio.
En la mayoría de los casos se puede sugerir una miringotomía , procedimiento quirúrgico que consiste en realizar una pequeña abertura en el tímpano para drenar el líquido y aliviar la presión del oído medio. Se coloca un pequeño tubo en la abertura del tímpano para ventilar el oído medio e impedir la acumulación de líquido. Una vez que se drena el líquido, se recupera la audición. Los tubos normalmente se caen por sí solos entre seis y doce meses después de su colocación.
Pruebas complementarias del tratamiento de mastoiditis
Para el diagnóstico y tratamiento de la mastoiditis es necesario realizar pruebas como:
Radiografía de la apófisis mastoidea , en general esta prueba ofrece poca información. Tomografía computarizada del oído,
Tomografía computarizada de la cabeza,
Análisis de sangre , un cultivo del oído infectado, entre otras pruebas.
Factores desencadenantes de mastoiditis
La mastoiditis se desencadena a partir de una infección del oído medio (otitis media aguda).
Factores de riesgo de mastoiditis
Los factores de riesgo de la mastoiditis incluyen : la edad , los niños de 2-5 años son los más propensos a tener este trastorno. La coalescencia , que es una infección persistente aguda en la cavidad mastoidea puede conducir a una osteítis rarificada, que destruye las células que forman trabéculas óseas. Otitis media aguda recurrente. Colesteatoma que es un crecimiento anormal de la piel del oído medio, detrás de la membrana del tímpano. Entre otros factores.
Complicaciones de la mastoiditis
Las complicaciones de la mastoiditis incluyen:
Pérdida de la audición.
Infección grave en tejidos cercanos.
Destrucción del hueso mastoideo.
Parálisis facial (complicaciones intracraneales).
Meningitis.
Problemas en el oído interno.
Absceso en mastoide y tortícolis
Daños en los nervios de la cara.
Mastoiditis crónica.
Osteomielitis del temporal.
Prevención de la mastoiditis
La mejor forma de prevenir la mastoiditis es tratar la infección del oído antes de que se extienda al hueso mastoideo.
Especialidades a las que pertenece la mastoiditis
La mastoiditis pertenece a la especialidad de otorrinolaringología, que es la parte de la medicina que se ocupa del tratamiento y diagnóstico de las enfermedades de la nariz, oído, y boca.
Preguntas frecuentes:
¿Dónde se encuentra la apófisis mastoides?
La apófisis mastoides se localiza en la parte posteroinferior del hueso temporal en el cráneo. El hueso temporal es un hueso par del cráneo y tiene forma irregular.
¿Qué es un colesteatoma de oído?
Es un crecimiento anormal de piel del oído medio detrás de la membrana del tímpano.
¿Qué es el hueso mastoides?
Es un hueso prominente situado justamente detrás del oído, está compuesto por celdillas neumáticas que drenan el oído medio.
¿A quién afecta la mastoiditis?
La mastoiditis afecta en la mayoría de los casos a niños entre los 2 y los 5 años.
¿Cómo se forma el arco cigomático?
El arco cigomático se forma en la unión de la apófisis cigomática del hueso temporal y el hueso cigomático o malar.

Enfermedad
Mononucleosis
¿Qué es la mononucleosis?
La mononucleosis o enfermedad del beso es una enfermedad infecciosa de origen vírico, producida por el virus de Epstein-Barr. La mayor incidencia es en adolescentes, y alrededor del 95% de los adultos de entre 35 y 40 años han sido infectados. El virus se transmite a través de la saliva , puede precisar asistencia de urgencia si se da un gran aumento del bazo o se presenta el síndrome de Guillain Barré. Es una enfermedad de tipo leve.
Tipos de mononucleosis
La mononucleosis es una enfermedad infecciosa que puede presentarse en forma poco sintomática en niños, o bien presentar más síntomas, pero esto es más típico de adultos. No existen distintos tipos de mononucleosis, solo diferencia de gravedad en los síntomas.
Causas de la mononucleosis
La mononucleosis tiene como causa la infección por el virus de Epstein Barr. Este virus se contagia por contacto con saliva de un paciente infectado.
Síntomas de la mononucleosis
Los síntomas de la mononucleosis son: fiebre, malestar general, dolor muscular, amígdalas aumentadas de tamaño con secreciones pegadas a las mismas, adenopatías cervicales y aumento del bazo.
Tratamiento para la mononucleosis
La mononucleosis no tiene tratamiento para la infección, será necesario tratamiento sintomático con analgésicos, reposo y líquidos abundantes , así como evitar los deportes de contacto.
Pruebas complementarias del tratamiento de la mononucleosis
Se harán analíticas de sangre en las que se busca presencia de glóbulos blancos más altos de lo normal, con presencia de linfocitos atípicos, anticuerpo frente al virus de Epstein Barr.
Factores desencadenantes de la mononucleosis
El factor desencadenante es la infección con virus de Epstein Barr.
Factores de riesgo de la mononucleosis
El factor de riesgo central de la mononucleosis es el contacto con saliva de pacientes enfermos , ya sea mediante besos o por contacto con vasos o cubiertos de la persona enferma.
Complicaciones de la mononucleosis
Síndrome de Guillain Barré.
Convulsiones.
Anemia.
Hepatitis con ictericia.
Aumento y rotura del bazo.
Erupción cutánea.
Prevención de la mononucleosis
No compartir vasos o cubiertos de personas enfermas.
No besar a personas enfermas.
Especialidades a las que pertenece la mononucleosis
El especialista que controla la mononucleosis es el médico de familia, pero en caso de complicaciones, puede ser necesario el control por un médico de medicina interna o de la especialidad de neurología.
Preguntas frecuentes:
¿Cómo se contagia la mononucleosis?
La mononucleosis se contagia a través del contacto con saliva de las personas infectadas, ya sea por besos o por compartir vasos o cubiertos. En casos excepcionales se puede contagiar por trasplante de médula ósea.
¿Por qué se inflama el bazo?
En la mononucleosis se produce una esplenomegalia inmune, esto se da como reacción a la infección por el virus de Epstein-Barr.
¿Cuál es la función del bazo?
El bazo tiene un a función inmunológica, produciendo sustancias que tratan de dañar a las bacterias y virus infecciosos, pero también actúa como sistema de filtro de la sangre eliminando células sanguíneas anormales, o aquellas que se deben eliminar por su envejecimiento.
¿Qué es la esplenomegalia?
La esplenomegalia es aumento del tamaño del bazo por encima de lo normal, eso se puede producir por enfermedades infecciosas como la mononucleosis, o inflamatorias, como la artritis reumatoide.
¿Cómo se llama la operación del bazo?
La operación del bazo se conoce como esplenectomía , y en ella se procede a retirar el bazo. Puede ser consecuencia de un traumatismo en el cual se rompe, siendo necesaria su extirpación para controlar el sangrado, o bien en casos de secuestro de células sanguíneas, en el cual el bazo procede a mantener en su interior células como las plaquetas, alterando la función de ellas y siendo necesario extirparlo. La esplenectomía no lleva consigo más riesgos que el poder tener más infecciones, por ello, tras la esplenectomía, le recomiendan al paciente que se vacuna de neumonía y gripe.
Enfermedad
Neurofibromatosis
¿Qué es la neurofibromatosis?
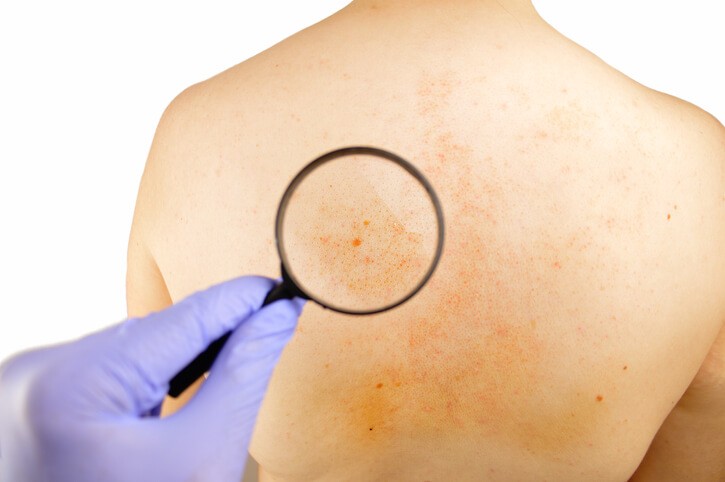
La neurofibromatosis es un conjunto de trastornos genéticos neurocutáneos (con manifestaciones neurológicas y cutáneas), que afecta la manera en que las células crecen y se forman, lo que hace que se formen tumores en el tejido del nervio. Estos tumores pueden desarrollarse en cualquier lugar del sistema nervioso, ya sea el cerebro, la médula espinal, o los nervios, y también en tejido no nervioso como huesos y piel. En general, los tumores son mayormente benignos (no cancerosos), pero a veces pueden convertirse en cáncer (malignos). Estos tumores pueden crecer en cualquier lugar del interior o de la superficie del organismo. Son enfermedades multisistémicas progresivas, hereditarias, raras o poco comunes. Puede desarrollarse en todo el mundo y no existen diferencias de sexo o de grupo racial. La neurofibromatosis se puede heredar de los padres o puede ocurrir por una mutación (cambio) en los genes.
Tipos de neurofibromatosis
Existen 3 tipos de neurofibromatosis, estos son:
Neurofibromatosis tipo 1: también conocida como enfermedad de Von Recklinghausen. Es el tipo de neurofibromatosis más común, aparece en la infancia y está causada por una anomalía en un gen en el cromosoma 17. Los signos suelen ser evidentes en el momento del nacimiento o poco después, y casi siempre antes de los 10 años. Estos son: manchas cutáneas sin relieve de color marrón claro o de color café con leche, pequeños bultos en el iris del ojo, los cuales son nódulos inofensivos no se pueden ver fácilmente y no afectan la visión, bultos suaves sobre la piel o debajo de ella o deformidades óseas, entre otros.
Neurofibromatosis tipo 2: también se denomina neurofibromatosis acústica bilateral. Es mucho menos frecuente que la neurofibromatosis tipo 1. Causada por una mutación en un gen localizado en el cromosoma 22, se presenta típicamente en la adolescencia o en la adultez temprana. Los signos y síntomas de la neurofibromatosis tipo 2 aparecen, por lo general, como resultado del desarrollo de tumores benignos que crecen lentamente (neurinoma del acústico) en los dos oídos.
Schwannomatosis: es un tipo bastante raro de neurofibromatosis, normalmente, afecta a las personas después de los 20 años. La schwannomatosis provoca la formación de tumores en los nervios del cuero cabelludo (craneales), espinales y periféricos, pero no en el nervio que transporta la información de sonido y equilibrio desde el oído interno hasta el cerebro.
Causas de la neurofibromatosis
La neurofibromatosis se produce por d efectos genéticos (mutaciones) que transmiten los padres , o se producen espontáneamente en la concepción. En la neurofibromatosis tipo 1, el cromosoma alterado es el 17, mientras que el cromosoma 22 es el responsable de la neurofibromatosis de tipo 2.
Síntomas de la neurofibromatosis
Los síntomas de la neurofibromatosis incluyen: manchas cutáneas sin relieve de color marrón claro, pecas en la zona de las axilas y la ingle, pequeños bultos en el iris del ojo (nódulos de Lisch), bultos suaves sobre la piel o debajo de ella , deformidades óseas, tamaño de la cabeza superior al promedio, pérdida de la audición gradual, zumbido en los oídos, equilibrio deficiente, dolores de cabeza, entumecimiento o debilidad en diversas partes del cuerpo y pérdida muscular.
Tratamiento para la neurofibromatosis
La neurofibromatosis no tiene cura, pero los signos y síntomas se pueden tratar. El tratamiento médico puede incluir: cirugía para quitar los tumores que causan dolor u otros problemas. Cuando la cirugía no es posible, se aconseja hacer seguimiento continuo y control del dolor.
Otras opciones de tratamiento son la radiación o quimioterapia para los tumores que se convierten en cáncer o que causan otros problemas, colocación de audífonos o implante auditivo de tronco encefálico para adolescentes y adultos que tienen neurofibromatosis tipo 2 con pérdida auditiva, y a quienes se les quitó parte del nervio auditivo.
Pruebas complementarias del tratamiento de la neurofibromatosis
Para el diagnóstico y tratamiento de la neurofibromatosis se necesitan pruebas como: examen ocular, examen de oído, radiografías, tomografías computarizadas y resonancias magnéticas , que pueden ayudar a identificar anomalías óseas, tumores en el cerebro y la médula espinal, y tumores muy pequeños. También se pueden realizar análisis genéticos entre otras pruebas.
Factores de riesgo de la neurofibromatosis
El factor de riesgo más importante de la neurofibromatosis es tener antecedentes familiares del trastorno. Aproximadamente la mitad de las personas con neurofibromatosis tipo 1 y tipo 2 heredaron la enfermedad. Cuando la neurofibromatosis tipo 1 y la neurofibromatosis tipo 2 no son heredadas, ocurren por nuevas mutaciones genéticas.
El patrón hereditario en el caso de la Schwannomatosis no es tan claro. Actualmente, los investigadores calculan que el riesgo de heredar Schwannomatosis de un padre afectado es de alrededor del 15%.
Complicaciones de la neurofibromatosis
Las complicaciones de la neurofibromatosis incluyen:
Problemas neurológicos.
Problemas respiratorios.
Cáncer.
Sordera parcial o total.
Lesión al nervio facial.
Múltiples tumores cerebrales benignos o tumores de la columna vertebral que requieren cirugías frecuentes.
Debilidad o entumecimiento en las extremidades.
Prevención de la neurofibromatosis
No se conocen formas específicas de prevenir esta afección, pero sí se recomiendan ciertos consejos genéticos a las personas con antecedentes familiares de este trastorno.
Especialidades a las que pertenece la neurofibromatosis
Las especialidades que afectan la neurofibromatosis forman un equipo multidisciplinar, ya que esta puede desarrollarse en diferentes partes del cuerpo. Estas son: neurología, neurocirugía, dermatología, genética, oftalmología, ortopedia, psicología y rehabilitación.
Preguntas frecuentes:
¿Cómo se hereda la neurofibromatosis?
La neurofibromatosis se hereda de forma autosómica dominante . Es decir, que, para tener la enfermedad, se necesita solo un cambio (mutación) en una copia del gen responsable de cada célula. Una persona afectada hereda la mutación de un padre afectado. Lo que quiere decir que se hereda de padres a hijos.
¿A qué cromosoma afecta la neurofibromatosis?
En la neurofibromatosis tipo 1, el cromosoma alterado es el 17, mientras que el cromosoma 22 es el responsable de la neurofibromatosis de tipo 2.
¿Qué son los nódulos de Lynch?
Los nódulos de Lynch son pequeños bultos en el iris del ojo . Estos nódulos inofensivos no se pueden ver fácilmente y no afectan la visión.
¿Qué es la esclerosis tuberosa?
La esclerosis tuberosa es un trastorno genético poco frecuente que hace que se formen tumores no cancerosos o benignos con crecimientos excesivos e imprevistos de tejido normal en muchas partes del cuerpo.
¿Qué es la enfermedad de Von Hippel Lindau?
La enfermedad de Von Hippel-Lindau (VHL) es una enfermedad rara que causa tumores y quistes en el cuerpo . Pueden crecer en el cerebro y en la médula espinal, en los riñones, en el páncreas, en las glándulas suprarrenales y en el tracto reproductivo. En general, los tumores son benignos o no cancerosos.

Enfermedad
Hipoglucemia
¿Qué es la hipoglucemia?
La hipoglucemia es una bajada de la cantidad de azúcar en la sangre por debajo de 60 mg/ml. En los recién nacidos son más frecuentes en los niños pretérmino, llegando a ser hasta del 14% de los casos. En los niños a término suele darse como mucho en un 7%. Las hipoglucemias en los diabéticos son más frecuentes en pacientes con insulina o secretagogos que con otros tratamientos hipoglucemiantes. Es una situación urgente de revertir ya que es grave porque puede poner en peligro la vida del individuo.
Causas de la hipoglucemia
La causa principal de la hipoglucemia es la alteración hormonal a nivel de hipófisis y tiroides . También se puede producir en pacientes normales sin alteraciones hormonales por causa de falta de alimento, exceso de ejercicio , o descarga insulínica en el páncreas.
Síntomas de la hipoglucemia
Los síntomas son: malestar, cansancio, adormecimiento, temblor, sudoración profusa, palpitaciones, mareos, visión borrosa, dolor de cabeza, convulsiones y trastorno del comportamiento.
Tratamiento para la hipoglucemia
El tratamiento para la hipoglucemia es dar azúcar de forma rápida. Se puede dar un producto azucarado como pueden ser los zumos de frutas , o también se puede dar directamente un sobre de azúcar disuelto en un vaso de agua. En casos muy difíciles de revertir y en pacientes diabéticos, puede ser necesario darles Glucagón mediante inyección subcutánea.
Pruebas complementarias del tratamiento de la hipoglucemia
La prueba complementaria será la determinación de glucosa en sangre capilar, hasta normalización de la misma, cada media hora.
Factores desencadenantes de la hipoglucemia
Los factores desencadenantes de la hipoglucemia son la falta de aporte de hidratos de carbono en la dieta , o el exceso de insulina en la sangre.
Factores de riesgo de la hipoglucemia
Son factores de riesgo para sufrir hipoglucemia en los pacientes en tratamiento con insulina y con secretagogos como Repaglinida y Glibenclamida . Los largos periodos de ayuno sin ingesta de hidratos de carbono , el periodo neonatal en niños pretérmino que tienen más problemas en regular hormonalmente sus niveles de glucemia, y también en niños a término en especial si son hijos de madres diabéticas.
Complicaciones de la hipoglucemia
Daños neurológicos.
Convulsiones.
Pérdida de conocimiento.
Coma.
Prevención de la hipoglucemia
No realizar ejercicio en ayunas.
Ingesta adecuada de hidratos de carbono.
Control capilar de glucemia.
Especialidades a las que pertenece la hipoglucemia
En el caso de hipoglucemias neonatales se trata de control con pediatras neonatólogos, en el resto de casos, se controla por el endocrino.
Preguntas frecuentes:
¿Qué es la hipoglucemia en bebés?
La hipoglucemia en bebés es la bajada de azúcar que se puede producir en los recién nacidos, más frecuente en niños prematuros, en niños nacidos a término que presentan madres diabéticas en el embarazo, y en niños con retraso en el crecimiento intrauterino.
¿Qué puede ocasionar la hipoglucemia?
Las hipoglucemias se producen por el exceso de insulina o por la falta de hidratos de carbono. En personas con tratamiento con insulina o fármacos secretagogos (fármacos que producen la secreción de insulina), se pueden producir hipoglucemias. En los neonatos que no tienen aún una buena regulación hormonal también se produce por parte del organismo un exceso de insulina que es la que causa la hipoglucemia. Las personas que tienen largos periodos de ayuno pueden presentar una hipoglucemia por falta de ingesta.
¿Qué diferencia hay entre hiperglucemia e hipoglucemia?
Las hiperglucemias son valores por encima de lo normal de azúcar en sangre (son niveles normales entre 70 y 129 mg/dl). La hipoglucemia son valores por debajo de lo normal de azúcar en sangre . Para tener síntomas de hipoglucemia, la glucosa deberá de estar por debajo de 60 mg/dl.
¿Cuáles son los niveles normales de azúcar en sangre?
Los niveles normales de azúcar en sangre son diferentes antes y después de la ingesta, así, en ayunas se consideran normales niveles de entre 70 y 128 mg/ml, por encima de estas cifras se habla de hiperglucemia, cuando se ha consumido alimento se considera que a las dos horas de haberlo ingerido los niveles de azúcar deben estar por debajo de 140 mg/ml
¿Qué es la hipoglucemia reactiva?
La hipoglucemia reactiva o hipoglucemia postprandial es la que se produce unas cuatro horas después de comer y no necesita un tratamiento especial, salvo el regular la ingesta de alimentos. Suele ser suficiente con no comer alimentos azucarados con el estómago vacío y hacer cinco comidas al dia.

Enfermedad
Ictericia
¿Qué es la ictericia?
La ictericia es la aparición de coloración amarillenta de la piel, las mucosas (revestimientos de los orificios corporales) y la conjuntiva ocular (el blanco de los ojos se vuelve amarillento). Es un síntoma que aparece por un aumento en el torrente sanguíneo de la bilirrubina más de 2.25 mg/dL, una sustancia producida por la degradación de los glóbulos rojos en el bazo , apareciendo la bilirrubina indirecta o no conjugada, y metabolizada en el hígado, dándose la bilirrubina directa o conjugada, que puede aumentar su concentración en el organismo por varias vías y distintas patologías.
Su frecuencia de aparición varía según la patología de base que produzca el aumento de la bilirrubina, siendo un síntoma frecuente, por ejemplo, en el caso de la llamada ictericia fisiológica del recién nacido. Las patologías en el adulto que más frecuentemente desencadenan la ictericia, son aquellas que producen lesión en las células hepáticas (hepatitis y cirrosis).
Aunque existen patologías con buen pronóstico que hacen que aumente la bilirrubina en sangre de forma reversible con tratamiento, en otras ocasiones la presencia de ictericia puede ser un signo del padecimiento de una enfermedad grave.
Tipos y causas de ictericia
La ictericia se produce por diferentes tipos de mecanismos por los que aumenta la bilirrubina en el cuerpo:
Por aumento de su formación.
Por disminución de su depuración hepática.
Por obstrucción al flujo biliar.
Aumento de la bilirrubina indirecta o no conjugada con función hepática normal :
Cuando hay una destrucción de glóbulos rojos (hemólisis).
Cuando hay una destrucción de glóbulos rojos alterados en la médula ósea (eritropoyesis ineficaz).
Cuando se realizan transfusiones al paciente o por la reabsorción de grandes cantidades de sangre que se sale de los vasos sanguíneos en hematomas o infartos en los tejidos.
En la ictericia fisiológica del recién nacido: por una falta de maduración de la enzima que transforma la estructura de la bilirrubina.
Por la enfermedad de Cliger-Najar: debida a alteraciones genéticas que producen un déficit de la enzima que transforma la bilirrubina en el hígado.
Por la enfermedad de Gilbert: déficit parcial de la enzima que se transmite genéticamente.
Por incremento de la producción de bilirrubina : se puede dar en varias situaciones:
Por déficit en el transporte de la bilirrubina en la sangre y su captación por el hígado : el aumento lo pueden producir algunos fármacos ( Rifampicina, Ciclosporina, Indinavir, Probenecid… ), también puede producirse por enfermedades como la sepsis o la insuficiencia cardíaca.
Por alteraciones en la conjugación de la bilirrubina : modificación de su estructura en el hígado para ser excretada después por la vesícula biliar. Esta alteración aparece en las siguiente situaciones:
Aumento de bilirrubina directa o conjugada con función hepática normal : se produce por dos enfermedades raras hereditarias:
Enfermedad de Dubin-Johnson.
Enfermedad de Rotor: en la que se produce una alteración de la excreción de la bilirrubina a los conductos biliares.
Aumento de la bilirrubina directa o mixta (directa e indirecta), con alteraciones de la función del hígado :
Por fracaso global de la función hepática que aparece en enfermedades como hepatitis, “hígado graso” (esteatosis hepática), toma de fármacos, alcohol, cirrosis, alteraciones del tiroides…etc.
Por bloqueo del paso de la bilis al duodeno: cuando existe un obstáculo en el tejido del hígado, lo que puede producirse en enfermedades como infección de Epstein Barr, sarcoidosis, tuberculosis, linfoma y/o colangitis biliar primaria, o por obstrucción de la vía biliar en el trayecto que pasa fuera del hígado, lo que se produce en enfermedades como coledocolitiasis, quistes, y enfermedades tumorales de la vía biliar, entre otras.
Síntomas de la ictericia
El signo fundamental de la ictericia es la aparición de una coloración amarillo-verdosa y naranja u ocre en la piel , que es apreciable en la conjuntiva ocular cuando la bilirrubina en sangre aumenta a partir de 2 mg/dl, y en la piel a partir de 3 mg/dl.
Además, este signo puede acompañarse de un conjunto de síntomas variados dependiendo de la causa del aumento de la bilirrubina: picor, cambio de la coloración de las heces (heces blancas o claras), aumento de la coloración de la orina , fiebre, dolores articulares y musculares, falta de apetito, pérdida de peso, dolor abdominal…etc.
Tratamiento para la ictericia
El tratamiento fundamental es el específico de la causa que ha originado el aumento de la bilirrubina y con ello la ictericia. En caso de patologías graves se debe ingresar al paciente (en casos de fallo hepático agudo grave, colecistitis, colangitis…etc.). En ocasiones es preciso en el tratamiento la realización de técnicas endoscópicas (CPRE) o quirúrgicas
Puede administrarse un tratamiento sintomático para el control del picor, por ejemplo con administración de fármacos como Colestiramina, Rifampicina o Fenobarbital . Para tratar de disolver los cálculos (piedras) biliares que producen colestasis o acúmulo de bilis por obstrucción de las vías biliares, se pueden utilizar fármacos como el ácido ursodesoxicólico ( Ursubilane ®). A veces es preciso tratar el déficit vitamínico que se puede producir en colestasis intensas y prolongadas por malabsorción, administrando por ejemplo, suplementos de vitamina A ( Auxina A Masiva ®), vitamina E ( Auxina E ®), vitamina D (Vitamina D3 ), y, si se constata necesidad, la vitamina K ( Konakion ® ).
El paciente debe estar bien hidratado para evitar la toxicidad de la bilirrubina a nivel del riñón.
Pruebas complementarias del tratamiento de la ictericia
Analítica de sangre : con determinación de hemograma, bioquímica que incluya enzimas hepáticas, fosfatasa alcalina, y bilirrubina.
Según la sospecha diagnóstica se solicitará en la analítica el estudio de serología de los virus de la hepatitis A, B y C (para detectar su presencia), determinantes del metabolismo del hierro (hierro, ferritina y transferrina), marcadores tumorales…etc. También se puede solicitar la determinación de algunas vitaminas que, cuando existe una obstrucción biliar prolongada, pueden no absorberse adecuadamente.
Se realiza una ecografía abdominal como técnica de imagen de elección para valorar la patología hepatobiliar, sobre todo si se sospecha de ictericia por obstrucción de la vía biliar.
Otras pruebas de imagen que complementan la visualización del abdomen y detectan lesiones que no se detectan con la ecografía y que se pueden realizar son un TAC abdominal , una colangioresonancia y una colangiopancreatografía retrógrada endoscópica (CPRE) .
En ocasiones, según la causa, puede precisarse la realización de una biopsia hepática : extracción de una pequeña cantidad de tejido para analizarlo.
Factores desencadenantes de la ictericia
El factor desencadenante de la ictericia es el acúmulo en la sangre de la bilirrubina (conjugada o directa / no conjugada o indirecta).
Factores de riesgo de la ictericia
Consumo de alcohol.
Factores de riesgo para el contagio de hepatitis víricas como prácticas sexuales sin protección, realización de tatuajes o piercings , requerimiento de transfusiones sanguíneas, y administración de fármacos o drogas por vía intravenosa.
Exposición a agentes químicos, toxinas hepáticas, fármacos (antiinflamatorios no esteroideos, antibióticos, estatinas…etc), esteroides anabolizantes, preparados de herbolario o multivitamínicos.
Antecedentes de cirugía hepática o biliar previa.
Antecedentes familiares de enfermedades hepáticas o padecimiento de ictericia.
Obesidad.
Embarazo.
Haber recibido un trasplante de médula ósea o hepático.
Edad: recién nacidos, sobre todo si son prematuros.
Bajo peso al nacer.
Lactancia materna exclusiva.
Alta precoz del recién nacido sin seguimiento posterior.
Sexo masculino.
Hijo de madre diabética.
Tener un hermano que al nacer tuviera ictericia.
Pérdida de peso en el recién nacido.
Padecimiento de enfermedades que producen la obstrucción biliar como tumores, o cálculos.
Padecer traumatismos con gran producción de hematomas.
Complicaciones de la ictericia
Alteraciones neurológicas por aumento grave de bilirrubina : encefalopatía aguda.
Prevención de la ictericia
No consumir alcohol.
No consumir drogas por vía parenteral.
Medidas de protección en las relaciones sexuales.
Vacunación contra la hepatitis.
Realizar una dieta variada, rica en fibra y verdura.
Control de los niveles de colesterol.
Tratamiento de los procesos de litiasis biliar para prevenir obstrucciones.
En recién nacidos se aconseja lactancia materna al menos 8-12 veces al día durante los primeros días, y aquellos que pierden más del 10% de su peso al nacer deben ser evaluados por un profesional entrenado en lactancia.
Evitar medicamentos y toxinas que pueden causar hemólisis o dañar directamente el hígado.
Especialidades a las que pertenece la ictericia
Los médicos especialistas que evalúan y tratan la ictericia de los pacientes pueden ser especialistas en aparato digestivo, pediatras, cirujanos generales, médicos internistas…etc, dependiendo de la causa que la produce.
Preguntas frecuentes:
¿Qué es la bilirrubina?
Es un pigmento biliar rojo que se forma por degradación de la hemoglobina de los glóbulos rojos en el bazo (como bilirrubina no conjugada),que es transportada unida a una proteína hacia el hígado (donde se conjuga) y posteriormente se excreta por las vías biliares hacia el intestino, donde se elimina por las heces en un 90%. Un pequeño porcentaje se elimina por la orina.
¿Cuánto tarda en quitarse la ictericia?
Depende de la causa del aumento de la bilirrubina y del tratamiento que requiera la patología que lo produce.
¿Qué pasa cuando tienes niveles altos de bilirrubina?
La bilirrubina cuando se presenta en unos niveles más altos de lo normal en la sangre produce una pigmentación de los tejidos mejor vascularizados (donde más sangre llega), como son la piel y la escleróticas (el blanco de los ojos).
¿Es más frecuente la ictericia en recién nacidos que en otras edades?
Sí, la denominada ictericia del recién nacido es una causa muy frecuente de ictericia en los niños por la inmadurez hepática que todavía pueden presentar. Aun así, esta no es la única causa que puede desencadenar la ictericia en los niños que, al igual que los adultos, pueden padecerla por otros motivos de aumento de la bilirrubina que.
¿Cómo evitar la ictericia en un recién nacido?
L a ictericia fisiológica del recién nacido no se puede prevenir, pero es fundamental el control del bebé por parte de profesionales en los días previos al nacimiento, sobre todo si el bebé presenta factores de riesgo para desarrollar la ictericia, y si este es prematuro.

Enfermedad
Herpangina
¿Qué es la herpangina?
La herpangina es una enfermedad infecciosa que puede ser producida por varios virus del género Enterovirus , que aparece normalmente en niños menores de 4 (años aunque también se puede dar en niños de entre 3-10 años), sobre todo en verano y en otoño. Produce lesiones en la boca y la faringe muy dolorosas. Es una enfermedad común que habitualmente no presenta gravedad, aunque produce muchas molestias al niño.
Causas de la herpangina
El origen de esta enfermedad es la infección por virus del género Enterovirus (Cosackie A1-10, A16, A22 y B1-5 y los Echovirus 3, 6, 9, 11, 16, 17, 25 y 30), cuya transmisión se realiza por contagio fecal-oral o por pequeñas gotas expulsadas por la tos. Su periodo de incubación es de 3 a 6 días, y durante él pueden ser contagiado a otros niños.
Síntomas de la herpangina
Aparece fiebre y malestar general de forma brusca con dolores musculares . Comienzan a salir unas manchitas rojas en la boca y en la faringe que después se convierten en pequeñas vesículas de 1-2 mm, de coloración blanquecino-grisáceas con una corona rojiza alrededor. Poco a poco se van agrandando y finalmente tienden a ulcerarse. Esto produce un dolor importante en la orofaringe , sobre todo al tragar. Evoluciona a una resolución espontánea en unos 5-6 días.
Tratamiento para la herpangina
El tratamiento es sintomático, adoptando medidas generales de hidratación y alimentación blanda y poco irritante. Además, se indica analgesia y control de la fiebre (por ejemplo con Paracetamol ). A veces se asocian soluciones anestésicas tópicas para ayudar a controlar el dolor en las lesiones.
Pruebas complementarias del tratamiento de la herpangina
El diagnóstico de la herpangina se realiza básicamente por la situación clínica que presenta el paciente. Sólamente en casos dudosos y muy determinados se realizan cultivos celulares y determinación de la presencia del virus en las heces y el exudado de las lesiones.
Factores desencadenantes de la herpangina
El factor desencadenante de la infección es la entrada del virus en el organismo.
Factores de riesgo de la herpangina
La convivencia o contacto con un paciente que tiene la infección es el mayor factor de riesgo para poderse contagiar por el virus y padecer esta enfermedad.
Complicaciones de la herpangina
Las principales complicaciones posibles son la deshidratación del niño y la anorexia (falta de apetito), producidas por el dolor que le produce el tragar por las lesiones que le salen en la boca y en la faringe.
Prevención de la herpangina
Para prevenir la infección se debe lavar las manos del niño a menudo para prevenir la propagación de la enfermedad, así como las de todas las personas que conviven con él.
También es recomendable lavar aquellos elementos y ropa (sábanas, toallas…etc.) con los que habitualmente está en contacto el niño.
Especialidades a las que pertenece la herpangina
Es una enfermedad que de manera habitual es diagnosticada y tratada por el pediatra o el médico de familia.
Preguntas frecuentes:
¿Qué es el virus pie, mano, boca?
Los virus que provocan la enfermedad llamada boca-mano-pie, son algunos de los virus de la especie de los Enterovirus , provocando esta infección que aparece sobre todo en niños de 1-3 años y que se da en brotes, sobre todo en primavera y verano. Produce fiebre, malestar general y aparición de ampollas pequeñas dentro y fuera de la boca, palmas de las manos, plantas de los pies y el área del pañal.
¿Qué es un exantema viral?
Un exantema viral es la aparición de una erupción cutánea producida por la infección de un virus. Existen varios tipos de infecciones víricas que pueden producir este tipo de lesiones dérmicas con características comunes y diferenciales de cada una (sarampión, rubéola, mononucleosis…etc).
¿Qué es el rash cutáneo?
Un rash cutáneo es una erupción de la piel que tiene unas características morfológicas según una enfermedad concreta. Frecuentemente lo que se da es enrojecimiento, picor y pequeños “granitos”.
¿Qué es el sarpullido en la piel?
Un sarpullido es un nombre coloquial que se le da a la aparición de lesiones punteadas rojizas que producen picor en la piel.

Enfermedad
Fibrosis Quística
¿Qué es la fibrosis quística?
Enfermedad autosómica recesiva (ambos padres deben tener el gen) que se da tanto en hombres como en mujeres, siendo mayor el índice de supervivencia en los hombres. Es más común en niños y adultos jóvenes. Es una enfermedad de tipo grave.
Tipos de fibrosis
Existen numerosos tipos de fibrosis, siendo las más habituales:
Fibrosis quística: afecta a los pulmones y al páncreas, por un exceso de producción de mocos las cuales se acumulan en las vías respiratorias y produce alteraciones en las mismas.
Fibrosis pulmonar: afecta al tejido de los pulmones, el cual se cicatriza y se vuelve grueso, provocando alteraciones en la respiración y la oxigenación de los órganos.
Fibrosis endomiocárdica: en este caso la fibrosis se produce en el endocardio al inflamarse por engrosarse las paredes del corazón.
Causas de la fibrosis quística
La fibrosis quística es una enfermedad hereditaria que se ocasiona por una anomalía en uno de los genes del individuo.
Esta alteración del gen provoca que el organismo genere moco excesivo el cual se acumula en las vías respiratorias, los pulmones y el páncreas generando problemas graves en el cuerpo del paciente.
Síntomas de fibrosis quística
Al ser una enfermedad que sobre todo afecta a los pulmones los principales síntomas se manifiesta en las vías respiratorias, pero también en otras partes del cuerpo. Los síntomas más frecuentes son:
Pólipos nasales.
Congestión nasal.
Neumonías.
Tos.
Fiebre.
Infección.
Tratamiento para la fibrosis quística
La finalidad del tratamiento es controlar los síntomas de la enfermedad ya que no tiene una cura a día de hoy.
El tratamiento suele basarse en medicamentos a ntiinflamatorios, antibióticos y broncodilatadores, entre otros.
También existen terapias adicionales como fisioterapia o la terapia del chaleco para reducir la acumulación de mucosa en el pecho. En algunos casos el paciente puede necesitar una intervención quirúrgica para eliminar pólipos nasales o incluso realizar un trasplante del pulmón.
Cada tratamiento es diferente según el paciente y la gravedad de su enfermedad.
Pruebas complementarias del tratamiento de fibrosis quística
Al tratarse de una enfermedad hereditaria las pruebas se suelen hacer en la primeras horas de vida de los bebés, de manera que en una analítica se observan los niveles del tripsinógeno inmunorreactivo (sustancia química que libera el páncreas que indica fibrosis quística), aunque tras un parto prematuro o complicado pueden estar alterados por lo que se suelen realizar otras pruebas como el test del sudor.
También, puede realizarse un estudio genético de los padres para ver si son portadores del gen anómalo y la posibilidad de que el bebé padezca la FQ.
Factores desencadenantes de la fibrosis quística
El factor desencadenante de la fibrosis quística es la mutación de un gen.
Factores de riesgo de fibrosis quística
Al tratarse de una mutación en los cromosomas uno de los factores de riesgo es la herencia genética , transmitiendo la enfermedad de padres a hijos.
Otro factor de riesgo es la raza , ya que es más habitual en personas blancas del norte de europa.
Complicaciones de la fibrosis quística
Insuficiencia respiratoria.
Neumotórax.
Hemoptisis (tos con sangrado).
Reagudizaciones (agravamiento de los síntomas de la FQ).
Aparición de infecciones crónicas.
Prevención de la fibrosis quística
La fibrosis quística no se puede prevenir ya que es hereditaria fruto de una alteración del cromosoma 7.
La única medida preventiva es analizar los cromosomas de los padres para evaluar la posibilidad de que se transfiera a los hijos.
Especialidades a las que pertenece la fibrosis quística
La fibrosis quística es tratada por la rama médica de neumología y si se precisa intervención quirúrgica sería tratada por el cirujano torácico.
Preguntas frecuentes:
¿Es la fibrosis quística hereditaria?
Si. Su origen está en la mutación de un gen del cromosoma 7 lo que genera una excesiva cantidad de moco que se acumula en las vías respiratorias y páncreas.
¿Qué esperanza de vida tiene alguien con fibrosis quística?
La esperanza de vida en pacientes con fibrosis quística cada vez es mayor, siendo a día de hoy de casi 40 años en muchos casos.
¿Cómo se hace el test del sudor?
Mediante el test del sudor se mide la cantidad de cloruro sódico presente en el organismo, el cual es indicador de fibrosis quística.
La prueba se realiza colocando un par de electrodos en la zona delantera del brazo y se suministra un medicamento a través de ellos, de manera que se estimulan las glándulas sudoríparas.Justo después se coloca otro dispositivo que recogerá la muestra de sudor.
¿Es contagiosa la fibrosis quística?
No. Es una enfermedad congénita que se origina por la mutación de un gen.
¿A quién afecta la fibrosis quística?
Al ser una enfermedad congénita que se transmite de manera autosómica recesiva, es decir, que se transmite de padres sanos a hijos , es a estos a quienes afecta. Esta enfermedad además es más frecuente en personas de raza blanca.

Enfermedad
Psicología Infantil
Actualizado el 10/01/2022
La psicología infantil está centrada en el estudio del comportamiento de los niños, teniendo en cuenta el desarrollo físico, cognitivo, social y afectivo, que se produce en las primeras etapas de la vida.
¿Qué es la psicología infantil?
La Psicología Infantil aborda el comportamiento, el desarrollo y las necesidades psicológicas de niños, adolescentes y de sus familias. De este modo, se encarga del estudio y tratamiento de los problemas psicológicos que se pueden producir dando lugar a patologías como autismo, hiperactividad, adicciones, acoso, etc.
Desarrollo infantil
Determinadas situaciones relacionadas con el desarrollo de los niños y adolescentes pueden influir en su comportamiento:
Factores ambientales . El entorno en el que crece el niño es un factor clave a la hora de desarrollar su carácter y funcionamiento. Son clave el entorno familiar y escolar. Existen niños especialmente susceptibles en los que pequeños cambios son suficientes para alterar su comportamiento. Otros presentan una gran capacidad de adaptación, incluso ante situaciones graves.
Factores biológicos. Las alteraciones durante el embarazo y el parto y los antecedentes familiares de enfermedades mentales son factores que influyen en el comportamiento de los niños. De igual modo, la genética puede condicionar de manera importante el desarrollo y el comportamiento del niño, así como la predisposición a padecer determinadas patologías psicológicas.
De este modo, el análisis de los factores ambientales y biológicos puede permitir comprender su comportamiento y la presencia de trastornos en el ámbito social, emocional y afectivo o en el aprendizaje.
Función de un psicólogo infantil
Los psicólogos infantiles trabajan para prevenir y tratar patologías y trastornos a través de la investigación, la educación y la atención directa al paciente. Entre sus funciones también está promover conductas que mejoren la salud psicológica y física y tratar el comportamiento y los aspectos emocionales que tienen lugar en los más jóvenes.
La intervención psicológica infantil se sirve de técnicas diferentes a las utilizadas con adultos. El psicólogo infantil debe partir de un conocimiento profundo en otras áreas de la psicopatología, incluyendo la psicología evolutiva, de la educación y el desarrollo neurocognitivo, entre otras.
Evaluación psicológica
El proceso de evaluación psicológica debe utilizar unas herramientas psicométricas adaptadas a las características de los pacientes en edad infantil. Una de las evaluaciones previas necesarias es el grado de desarrollo neurocognitivo del niño. Además, para llevar a cabo una evaluación psicológica se deberá tener en cuenta que los tiempos de trabajo son menores, puesto que los niños son más propensos al agotamiento y la pérdida de atención.
Trastornos psicológicos más comunes en niños
Los trastornos psicológicos más habituales en niños tienen una repercusión directa en su manera de comportarse, aprender y manejar las emociones, lo que suele causar problemas en sus actividades y suele ser motivo de preocupación en sus padres.
Entre los trastornos más comunes destacan:
Problemas de ansiedad.
Depresión.
Trastornos de la conducta.
Trastorno por déficit de atención e hiperactividad (TDAH).
Trastorno obsesivo-compulsivo.
Trastorno por estrés postraumático.
Otras afecciones que afectan el aprendizaje, el comportamiento y las emociones de los niños incluyen las discapacidades del aprendizaje y del desarrollo y patologías como el autismo. Además, se cuentan también el consumo de sustancias, especialmente en adolescentes, y las autolesiones.
Técnicas de la psicología infantil
Es importante tener en cuenta que las habilidades comunicativas de los niños, especialmente los de menor edad, son limitadas. Esto es todavía más notorio cuando se trata de describir e identificar emociones, afectos y sentimientos. De este modo, se hace indispensable que el psicólogo infantil domine las herramientas y técnicas psicológicas necesarias para trabajar con los más jóvenes interaccionando con ellos de una forma natural.
En este sentido, se pueden utilizar técnicas basadas en el dibujo, los juegos, así como la representación y expresión corporal.
Preparación
Es importante la implicación de la familia y, en su caso, de los educadores del niño a la hora de afrontar una terapia o evaluación psicológica infantil. De este modo, los padres o adultos a cargo del niño deberán acudir previamente a una cita con el psicólogo infantil para preparar la estrategia.
Duración de las terapias psicoterapéuticas infantiles
La duración de las terapias en psicología infantil puede ser muy variable y dependerá de la patología y las características de partida de cada niño. A grandes rasgos, las terapias infantiles suelen durar unos meses hasta que se nota una mejoría en el niño, y posteriormente tendrán lugar citas concretas para revisar que la evolución es la adecuada.
En cualquier caso, la realización de una evaluación psicológica ante un comportamiento anormal o llamativo para los padres o educadores no conlleva necesariamente la presencia de una patología o trastorno psicológico ni la necesidad de una terapia.
Preguntas frecuentes
¿En qué se diferencian la psicología infantil y la de adultos?
La psicología analiza la situación psicológica y emocional del individuo para generar pautas de mejora que puedan redundar en un mayor bienestar y calidad de vida, enfrentando trastornos y patologías. La psicología infantil tiene en cuenta, además, el entorno y las circunstancias biológicas del niño haciendo un especial hincapié en el desarrollo físico y emocional.
¿Son especiales los psicólogos para niños?
Los psicólogos infantiles están especializados en la rama de la psicología infantil, por tanto, conocen el desarrollo de los niños y cómo abordar los trastornos y patologías que se pueden dar en esta etapa de la vida.
¿Qué técnicas o terapias utiliza la psicología infantil?
La psicología infantil desarrolla terapias mediante juegos o de manera colectiva con la participación de los padres o familiares para que el niño se sienta a gusto durante su puesta en marcha y pueda comportarse de forma espontánea.
¿Cuál es la edad mínima recomendada para ir al psicólogo?
No existe una edad mínima recomendada para acudir al psicólogo. Ante disfunciones en el desarrollo y el comportamiento de los pequeños siempre es recomendable consultar con un profesional.
¿Qué es la psicología infanto-juvenil?
La psicología infanto-juvenil es aquella que centra su estudio y tratamiento en pacientes desde su nacimiento hasta llegar a la etapa adulta.
¿De qué modo ha afectado la pandemia de la COVID-19 a la psicología infantil?
Los niños y adolescentes constituyen un colectivo especialmente vulnerable ante situaciones estresantes inesperadas de carácter global como la pandemia de la COVID-19. Entre los principales riesgos a los que han estado expuestos destaca el estrés psicosocial. La cuarentena, la hospitalización del niño o un familiar son situaciones que pueden generar altos niveles de estrés. Además, la limitación de acceso a los servicios de salud mental durante los momentos más graves de la pandemia ha agravado los problemas psicológicos previos del niño o provocado nuevos problemas. Este hecho ha sido especialmente grave en el caso de colectivos con patologías como la diversidad funcional o el autismo.
Bibliografía
Asociación Española de Psicología del niño y adolescente.
Asociación Española de Pediatría. En Familia. Comportamiento en niños preescolares: algunas dificultades. Consultado: 27/12/2021 .
Parrish C et al. Pediatric medical psychology. Int Rev Psychiatry 2020; 32(3): 284-297. Doi: 10.1080/09540261.2019.1705258 .
Centros para el Control y la Prevención de Enfermedades. La salud mental de los niños. Tipos de afecciones. 22/03/2021. Consultado: 27/12/2021 .
Plataforma de Asociaciones de Psiquiatría y Psicología Clínica por la Salud Mental de la Infancia y Adolescencia de España. Salud Mental en la Infancia y la Adolescencia en la era del COVID-19. 2020. Consultado: 27/12/2021 .
Enfermedad
Enfermedad de Perthers
¿Qué es la enfermedad de Perthes?
La enfermedad de Perthes, también conocida como Legg-Perthes-Calve es una afectación de la cabeza del fémur en la cual se produce necrosis por falta de aporte sanguíneo a la misma. Se da en niños en un 80% de los casos y suele ser unilateral (en una sola pierna), aunque hasta un 10% son bilaterales (en ambas piernas). Suele presentarse entre los 3 y los 12 años , y se da en 1 de cada 10.000 niños. Es una enfermedad leve, aunque puede ser más grave en niños mayores.
Causas de la enfermedad de Perthes
La causa es la falta de aporte sanguíneo de modo efectivo a la cabeza del fémur.
Síntomas de la enfermedad de Perthes
Los síntomas suelen ser dolor en la cadera , que se intensifica cuando el paciente realiza actividad física, que puede irradiarse hacia la rodilla y causar cojera y que se alivia con el reposo. Además habrá restricción de la movilidad a la exploración en rotación interna y separación, pudiendo aparecer una atrofia del músculo cuádriceps en casos más avanzados.
Tratamiento para la enfermedad de Perthes
El tratamiento estará compuesto por antiinflamatorios y reposo , por ello, será necesaria la deambulación con muletas y la colocación de inmovilizaciones si se precisa, para mantener una correcta alineación de la cadera, así como ejercicios de fisioterapia en agua para tratar de mantener la musculatura sin realizar carga sobre el hueso.
En niños mayores de 12 años o en casos muy evolucionados puede ser necesaria la cirugía de cadera , bien para alargar un tendón, bien para intervenir sobre la pelvis situando de modo correcto la cabeza del fémur sobre el cotilo.
Pruebas complementarias del tratamiento de la enfermedad de Perthes
La prueba complementaria principal será de imagen, una radiografía de ambas caderas y, cuando esta sea normal y haya una alta sospecha de enfermedad, puede ser necesario realizar una resonancia magnética que permitirá ver lesiones más precoces.
Factores de riesgo de la enfermedad de Perthes
Entre los factores de riesgo de la enfermedad de Perthes están el sexo, ya que los niños sufren 4 veces más esta enfermedad que las niñas, la complexión, ya que si los niños son delgados o tienen mucha actividad física también tendrán más posibilidades de sufrirla, y si son más pequeños de lo normal para su edad, lo cual constituye otro factor de riesgo.
Complicaciones de la enfermedad de Perthes
Artrosis de cadera en adultos.
Prótesis de cadera precoz en adultos.
Prevención de la enfermedad de Perthes
Los factores de riesgo de esta enfermedad hacen que no sea prevenible.
Especialidades a las que pertenece la enfermedad de Perthes
El médico implicado en el tratamiento y control de la enfermedad de Perthes será el traumatólogo
Preguntas frecuentes
¿Cuáles son las fases de la enfermedad de Perthes?
Las fases de la enfermedad de Perthes son:
Etapa inicial : se detiene el crecimiento de la cabeza femoral, hay una zona de fractura bajo el cartílago, la cabeza se ve más densa de lo normal y dura unos seis meses.
Etapa de fragmentación : se produce una esclerosis de la cabeza del fémur, hay zonas más claras, el acetábulo se vuelve irregular, y suele durar unos 8 meses.
Etapa de osificación : se comienza a regenerar la cabeza femoral, que comienza a redondearse. Fase que dura unos 12 meses.
Etapa residual : abarca todo el crecimiento del niño, el hueso se remodela a nivel de fémur y del acetábulo.
¿A quién afecta la enfermedad de Perthes?
La enfermedad de Perthes afecta a niños de entre 3 y 12 años , siendo más frecuente en niños que en niñas (afecta a 4 niños por cada niña). La enfermedad deja más secuelas entre los niños más mayores que entre los más pequeños.
¿Qué secuelas tiene la enfermedad de Perthes?
Las secuelas aparecen a largo plazo, pudiendo dar lugar a artrosis y precisar de prótesis de cadera de forma precoz en la edad adulta. Si el niño es mayor y la lesión más lateral y más extensa, es más fácil es que haya secuelas en un futuro.
¿Qué es la enfermedad de Batten?
La enfermedad de Batten es un trastorno del sistema nervioso , que es hereditario y mortal , y cuyos síntomas aparecen entre los 5 y 10 años. El primer síntoma suelen ser convulsiones seguidas de alteración en la visión, se puede producir un deterioro mental y los niños pueden quedar encamados, ciegos y dementes. La mortalidad se suele producir alrededor de los 20 años, se da en 2 de cada 100.000 nacidos vivos, y para padecer esta enfermedad los dos padres deben ser portadores del gen anómalo, el gen afectado es el que produce la CLN3.
¿Qué es la enfermedad de Kohler?
La enfermedad de Kohler es una enfermedad que se produce en niños de entre 3 a 5 años, que suele ser unilateral y se da más en varones. En ella se produce aplanamiento y esclerosis del hueso escafoides , el niño presenta dolor e inflamación en la zona del pie, con mayor dolor a la presión en el arco interno del mismo. Raramente persiste más de dos años, su tratamiento es reposo, alivio del dolor y evitar el peso sobre la zona ósea. El cuadro se resuelve pasado ese tiempo, sin secuelas para el niño.

Enfermedad
Enfermedad de Mano-Pie-Boca
¿Qué es la enfermedad mano-pie-boca?
La enfermedad de manos, pies, boca es una infección de origen viral muy contagiosa , generalmente benigna, que es común en la infancia, afecta la cavidad oral y la región distal de las extremidades (manos y pies), que se caracteriza por la presencia de vesículas (pequeñas ampollas llenas de líquido en la piel) y llagas en la boca y una erupción cutánea en las manos y los pies.
Es más frecuentes en niños menores de 10 años, pero puede contagiarse a personas de todas las edades y en ambos sexos. Se extiende fácilmente a través del contacto con manos no lavadas, heces, saliva, mocos o el líquido de las ampollas . Su incidencia es mayor en los sitios donde hay poca higiene y sobrepoblación, normalmente se da en guarderías, centros de preescolar y otros lugares donde los niños comparten espacios reducidos y tienen contacto con objetos contaminados. Suele aparecer en los meses de verano y otoño y puede afectar a varios miembros de la familia. Es una enfermedad leve muy común, que desaparece espontáneamente después de algunos días.
Tipos de enfermedad mano-pie-boca
No se conocen tipos de la enfermedad mano pie boca.
Causas de la enfermedad mano-pie-boca
La causa más frecuente de la enfermedad de manos, pies y boca es la infección con el coxsackievirus A16, que pertenece al grupo de los enterovirus no polio. También existen otros tipos de enterovirus que lo pueden causar, lo que quiere decir que puede volver a repetirse.
Su transmisión es fundamentalmente fecal-oral , la ingestión oral es la principal fuente de infección por el coxsackievirus. La enfermedad se propaga por el contacto de persona a persona a través de los fluidos como: saliva, fluidos de las ampollas, heces, secreciones nasales y descargas de la garganta . También es posible que se transmitan con el contacto de objetos contaminados de los enfermos.
Síntomas de la enfermedad mano-pie-boca
La enfermedad mano pie boca tiene un periodo de incubación de 3 a 7 días , los síntomas que puede causar son: fiebre, dolor de garganta, cefalea, dolor abdominal, pérdida de apetito , lesiones dolorosas vesiculares (ampollas), de color rojo en la lengua, las encías y la cara interna de las mejillas, erupciones con ampollas pequeñas en las manos, los pies y en la zona donde se coloca el pañal que pueden estar sensibles o causar dolor si se presionan e irritabilidad en bebés y niños pequeños.
Tratamiento para la enfermedad-mano-pie-boca
No existe un tratamiento específico para la enfermedad de manos, pies y boca. Por lo general, los signos y síntomas duran entre siete y diez días. Para tratar los síntomas usan analgésicos-antitérmicos como paracetamol o ibuprofeno, para controlar la fiebre, el dolor y el malestar general causado por la enfermedad. También la hidratación, la ingesta de líquido es muy importante para evitar complicaciones. Un anestésico oral tópico puede ayudar a aliviar el dolor de las llagas en la boca.
Pruebas complementarias del tratamiento de la enfermedad mano-pie-boca
Para el diagnóstico y tratamiento se realiza un examen físico . Normalmente, se puede emitir sólo con los síntomas ya que son muy característicos, con solo ver las lesiones en la piel, ampollas y erosiones en las manos, los pies y la boca.
Factores desencadenantes de la enfermedad mano-pie-boca
El factor desencadenante principal de la enfermedad mano pie boca es el contacto con el virus coxsackievirus A16.
Factores de riesgo de la enfermedad mano-pie-boca
Los factores que aumentan el riesgo de la enfermedad mano pie boca incluyen:
La edad: la enfermedad de manos, pies y boca afecta principalmente a niños de menos de 10 años, principalmente niños menores de 5 años y lactantes.
Factor ambiental: los niños que se encuentran en centros de cuidado infantil son particularmente propensos a los brotes de la enfermedad de manos, pies y boca, debido a la propagación de infecciones en el contacto de persona a persona, y los niños pequeños son los más vulnerables.
Complicaciones de la enfermedad mano-pie-boca
La complicación más frecuente de la enfermedad de manos, pies y boca es:
La deshidratación: la enfermedad puede causar llagas en la boca y en la garganta, lo que produce dolor y dificultad para tragar.
Convulsiones.
Las complicaciones graves son poco frecuentes como son:
Onicomadesis: caídas de las uñas de las manos y los pies.
Encefalitis.
Meningitis aséptica.
Prevención de la enfermedad mano-pie-boca
Para prevenir la enfermedad mano pie boca es necesario:
Lavarse las manos frecuentemente con agua y jabón, en especial después de ir al baño o cambiar un pañal y antes de preparar alimentos y comer.
Desinfectar las áreas comunes.
Aislar a las personas que se puedan contagiar.
Evitar el contacto con personas que tengan esta enfermedad.
Especialidades a las que pertenece la enfermedad mano-pie-boca
La especialidad a la que pertenece la enfermedad mano pie boca es pediatría, la que se ocupa del estudio del crecimiento y el desarrollo de los niños hasta la adolescencia, así como del tratamiento de sus enfermedades.
Preguntas frecuentes
¿Cómo se contagia el virus mano-pie-boca?
Se contagia de persona a persona y se extiende fácilmente a través del contacto con manos no lavadas, heces, saliva, mocos o el líquido de las ampollas.
¿Cuánto tiempo dura la enfermedad mano-pie-boca?
La enfermedad mano pie boca dura de 3 a 7 días.
¿Qué es la enfermedad del beso?
La mononucleosis infecciosa o también conocida como la enfermedad del beso está provocada por un virus que se transmite a través de la saliva , se puede contraer al besar a alguien, aunque también cuando se queda expuesto a alguien que tose o estornuda, o al compartir un vaso o utensilio con alguien que tiene mononucleosis.
¿Qué es escarlatina infantil?
La escarlatina en niños, es una enfermedad exantemática causada por una bacteria , el estreptococo beta-hemolítico del grupo A, perteneciente a la misma familia que los gérmenes responsables de la amigdalitis. La bacteria se difunde a través del contacto directo con el moco o la saliva del niño infectado, con la saliva que se expulsa con la tos, con los estornudos o simplemente hablando, y penetra en el organismo a través de las mucosas de la nariz y de la boca.
¿Qué es un exantema viral?
El exantema vírico es una enfermedad producida por un virus que se manifiesta principalmente como una erupción rosacea en la piel . Es una enfermedad de carácter leve, provocada por un tipo de virus del herpes humano que provoca fiebre y erupciones similares a las del sarampión y la rubéola.
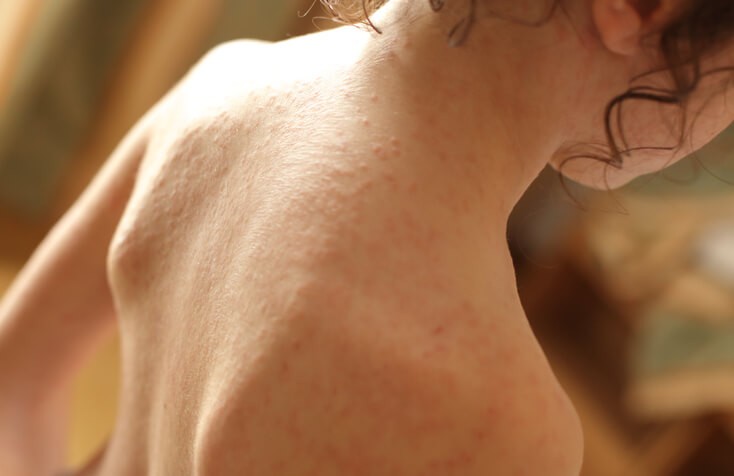
Enfermedad
Escarlatina
¿Qué es la escarlatina?
La escarlatina es una enfermedad producida por una bacteria cuando un paciente sufre amigdalitis estreptocócica , lo que provoca en el paciente una erupción en la piel de color rojo brillante, la cual se presenta en todo el cuerpo. Es también conocida por el nombre de fiebre escarlata , y es más frecuente en niños que en adultos. Se da en pacientes con amigdalitis estreptocócica. Se trata de una enfermedad de tipo leve que pertenece a la especialidad de enfermedades infecciosas.
Tipos de escarlatina
La escarlatina no se divide en diferentes tipos, ya que siempre es provocada por la bacteria Streptococcus del grupo A, conocida comúnmente como bacteria estreptococo.
Causas de la escarlatina
La causa principal por la cual se produce la escarlatina es debido a una infección bacteriana que expulsa una toxina, que a su vez provoca una erupción cutánea de tono rojizo generalizada por todo el cuerpo, así como otros síntomas.
Esta bacteria es la misma que provoca la amigdalitis estreptocócica.
Síntomas de la escarlatina
El principal síntoma de la escarlatina es la erupción de color rojo que se manifiesta por todo el cuerpo del paciente, teniendo un aspecto similar a una quemadura por el sol.
Otros síntomas son la llamada lengua de fresa , que provoca que se vea de color rojo e hinchada, con partes blancas. También se producen manchas en la cara marcando la zona de los labios con un anillo blanco.
El resto de síntomas destacados son fiebre, dolor de garganta, ganglios inflamados o dolores de cabeza, entre otros.
Tratamiento para la escarlatina
Al tratarse de una enfermedad bacteriana, el paciente será tratado con antibióticos para eliminar la infección, siendo muy importante completar el periodo indicado de toma del antibiótico para evitar que haya complicaciones por no eliminarse correctamente la bacteria.
También pueden recetarse al paciente cremas o medicamentos concretos para aplicar sobre las erupciones cutáneas y aliviar los síntomas, así como analgésicos para la fiebre y los dolores.
Pruebas complementarias del tratamiento de escarlatina
Para determinar si el paciente sufre escarlatina lo primero es realizar un examen físico , donde se le visualiza la garganta y las amígdalas.
Después, se evalúa si existe inflamación en los ganglios de la zona de la garganta, y por último se analizan las manchas rojizas de la piel por la erupción cutánea.
En algunos casos, el médico puede extraer una muestra de la parte de la faringe para realizar una analítica y ver si existe la presencia de las bacterias estreptocócicas.
Factores desencadenantes de la escarlatina
El principal factor desencadenante de la escarlatina o fiebre escarlata es la amigdalitis estreptocócica.
Factores de riesgo de la escarlatina
Esta enfermedad es más frecuente en niños que en adultos, sobre todo en edades comprendidas entre los 5 y los 15 años.
Al transmitirse por fluidos como la saliva, hay más riesgo de contagio entre familiares y amigos.
Complicaciones de la escarlatina
Fiebre reumática.
Infección de la bacteria en la piel, sangre, riñones… etc.
Anomalías en el sistema nervioso y articulaciones.
Prevención de la escarlatina
Mantener una correcta higiene, sobre todo lavando las manos antes de ingerir alimentos.
Evitar el uso compartido de cubiertos y/o alimentos.
Al toser o estornudar taparse la nariz y la boca.
Esterilizar los juguetes infantiles.
Especialidades a las que pertenece la escarlatina
La escarlatina es tratada por médicos de medicina general y los especialistas en enfermedades infecciosas.
Preguntas frecuentes
¿Es contagiosa la escarlatina?
Sí, se contagia a través de la saliva . Cuando entra en contacto la saliva de un paciente infectado con otra persona.
Desde los primeros síntomas ya se puede contagiar, y no es hasta las 48 horas siguientes de iniciar el tratamiento antibiótico cuando deja de ser una enfermedad infecciosa.
¿Qué personas tienen más riesgo de sufrir escarlatina?
La escarlatina se produce a raíz de una amigdalitis bacteriana que suele ser más frecuente en niños , y en personas que padecen amigdalitis frecuentes.
¿Cuánto tiempo dura la escarlatina?
Desde el contagio hasta que se supera la enfermedad, la escarlatina tiene una duración de entre 15 y 20 días.
¿Cuál es el periodo de incubación de la escarlatina?
El periodo de incubación se da entre los 2 y los 5 días previos a que aparezcan los primeros síntomas.
¿Puede haber escarlatina sin fiebre?
Sí. Aunque la fiebre es un síntoma característico del estreptococo que produce la escarlatina, en algunos casos puede no manifestarse.

Enfermedad
Enfermedad de Hirschsprung
¿Qué es la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung, también conocida como megacolon congénito, es la obstrucción congénita del colon producida por alteraciones en la inervación de este, que dan lugar a una falta de relajación del mismo y puede presentarse al nacer o aparecer algo más tarde. Se da entre 1 y 5 de cada 10.000 nacidos vivos y, en el 80% de los casos, el defecto está tan solo en el recto. El 10% de los casos ocupan el recto y el sigma y, por último, el 10% restante altera también el colon. Puede producir una perforación intestinal que precise de cirugía de urgencia, por lo que es considerada una enfermedad de tipo grave.
Tipos de enfermedad de Hirschsprung
Enfermedad de Hirschsprung de segmento ultracorto : ocupa solo el esfínter interno o un pequeño segmento yusta-anal.
Enfermedad de Hirschsprung de segmento corto : no va más allá de unión del recto con el sigma.
Enfermedad de hirschsprung de segmento largo : si la alteración va más allá de la unión del recto con el sigma.
Causas de la enfermedad de Hirschsprung
La causa es la alteración de la inervación del intestino, que da lugar a que no se puedan empujar las heces hacia el exterior al no producirse la relajación del intestino, lo cual da lugar a una obstrucción por detrás de dicho nivel.
Síntomas de la enfermedad de Hirschsprung
El primer síntoma que suele aparecer es la dificultad para expulsar el meconio tras las 24 o 48 horas después del nacimiento. Otros síntomas serán heces explosivas y poco frecuentes, ictericia, falta de apetito, falta de ganancia de peso, vómitos y heces acuosas en los recién nacidos, y, en niños más mayores, puede aparecer falta de apetito, retraso del crecimiento y vientre hinchado.
Tratamiento para la enfermedad de Hirschsprung
Pueden ser necesarios enemas para vaciar el intestino, tras ello, hay que extirpar la parte de intestino anómalo, procediendo a realizar una anastomosis entre la parte sana del colon y el ano. Este procedimiento puede ser bien en un solo acto quirúrgico, bien en dos, siendo necesaria una colostomía (dar salida al recto a través del abdomen) durante un tiempo.
Pruebas complementarias del tratamiento de la enfermedad de Hirschsprung
Las pruebas complementarias serán manometría del ano, pruebas de imagen como radiología simple de abdomen o enema opaco, y además puede ser necesaria una biopsia anal para llegar al diagnóstico correcto.
Factores desencadenantes de la enfermedad de Hirschsprung
El factor desencadenante de la enfermedad de Hirschsprung es la falta de peristaltismo , que es el conjunto de movimientos de contracción del tubo digestivo que permiten la progresión de su contenido desde el estómago hacia el ano. Esto se produce por alteración en la relajación del colon, lo cual da lugar a una obstrucción a este nivel.
Factores de riesgo de la enfermedad de Hirschsprung
Entre los factores de riesgo está el tener un hermano con enfermedad de Hirschsprung , lo cual aumenta el riesgo, también el ser varón, ya que es más frecuente en varones, y padecer síndrome de Down , ya que en niños con esta patología aparece con mayor frecuencia que el resto de la población.
Complicaciones de la enfermedad de Hirschsprung
Enterocolitis (inflamación del intestino delgado y del colon).
Perforación intestinal.
Síndrome del intestino corto (pérdida anatómica o funcional de una parte del intestino delgado que ocasiona un cuadro clínico de graves alteraciones metabólicas y nutricionales).
Especialidades a las que pertenece la enfermedad de Hirschsprung
El niño será diagnosticado en general por un pediatra, y el tratamiento dependerá de un cirujano digestivo
Preguntas frecuentes
¿Debo tomar una dieta especial si tengo la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung no deja prácticamente secuelas tras la cirugía, las personas que la padecen pueden hacer una vida normal con dieta normal. Si el paciente presenta estreñimiento como secuela, deberá realizar una dieta rica en fibra con parte importante de frutas y verduras.
¿A quién afecta la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung afecta sobre todo a niños , dos veces más que a las niñas y, al ser una enfermedad congénita, se halla presente desde el nacimiento aunque en los casos más leves pueden tardar hasta seis meses en diagnosticarse.
¿Es hereditaria la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung puede ser hereditaria, aunque haya casos aislados, también se pueden presentar varios casos en una misma familia. La herencia es compleja ya que se encuentran alteraciones hasta en 11 genes diferentes capaces de producir la enfermedad. Es más frecuente en pacientes con Síndrome de Down.

Enfermedad
Enfermedad de Kawasaki
¿Qué es la enfermedad de Kawasaki?
La enfermedad de Kawasaki también conocida como síndrome mucocutáneo ganglionar, es una vasculitis aguda (inflamación aguda de los vasos sanguíneos), multisistémica auto limitada y febril casi exclusiva de lactantes y niños . Es una enfermedad que afecta a la piel, la boca y los ganglios linfáticos.
Produce la inflamación de las paredes de las arterias medianas de todo el organismo y tiende a afectar las arterias coronarias que suministran sangre al músculo cardíaco. Afecta, principalmente, a los niños menores de 5 años. Es más frecuente en niños con antepasados de origen japonés o coreano , aunque se puede dar en todos los grupos étnicos. Predomina más en el sexo masculino y es la mayor causa de anomalías cardiacas adquirida en los países occidentales. Esta enfermedad es poco común, rara para esta época y potencialmente mortal para los niños.
Tipos de enfermedad de Kawasaki
No han identificado tipos de la enfermedad de Kawasaki.
Causas de la enfermedad de Kawasaki
La enfermedad de Kawasaki, es todavía desconocida para la ciencia, aunque fue descubierta hace 40 años no se ha encontrado ninguna causa específica que la produce. Se sospecha de una respuesta inmunológica inducida por cualquier agente infeccioso o un superantígeno bacteriano en niños genéticamente susceptibles.
Síntomas de la enfermedad de Kawasaki
Los síntomas de la enfermedad de Kawasaki incluyen:
Fiebre que frecuentemente es superior a los (39°C) y dura más de tres días.
Ojos demasiado inyectados de sangre o rojos (sin pus ni supuración).
Una erupción en la parte principal del cuerpo (tronco) y en la zona genital, sin apariencia de ampollas.
Labios rojos brillantes , con hendiduras o agrietados.
Mucosas rojas en la boca.
Ganglios linfáticos del cuello y quizá de otra zona, inflamados.
Palmas de las manos y plantas de los pies rojas e hinchadas.
Irritabilidad.
Inflamación y dolor articular , con frecuencia en ambos lados del cuerpo.
Diarrea, vómitos y dolor abdominal. Entre otros síntomas.
Tratamiento para la enfermedad de Kawasaki
El tratamiento debe iniciarse lo antes posible tras la aparición de la fiebre. Los objetivos del tratamiento inicial son bajar la fiebre, la inflamación y prevenir el daño cardíaco.
Generalmente, el tratamiento consiste en administrar gammaglobulinas G no modificadas (anticuerpos purificados) por vía intravenosa. Las gammaglobulinas son un componente de la sangre que ayuda a luchar contra las infecciones. Las dosis altas de aspirina pueden ayudar a tratar la inflamación.
La aspirina también puede aliviar el dolor y la inflamación articular y también reducir la fiebre.
El tratamiento de Kawasaki es una excepción rara a la norma de no administrar aspirina a los niños. Una vez que no haya más fiebre, es posible que el niño necesite tomar una dosis baja de aspirina durante al menos seis semanas o más.
Pruebas complementarias del tratamiento de la enfermedad de Kawasaki
No existe una prueba específica disponible para el diagnóstico y tratamiento de la enfermedad de Kawasaki. Pero sí algunas pruebas que pueden ayudar a diagnosticarla como son: análisis de orina, análisis de sangre, radiografía de tórax y cuello, ecocardiograma y electrocardiograma.
Factores desencadenantes de la enfermedad de Kawasaki
No se conocen factores desencadenantes de la enfermedad de Kawasaki.
Factores de riesgo de la enfermedad de Kawasaki
Los factores de riesgo de la enfermedad de Kawasaki incluyen:
La edad: Los niños menores de 5 años tienen más riesgo de contraer la enfermedad de Kawasaki.
El origen étnico: Los niños de ascendencia asiática o de las Islas del Pacífico, como los japoneses o coreanos, tienen niveles más altos de enfermedad de Kawasaki.
El sexo: Los niños tienen un poco más de posibilidades que las niñas de contraer la enfermedad de Kawasaki.
Complicaciones de la enfermedad de Kawasaki
Las complicaciones de la enfermedad de Kawasaki incluyen:
Aneurisma en las arterias coronarias.
Inflamación de los vasos sanguíneos, generalmente de las arterias coronarias que suministran sangre al corazón.
Problemas de válvula cardíaca.
Inflamación del músculo cardíaco (miocarditis).
Ataque cardíaco.
Prevención de la enfermedad de Kawasaki
La enfermedad de Kawasaki no se puede prevenir ya que no se conoce su causa.
Especialidades a las que pertenece la enfermedad de Kawasaki
La enfermedad de Kawasaki pertenece a la especialidad de cardiología pediátrica. La cardiología pediátrica se dedica al estudio, diagnóstico y tratamiento de las enfermedades del corazón en los niños.
Preguntas frecuentes:
¿Cómo se transmite la enfermedad de Kawasaki?
No se conocen formas de transmisión de la enfermedad de Kawasaki.
¿Es curable la enfermedad de Kawasaki?
Si, la enfermedad de Kawasaki es totalmente curable.
¿Cuales son las secuelas de la enfermedad de Kawasaki?
Las secuelas de la enfermedad de Kawasaki incluyen: arritmias (cambios en el latido cardíaco) y se pueden producir anomalías en el funcionamiento de algunas válvulas cardíacas.

Enfermedad
Difteria
¿Qué es la difteria?
La difteria es una enfermedad infecciosa producida por una bacteria , la corynebacterium diphtheriae , en la antigüedad conocida con el nombre vulgar de garrotillo. En España no se dan casos de difteria desde el año 1986, pero sí se producen en otras zonas del este de Europa. Tiene una tasa de mortalidad en la difteria no cutánea de entre 5 y 10% , suele aparecer en los meses fríos y es más frecuente en menores de 15 años no inmunizados y en adultos que perdieron la inmunidad. Puede dar lugar a obstrucción de las vías aéreas, también puede producir miocarditis (inflamación del miocardio) y en algunos casos puede dar lugar a una neuropatía (enfermedad del sistema nervioso). Es una enfermedad grave dada su tasa de mortalidad.
Tipos de difteria
Los tipos de difteria son:
Difteria nasal : puede ser leve y cronificarse, da lugar a ulceraciones en el interior de la nariz.
Difteria faringoamigdalina: cursa con dolor de garganta y aumento de los ganglios del cuello, en casos graves pueden crearse membranas traqueales que pueden obstruir las vías respiratorias
Difteria cutánea : la mayoría de las lesiones se producen en los miembros, en ocasiones son superficiales y en el tórax lesiones más profundas a modo de úlceras que se recubren de una membrana grisácea.
Causas de la difteria
La causa de la difteria es la infección por parte del corynebacterium diphtheriae .
Síntomas de la difteria
En la difteria faríngea, se produce dolor de garganta, fiebre, dificultad para tragar, aumento del ritmo cardíaco, náuseas, vómitos y escalofríos . Posteriormente se va a observar la presencia de una membrana sobre las amígdalas, puede haber ronquera, cuello hinchado y ruido al respirar.
En la piel se pueden producir úlceras que no curan y que presentan una membrana gris que la recubre.
En la nariz se suele producir un cuadro más leve en el cual se producen secreciones.
En casos más graves puede haber postración (decaimiento), palidez e incluso llegar al coma.
Tratamiento para la difteria
Se debe administrar la antitoxina diftérica tan pronto como se sospeche la enfermedad, aunque no se tengan pruebas de laboratorio que lo confirmen.
El tratamiento de la difteria es con antibióticos como la Penicilina G Procaina en vía intramuscular en dosis de 300.000 unidades internacionales en pacientes menores de 10 kg y de 600.000 unidades internacionales en pacientes de más de 10 kg durante 14 días o la Eritromicina a dosis de 40 mg/kg/día en dosis cada 6 horas durante 14 días para eliminar la bacteria.
Pruebas complementarias del tratamiento de la difteria
Las pruebas complementarias serán el cultivo de las membranas y la tinción de gram que colorea las bacterias.
Se realiza una prueba de producción de la toxina difteria o bien se busca en la bacteria el gen productor de la misma.
Deben realizarse pruebas de electrocardiograma que permitirán descartar lesiones del corazón llamadas miocarditis.
Factores desencadenantes de la difteria
No hay factores desencadenantes de la difteria salvo el contagio con la bacteria corynebacterium diphtheriae .
Factores de riesgo de la difteria
El factor de riesgo principal es no presentar inmunidad para la bacteria, esta inmunidad solo se adquiere mediante la vacunación.
Complicaciones de la difteria
Obstrucción respiratoria.
Miocarditis.
Coma
Prevención de la difteria
Vacunación de la difteria mediante la vacuna con tétanos-difteria-tosferina y vacunación en adultos con la vacuna de tétanos-difteria con una periodicidad de cada diez años. La eficacia de la vacuna es del 97%.
Especialidades a las que pertenece la difteria
La difteria es una enfermedad que se controla por los servicios de medicina infecciosa de los hospitales que están formados por médicos de medicina interna.
Las difterias amigdalinas serán ingresadas en UCI y por tanto serán controladas por médicos intensivistas.
Preguntas frecuentes:
¿Cómo se contagia la difteria?
La difteria se contagia a partir de personas infectadas, que mediante las gotitas emitidas en estornudos y/o toses , dejan las bacterias en el aire, desde donde serán adquiridas por otras personas sensibles al germen.
¿Cuál es el nombre de la vacuna contra la difteria?
La vacuna contra la difteria es la vacuna DPT en niños, ya que lleva también inmunidad contra las tosferina y el tétanos. En los adultos es la Td, que lleva tambien la inmunidad para la tosferina.
¿Qué es el DTP?
La DTP es la vacuna contra el tétanos corresponde a la letra T, la tosferina corresponde a la letra P, ya que la bacteria que la produce es la bordetella pertussi , y la difteria que corresponde a la letra D.
Esta es la vacuna que se administra a los niños a los 2-4-6 meses con un recuerdo a los 18 meses y otro a los 4 años.
¿En qué países es más probable coger la difteria?
En Asia, países como India, Nepal y Bangladesh, Irán y Afganistán. En el sudeste asiático, países como Filipinas, Indonesia, Vietnam, Laos y Papua Nueva Guinea. En África en Nigeria. En Sudamérica en Brasil. Y en Europa en Albania, Armenia, Azerbaiyán, Bielorrusia, Estonia, Georgia, Kazajistán, Latvia, Lituania, Moldavia, Rusia, Tayikistán, Turkmenistán, Ucrania y Uzbekistán
¿Qué es la poliomielitis?
La poliomielitis es una enfermedad infecciosa, producida por el virus de la polio , que da lugar a daño en el tejido nervioso pudiendo causar parálisis.
Los síntomas son fiebre, cansancio, cefalea, vómitos, rigidez de cuello y dolor en los miembros, y puede causar una parálisis permanente. Es una enfermedad sin cura pero que se previene de modo eficaz mediante la vacunación.
Artículos por especialidad
CertificadosAlergologíaAnatomía PatológicaAnestesiología y ReanimaciónAngiología y Cirugía VascularAnálisis ClínicosAparato DigestivoCardiologíaChequeosCirugía General y del Aparato DigestivoCirugía General y del Aparato Digestivo PediátricaCirugía Oral y MaxilofacialCirugía Ortopédica y TraumatologíaCirugía Ortopédica y Traumatología PediátricaCirugía PediátricaCirugía Plástica y ReparadoraCirugía TorácicaClínica u HospitalDermatología Médico-Quirúrgica y VenereologíaEndocrinología y NutriciónEnfermeríaFisioterapiaGenética HumanaGinecología y ObstetriciaInmunologíaLogopedia y FoniatríaMedicina Estética y Unidad LaserMedicina Física y RehabilitaciónMedicina GeneralMedicina InternaMedicina NuclearMedicina del DeporteNefrologíaNeumologíaNeurocirugíaNeurofisiología ClínicaNeurologíaNutrición y DietéticaOdontología y EstomatologíaOftalmologíaOncología MédicaOncología RadioterápicaOsteopatíaOtorrinolaringologíaPediatríaPodologíaPoliclínicasPreparación al PartoPsicologíaPsiquiatríaRadiodiagnóstico-Diagnóstico Por ImagenReumatologíaTricologíaUnidad del DolorUrgencias HospitalariasUrología
Todas las especialidades  Savia
Savia