Enfermedades

Enfermedad
Esclerosis Lateral Amiotrófica
¿Qué es la Esclerosis Lateral Amiotrófica?
La esclerosis lateral amiotrófica es una en fermedad neurodegenerativa de tipo muscular que provoca la degeneración progresiva de las neuronas motoras, lo que limita el movimiento. Es también conocida como ELA o ALS , y se suele presentar en pacientes a partir de lo 50 años, siendo más frecuente en hombres que en mujeres. Se trata de una enfermedad de tipo grave perteneciente a la especialidad de neurología.
Tipos de esclerosis
Según el origen de la esclerosis lateral amiotrófica existen dos tipos:
Bulbar : el origen está en alteraciones que sufren las neuronas motoras del encéfalo, lo cual afecta primariamente al habla y al proceso de comer.
Medular : en este caso, la ELA se manifiesta al presentar debilidad motora en las extremidades del cuerpo.
Causas de la esclerosis lateral amiotrófica
La esclerosis lateral amiotrófica tiene diferentes causas, siendo la más conocida la debida a la herencia genética.
En muchos casos no es conocido su origen y en otros también puede deberse a una respuesta inmune del cuerpo que ataca al organismo del paciente, a un desequilibrio de sustancias químicas en el mismo o a una mutación de los genes que la desencadene pero que no sea por herencia genética.
Síntomas de esclerosis lateral amiotrófica
Los síntomas de la esclerosis lateral amiotrófica están relacionados con el sistema motor, siendo los principales:
Debilidad de la musculatura, sobre todo en las extremidades.
Calambres en los músculos.
Caídas por la pérdida de fuerza muscular.
Dificultades al hablar o comer.
Perder la respuesta motora al querer hacer un movimiento.
Tratamiento para la esclerosis lateral amiotrófica
En la actualidad no existe un tratamiento contra la ELA que permita una recuperación completa, pero bien es cierto que una medicación apropiada para cada paciente puede mejorar su calidad de vida y retrasar los síntomas más graves .
Generalmente, el tratamiento se basa en una medicación de por vida acompañada de terapias respiratorias, fisioterapia, ayuda psicológica y aprendizaje del lenguaje.
Pruebas complementarias del tratamiento de esclerosis lateral amiotrófica
Una vez analizados todos los síntomas del paciente se realizan una serie de pruebas para certificar si padece o no la ELA.
Entre estas pruebas se encuentran la resonancia magnética (tomando imágenes del cerebro y la médula espinal), una analítica completa de sangre, una electromiografía (consiste en la punción de músculos mediante una aguja para medir su actividad eléctrica), el estudio de la conducta (se analizan los nervios encargados de transmitir los impulsos nerviosos a los músculos) y en últimas opciones, se puede realizar una biopsia del músculo si aún hay ambigüedad en los resultados.
Factores desencadenantes de la esclerosis lateral amiotrófica
Los factores que provocan la esclerosis lateral amiotrófica son diferentes según cada paciente, siendo los principales la herencia genética o por respuestas autoinmunes del organismo.
Factores de riesgo de la esclerosis lateral amiotrófica
Hay una serie de factores que aumentan el riesgo de que una persona desarrolle la ELA, los más relevantes son:
La herencia genética.
El sexo, ya que es más frecuente en hombres que en mujeres.
La edad, suelen darse en personas mayores de 40 años.
Complicaciones de la esclerosis lateral amiotrófica
Demencia.
Dificultad para hablar.
Dificultad respiratoria, lo que puede requerir de una traqueotomía.
Dificultad para comer, necesitando una sonda.
Prevención de la esclerosis lateral amiotrófica
No fumar.
Evitar la exposición a productos tóxicos.
Realizar chequeos médicos.
Especialidades a las que pertenece la esclerosis lateral amiotrófica
La especialidad médica encargada de esta enfermedad es la neurología.
Preguntas frecuentes:
¿Qué diferencia hay entre esclerosis lateral amiotrófica y esclerosis múltiple?
La esclerosis múltiple (EM) se diferencia de la esclerosis lateral amiotrófica (ELA) debido a que la EM es una enfermedad autoinmune que tiene su origen en un virus o antígeno que ataca a las neuronas y su comunicación, provocando alteraciones cognitivas o emocionales, entre otras, mientras la ELA sólo afecta a las células motoras de los movimientos voluntarios.
¿Cuál es la esperanza de vida de una persona con esclerosis lateral amiotrófica?
Por lo general, los pacientes que son diagnosticados por ELA tienen una esperanza de vida entre los 3 y los 6 años desde que se les diagnostica.
¿Cómo sé si tengo ELA?
Si presenta algunos de los síntomas propios de la enfermedad, como la debilidad muscular o que el cuerpo no responde a los movimientos que quiere realizar, se debe acudir a un médico con urgencia para que al paciente se le realicen más pruebas y se de un diagnóstico seguro, ya que a menudo la ELA puede confundirse con otras enfermedades neurológicas.
¿Cuáles son los primeros síntomas de la esclerosis lateral amiotrófica?
Al ser una enfermedad que afecta a las neuronas motoras, los primeros síntomas que se muestran son: debilidad muscular en las extremidades, calambres, dificultad al hablar, comer y/o respirar.
Ante estos síntomas continuados es necesario acudir al médico.
¿Cuáles son las etapas de la ELA?
Los primeros síntomas que presenta la ELA se concentran en las manos y pies , extendiéndose progresivamente a otras partes del cuerpo según se van destruyendo las células neuronales motoras, incluso el paciente pierde el control de los esfínteres.
Poco a poco la enfermedad avanza hasta que afecta a funciones vitales como la respiración.

Enfermedad
Enfermedad de Menière
Actualizado el 13/12/2021
La enfermedad de Ménière es un trastorno del oído interno que afecta tanto a la audición como al equilibrio. Se caracteriza principalmente por la presencia de vértigos, constituyendo aproximadamente el 5% de todas las causas de vértigo.
¿Qué es la enfermedad de Ménière?
La enfermedad de Ménière es un síndrome clínico que afecta el equilibrio y la audición caracterizado por episodios de vértigo espontáneo que habitualmente se presentan con pérdida de audición o hipoacusia fluctuante que puede transformarse en persistente. Los pacientes escuchan ruidos (conocidos como acúfenos o tinnitus). En un 10-30% de los casos se pueden ver afectados los dos oídos.
Las crisis de vértigo son habitualmente mucho más frecuentes en los primeros años de la enfermedad.
La enfermedad de Ménière se presenta más habitualmente entre los 20 y los 50 años. Afecta más a mujeres que a hombres y cada año se registran de 34 a 190 casos por cada 100.000 habitantes.
Causas de la enfermedad de Menière
Las causas exactas de la enfermedad se desconocen. Se considera un trastorno multifactorial que se inicia probablemente por la combinación de factores genéticos y medioambientales. El exceso de fluido dentro de los canales del oído interno −conocido como hídrops endolinfático − presente en la mayoría de los pacientes con la enfermedad, se relaciona con los principales síntomas, si bien no explica todas las características clínicas de la enfermedad, incluyendo la progresión de la hipoacusia o la frecuencia de las crisis de vértigo.
Síntomas de la enfermedad de Ménière
Los síntomas que permiten diagnosticar la enfermedad, sin la existencia de otro diagnóstico que explique mejor los síntomas, incluyen:
Dos o más episodios de vértigo espontáneo con una duración entre 20 minutos y 12 h
Pérdida de audición o hipoacusia neurosensorial de frecuencias bajas y medias que debe ser documentada con audiometría.
Síntomas auditivos fluctuantes como hipoacusia, acúfenos y sensación de plenitud en el oído afectado.
Vértigo
El vértigo es uno de los principales síntomas de la enfermedad. Este se entiende como la sensación de movimiento propia cuando no se produce movimiento o la sensación de movimiento alterada durante un movimiento normal de la cabeza. Hay que diferenciarlo del mareo y la inestabilidad, si bien los pacientes con enfermedad de Ménière también pueden presentar mareos e inestabilidad a largo plazo.
Tratamiento para la enfermedad de Menière
No existe un tratamiento que pueda curar la enfermedad de Ménière, pero sí existen diversas estrategias que pueden ayudar a reducir la gravedad de los síntomas, especialmente la frecuencia de los episodios de vértigo.
En primer lugar, se recomienda seguir una dieta baja en sal y aumentar la ingesta de agua para prevenir la liberación de vasopresina y ayudar a mantener el equilibrio en el oído interno. La cafeína también puede provocar modificaciones en el volumen de la endolinfa por lo que se recomienda limitar el consumo de bebidas que la contengan (café, té, cola, etc.). De este modo se pretende controlar la acumulación de fluido en el oído interno que puede producir el vértigo.
Cuando el tratamiento dietético no resulta efectivo es necesario acudir a tratamientos médicos. Estos incluyen diferentes fármacos que se deben indicar en función de las características del paciente, como son los diuréticos y la betahistina.
Si estos no son efectivos, se debe realizar un tratamiento intratimpánico con esteroides como la dexametasona o con gentamicina, un antibiótico que se inyecta a través del tímpano y actúa en las células relacionadas con el equilibrio.
En ocasiones hay que recurrir a un tratamiento quirúrgico, realizando una neurectomía vestibular (una sección del nervio vestibular) o una laberintectomía. Se cree que la neurectomía vestibular es la técnica más eficaz en casos extremos en los que se producen crisis de vértigo con caídas (trastorno de Tumarkin) y para enfermedad de Ménière incapacitante. La laberintectomía es el método quirúrgico más antiguo para tratar la enfermedad y hoy en día se limita a pacientes de edad avanzada. La técnica se puede asociar con implantación coclear en caso de hipoacusia profunda en los dos oídos.
Pruebas complementarias del tratamiento de la enfermedad de Menière
El diagnóstico y tratamiento de la enfermedad se realiza en función de los síntomas que se presenten durante la enfermedad.
Entre las pruebas complementarias para el diagnóstico son: tomografía computarizada, resonancia magnética, estimulación calórica (exámenes de reflejos de los ojos), estudios de potenciales evocados, audiometría, pruebas vestibulares, electrococleografía, entre otras pruebas.
Factores de riesgo
Entre los factores que aumentan el riesgo de padecer la enfermedad de Ménière están: el consumo de alcohol, alergias, traumatismo craneal, antecedentes familiares, tabaquismo, enfermedad viral reciente, infección de oídos, estrés y migrañas, entre otros.
Complicaciones de la enfermedad de Menière
Entre las complicaciones de la enfermedad de Meniére están:
Episodios impredecibles de vértigo.
Trastorno de Tumarkin.
Pérdida de la audición permanente.
Imposibilidad de caminar o desempeñarse debido al vértigo incontrolable.
Fatiga y estrés emocional.
Ansiedad y depresión.
Especialidad médica encargada de tratar la enfermedad de Ménière
La enfermedad de Ménière pertenece a la especialidad de otorrinolaringología, que es la parte de la medicina especializada en el diagnóstico y tratamiento de las afecciones del oído, nariz y garganta.
Preguntas frecuentes
¿Cuántos tipos de vértigo hay?
Existen dos tipos básicos de vértigo: el vértigo periférico aparece como consecuencia de un problema en el oído interno que controla el equilibrio. Éste puede ser causado por efecto de ciertos medicamentos, haber sufrido una lesión (como un traumatismo craneal) o presentar una inflamación o presión en el nervio vestibular.
Por el contrario, el vértigo central es un problema cerebral. Puede ser causado por alguna enfermedad vascular, el consumo de ciertos fármacos, padecer migraña, esclerosis múltiple, haber sufrido un accidente cerebrovascular, o como causa de un tumor.
¿Qué es la neuritis vestibular?
La neuritis vestibular es un trastorno del sistema vestibular, la parte del oído interno que ayuda a controlar el equilibrio. Es causada frecuentemente por un virus que daña el nervio vestibular, que manda mensajes de movimiento y equilibrio entre el oído interno y el cerebro.
¿Qué es la laberintitis?
La laberintitis es una inflamación del laberinto, estructura del oído interno responsable del equilibrio.
¿Qué es la rehabilitación vestibular?
La rehabilitación vestibular es un tratamiento para el trastorno vestibular periférico unilateral que ayuda a mejorar el vértigo, el equilibrio y la movilidad.
¿Qué es el sentido cinestésico?
Es la capacidad que nos permite ser consciente del movimiento muscular y de la postura. El sentido cinestésico ayuda a controlar actividades como pararse, caminar, pasear, agarrar un objeto y hablar.
Bibliografía
López-Escámez JA et al. Criterios diagnósticos de enfermedad de Menière. Documento de consenso de la Bárány Society, la Japan Society for Equilibrium Research, la European Academy of Otology and Neurotology (EAONO), la American Academy of Otolaryngology-Head and Neck Surgery (AAO-HNS) y la Korean Balance Society. Acta Otorrinolaringológica Española 2016; 67(1): 1-7. DOI: 10.1016/j.otorri.2015.05.005 .
García E, González X. Actualización en el manejo del vértigo. AMF semFYC 2019;15(4):184-191. Consultado: 29/11/2021 .
Magnan J et al. European Position Statement on Diagnosis, and Treatment of Meniere’s Disease. J Int Adv Otol. 2018 Aug;14(2):317-321. Doi: 10.5152/iao.2018.140818 .
Murdin L, Schilder AG. Epidemiology of balance symptoms and disorders in the community: a systematic review. Otol Neurotol 2015 Mar; 36(3): 387-92. Doi: 10.1097/MAO.0000000000000691 .

Enfermedad
Epitrocleitis
¿Qué es la epitrocleitis?
La epitrocleitis es la inflamación de la inserción tendinosa que se encuentra en la cara interna del codo , también se conoce como codo de golfista. Afecta del 0,1 al 0.3% de la población y aparece entre los 40 y 50 años generalmente. En el 75% de los casos ocurre en el brazo dominante pudiendo afectar al nervio cubital. Es una enfermedad de tipo leve.
Tipos de epitrocleitis
La epitrocleitis es un solo tipo de enfermedad en la que se produce la inflamación de los músculos q ue se insertan en la parte medial del codo. Es una enfermedad que tiende a cronificarse , aunque tiene periodos largos de mejoría.
Causas de epitrocleitis
La causa principal del proceso de epitrocleitis, es el sobreesfuerzo por movimientos repetitivo s en la zona.
Síntomas de epitrocleitis
Los síntomas de la epitrocleitis son: dolor en la zona de la epitróclea (la cara interna del codo), que se irradia hacia el antebrazo, así como dolor al extender y flexionar la muñeca, dolor a la palpación y sensación de adormecimiento en la zona del antebrazo y la muñeca.
Tratamiento para la epitrocleitis
El tratamiento será por una parte conservador, con fisioterapia y farmacológico , y por otra tratamiento de tipo quirúrgico . El tratamiento conservador consiste en evitar el gesto que produce el dolor, realizar estiramientos tras hacer ejercicio, así como masajes transversales y la crioterapia, que puede mejorar el dolor. Puede ayudar colocarse una una codera para disminuir el esfuerzo sobre el tendón y el uso de antinflamatorios como el Ibuprofeno pueden aliviar la inflamación y el dolor. El tratamiento quirúrgico será un tratamiento excepcional, solo para tendinitis muy crónicas que no se alivian con tratamientos conservadores después de 6-12 meses de los mismos. Se puede realizar una cirugía abierta o una cirugía artroscópica que permite un tratamiento similar pero con mejor recuperación.
Pruebas complementarias del tratamiento de epitrocleitis
Las pruebas complementarias de imagen serán: radiografía de codo , que nos permite ver la calcificación del tendón, ecografía por parte de unidades especializadas, que puede dar información importante sobre los tendones, y la resonancia magnética , que además permite descartar otros procesos.
Factores desencadenantes de la epitrocleitis
Son factores desencadenantes los movimientos repetidos con el codo, en especial con este extendido.
Factores de riesgo de la epitrocleitis
Son factores de riesgo para esta lesión los traumatismos previos en la zona, soportar grandes pesos con los brazos y trabajar con martillos mecánicos o taladros. Está relacionada con prácticas de deporte como el golf, el tenis, el lanzamiento de jabalina y el béisbol.
Complicaciones de la epitrocleitis
Atrapamiento del nervio cubital.
Pérdida de fuerza muscular.
Neuropatía del nervio cubital.
Prevención de la epitrocleitis
Realización de estiramientos tras el entrenamiento.
Especialidades a las que pertenece la epitrocleitis
La epitrocleitis es controlada por el traumatólogo y el médico rehabilitador, el segundo será quien indique los ejercicios necesarios para la reparación tendinosa
Preguntas frecuentes
¿Qué diferencia hay entre epitrocleitis y epicondilitis?
La diferencia entre epicondilitis y epitrocleitis es la zona del dolor , y por tanto, los músculos implicados en su proceso.
En la epicondilitis el dolor se produce en la zona externa del codo y el músculo afectado es el supinador corto del carpo, sin embargo, en el caso de la epitrocleitis, el dolor se centra sobre la parte interna del codo y los músculos implicados, que suelen ser el pronador redondo y el músculo flexor radial del carpo.
¿Cuánto tiempo dura la recuperación de una epitrocleitis?
La recuperación de la epitrocleitis suele ser larga, esto se debe a que es muy difícil evitar los movimientos repetidos que se realizan en el trabajo o en un deporte determinado, pero se considera que el tratamiento no debe ser quirúrgico hasta que se ha mantenido de 6 a 12 meses el tratamiento conservador. Esto nos muestra que es un tipo de lesión de muy larga evolución, y, en muchos casos, tras un periodo de recuperación esta se vuelve a producir.
¿Qué ejercicios puedo hacer para curar la epitrocleitis?
Los ejercicios de estiramiento como flexionar y extender la muñeca, ejercicios de prona supinación de muñeca, flexión y extensión con peso ligero de muñeca con el codo apoyado, flexión extensión del codo con un peso de unos 500 gramos. Estos movimientos principalmente de estiramiento, se deben de realizar en especial tras hacer entrenamientos deportivos o en caso de trabajos que puedan provocar daño en estas articulaciones.
Enfermedad
Escabiosis
¿Qué es la escabiosis?
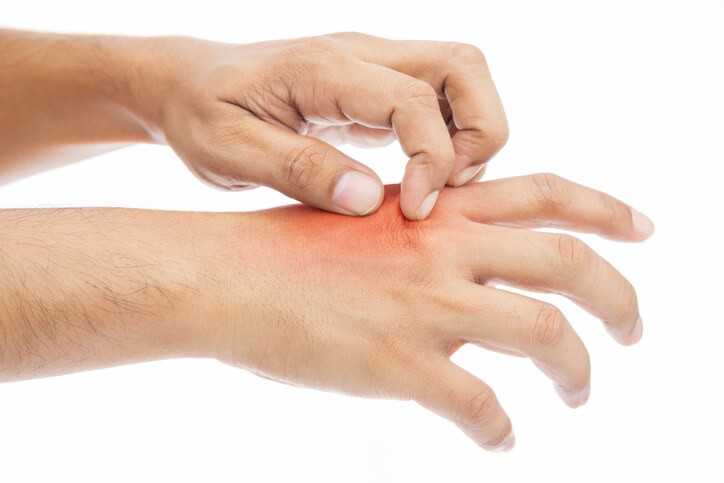
La escabiosis o sarna es una enfermedad cutánea de fácil propagación producida por un ácaro muy pequeño llamado sarcoptes scabiei de la variedad hominis , que infecta la piel y produce una erupción cutánea intensamente pruriginosa (picazón), con un patrón de distribución característico; se transmite por contacto directo o fomites (especialmente ropa, donde el parásito permanece viable 2-5 días).
Es una dermatosis parasitaria muy contagiosa y que se transmite fácilmente de una persona a otra por contacto físico, también puede ocurrir a través de animales u objetos. Su distribución es mundial, afecta a todas las edades y a ambos sexos.
Es un problema frecuente de salud relacionado con problemas sociales como la pobreza, hacinamiento, la desnutrición etc. Son más comunes en residencias de ancianos, residencias universitarias, guarderías y la prisión . La escabiosis debe tratarse rápidamente, de lo contrario puede ser muy peligrosa.
Tipos de escabiosis
Cuando se habla de la clasificación o los tipos de escabiosis, a lo que suelen referirse es a las diferentes maneras en las que la erupción puede aparecer. Estas pueden ser:
Sarna o escabiosis típica: Son erupciones cutáneas que aparecen en las manos y las muñecas principalmente. El cuero cabelludo y la cara no suelen verse afectados.
La escabiosis nodular: Es la más frecuente en lactantes y en niños pequeños. Puede deberse a hipersensibilidad a estos organismos retenidos. Presenta nódulo eritematoso de 5 a 6 cm en la ingle, genitales pliegues axilares y glúteos. Los nódulos son reacciones de hipersensibilidad y pueden persistir durante meses después de la erradicación de los ácaros.
La escabiosis infantil: Es una infestación de sarna que aparece en un niño o bebé, y se caracteriza a menudo por erupciones en las manos y los pies, así como la cara y el cuero cabelludo.
La escabiosis costrosa (noruega): se debe a una respuesta inmunitaria inadecuada por parte del huésped, lo que permite la proliferación de los ácaros que alcanza la cifra de millones. Aparecen parches eritematosos que descaman en las manos, pies y cuero cabelludo y pueden diseminarse.
La escabiosis incógnita: Es una forma generalizada y atípica producida por la aplicación de corticoides de uso tópico.
Causas de la escabiosis
La escabiosis es causada por el ácaro Sarcoptes Scabiei de la variedad hominis . El ácaro de ocho patas que causa la sarna en humanos es microscópico. El ácaro hembra excava justo debajo de la piel y produce un conducto en el que deposita huevos. Los huevos se abren, y la larva del ácaro llega hasta la capa externa de la piel donde madura y se puede propagar a otras zonas de la piel o de la piel de otras personas. La picazón de la sarna o escabiosis proviene de la reacción alérgica del organismo a los ácaros, sus huevos y sus excrementos.
Síntomas de la escabiosis
Los síntomas de la escabiosis son:
Prurito intenso (picazón grave), de predominio nocturno.
Úlceras sobre la piel por el rascado y la excavación.
Erupción cutánea , a menudo entre los dedos de manos y pies, la parte inferior de las muñecas, las axilas, las mamas y los glúteos.
Líneas delgadas y placas rojas en la piel . Entre otros síntomas.
Tratamiento para la escabiosis
El tratamiento primario para la escabiosis es con antiparasitarios (escabicidas) tópicos u orales como son:
La permetrina 5%: Es el fármaco de primera elección. Se trata de un piretroide sintético (pesticidas artificiales) que actúa sobre las membranas de las células nerviosas, retrasa la polarización y provoca la parálisis y la muerte del parásito. Se debe aplicar la crema en niños mayores y adultos desde el cuello hacia abajo y lavar después de 8 o 12 horas. Es necesario repetir el tratamiento a los 7 días.
Azufre: Se utiliza el precipitado de azufre al 6 o 10% en vaselina. Se aplica cada 24 horas durante tres días consecutivos, es eficaz y seguro, y suele utilizarse en lactantes menores de dos meses de edad.
La ivermectina: Está indicada en pacientes que no responden al tratamiento tópico, también si tienen inmunocompromiso y la escabiosis noruega. Se administra por vía oral una dosis única de 200 mg/kg.
Corticoides o antihistamínicos orales y/o tópicos : Se usan para el prurito (picazón).
El tratamiento va dirigido a pacientes, a sus contactos cercanos en forma simultánea, y a los objetos personales (vestimenta, toallas, ropa de camas) que deben lavarse con agua caliente y secarse con calor, además de aislarse por lo menos de 3 a 7 días, (en una bolsa de plástico cerrada), para evitar la infestación con ácaros que se desarrollan a partir de los huevos.
Pruebas complementarias del tratamiento de escabiosis
Para el diagnóstico y tratamiento, el médico debe realizar un examen físico completo donde va observar las características de la lesión en los surcos al examinar la piel en busca de signos de ácaros. Cuando localiza una madriguera de ácaros, puede hacer un raspado en esa zona para examinar la muestra bajo el microscopio . El examen puede determinar la presencia de ácaros o de sus huevos.
Factores desencadenantes de la escabiosis
El factor desencadenante es el contacto directo con el ácaro Sarcoptes Scabiei .
Factores de riesgo de la escabiosis
Entre los factores que aumentan el riesgo de contraer el ácaro Sarcoptes Scabiei incluyen: situaciones de hacinamiento como las guarderías, colegios, residencias, academias militares, campamentos, centros penitenciarios…
Convivir con una persona que padezca escabiosis o sarna. Entrar en contacto íntimo con alguien que padezca escabiosis o compartir sábanas o ropa , aunque es bastante raro el contagio.
Complicaciones de la escabiosis
El intenso rascado puede causar una infección secundaria de la piel como el impétigo, que es una infección superficial de la piel causada, con mayor frecuencia, por bacterias estafilocócicas o estreptocócicas.
La aparición de algunos nódulos intensamente pruriginoso que persisten aún después de controlar la parasitosis.
Prevención de la escabiosis
Para prevenir la escabiosis es necesario:
Evitar el hacinamiento.
Evitar el contacto con personas infectadas.
Lavar la ropa y sábanas con agua caliente.
Colocar los artículos que no se puedan lavar en una bolsa plástica sellada y dejarla en un lugar apartado durante un par de semanas. Los ácaros mueren después de unos días sin alimento.
Especialidades a las que pertenece la escabiosis
La escabiosis pertenece a la especialidad de dermatología, que se ocupa de tratar y diagnosticar las enfermedades de la piel.
Preguntas frecuentes
¿Se puede contagiar la escabiosis?
La escabiosis es contagiosa y el contagio se produce rápidamente por el contacto físico cercano, es decir, de persona a persona.
¿Cómo son las picaduras de los ácaros?
La picadura de los ácaros causa una erupción vesículo-papulo-eczematosa en forma lineal, con prurito (picazón) y enrojecimiento en los pliegues de la piel entre los dedos, alrededor de los genitales, en los lados de los pies y en las áreas del interior de los codos y las rodillas.
¿Qué es la sarna?
La sarna o escabiosis es una dermatosis parasitaria que provoca picazón intensa y es causada por pequeños ácaros o aradores de la sarna llamados Sarcoptes scabiei .
¿Cuándo deja de ser contagiosa la sarna?
Si se tiene un correcto tratamiento, los ácaros podrían dejar de ser contagiosos en 24 horas.
¿Cuánto tiempo tarda en curarse la sarna?
La sarna puede tardar en curarse hasta 3 semanas después de iniciarse el tratamiento.
Enfermedad
Enfermedad de Perthers
¿Qué es la enfermedad de Perthes?
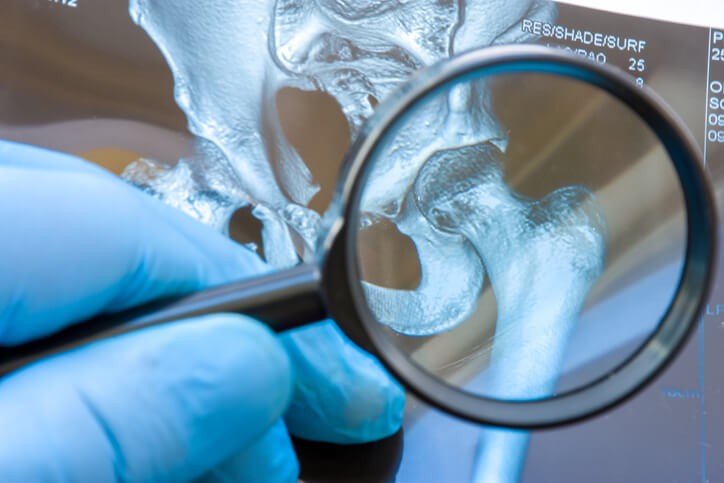
La enfermedad de Perthes, también conocida como Legg-Perthes-Calve es una afectación de la cabeza del fémur en la cual se produce necrosis por falta de aporte sanguíneo a la misma. Se da en niños en un 80% de los casos y suele ser unilateral (en una sola pierna), aunque hasta un 10% son bilaterales (en ambas piernas). Suele presentarse entre los 3 y los 12 años , y se da en 1 de cada 10.000 niños. Es una enfermedad leve, aunque puede ser más grave en niños mayores.
Causas de la enfermedad de Perthes
La causa es la falta de aporte sanguíneo de modo efectivo a la cabeza del fémur.
Síntomas de la enfermedad de Perthes
Los síntomas suelen ser dolor en la cadera , que se intensifica cuando el paciente realiza actividad física, que puede irradiarse hacia la rodilla y causar cojera y que se alivia con el reposo. Además habrá restricción de la movilidad a la exploración en rotación interna y separación, pudiendo aparecer una atrofia del músculo cuádriceps en casos más avanzados.
Tratamiento para la enfermedad de Perthes
El tratamiento estará compuesto por antiinflamatorios y reposo , por ello, será necesaria la deambulación con muletas y la colocación de inmovilizaciones si se precisa, para mantener una correcta alineación de la cadera, así como ejercicios de fisioterapia en agua para tratar de mantener la musculatura sin realizar carga sobre el hueso.
En niños mayores de 12 años o en casos muy evolucionados puede ser necesaria la cirugía de cadera , bien para alargar un tendón, bien para intervenir sobre la pelvis situando de modo correcto la cabeza del fémur sobre el cotilo.
Pruebas complementarias del tratamiento de la enfermedad de Perthes
La prueba complementaria principal será de imagen, una radiografía de ambas caderas y, cuando esta sea normal y haya una alta sospecha de enfermedad, puede ser necesario realizar una resonancia magnética que permitirá ver lesiones más precoces.
Factores de riesgo de la enfermedad de Perthes
Entre los factores de riesgo de la enfermedad de Perthes están el sexo, ya que los niños sufren 4 veces más esta enfermedad que las niñas, la complexión, ya que si los niños son delgados o tienen mucha actividad física también tendrán más posibilidades de sufrirla, y si son más pequeños de lo normal para su edad, lo cual constituye otro factor de riesgo.
Complicaciones de la enfermedad de Perthes
Artrosis de cadera en adultos.
Prótesis de cadera precoz en adultos.
Prevención de la enfermedad de Perthes
Los factores de riesgo de esta enfermedad hacen que no sea prevenible.
Especialidades a las que pertenece la enfermedad de Perthes
El médico implicado en el tratamiento y control de la enfermedad de Perthes será el traumatólogo
Preguntas frecuentes
¿Cuáles son las fases de la enfermedad de Perthes?
Las fases de la enfermedad de Perthes son:
Etapa inicial : se detiene el crecimiento de la cabeza femoral, hay una zona de fractura bajo el cartílago, la cabeza se ve más densa de lo normal y dura unos seis meses.
Etapa de fragmentación : se produce una esclerosis de la cabeza del fémur, hay zonas más claras, el acetábulo se vuelve irregular, y suele durar unos 8 meses.
Etapa de osificación : se comienza a regenerar la cabeza femoral, que comienza a redondearse. Fase que dura unos 12 meses.
Etapa residual : abarca todo el crecimiento del niño, el hueso se remodela a nivel de fémur y del acetábulo.
¿A quién afecta la enfermedad de Perthes?
La enfermedad de Perthes afecta a niños de entre 3 y 12 años , siendo más frecuente en niños que en niñas (afecta a 4 niños por cada niña). La enfermedad deja más secuelas entre los niños más mayores que entre los más pequeños.
¿Qué secuelas tiene la enfermedad de Perthes?
Las secuelas aparecen a largo plazo, pudiendo dar lugar a artrosis y precisar de prótesis de cadera de forma precoz en la edad adulta. Si el niño es mayor y la lesión más lateral y más extensa, es más fácil es que haya secuelas en un futuro.
¿Qué es la enfermedad de Batten?
La enfermedad de Batten es un trastorno del sistema nervioso , que es hereditario y mortal , y cuyos síntomas aparecen entre los 5 y 10 años. El primer síntoma suelen ser convulsiones seguidas de alteración en la visión, se puede producir un deterioro mental y los niños pueden quedar encamados, ciegos y dementes. La mortalidad se suele producir alrededor de los 20 años, se da en 2 de cada 100.000 nacidos vivos, y para padecer esta enfermedad los dos padres deben ser portadores del gen anómalo, el gen afectado es el que produce la CLN3.
¿Qué es la enfermedad de Kohler?
La enfermedad de Kohler es una enfermedad que se produce en niños de entre 3 a 5 años, que suele ser unilateral y se da más en varones. En ella se produce aplanamiento y esclerosis del hueso escafoides , el niño presenta dolor e inflamación en la zona del pie, con mayor dolor a la presión en el arco interno del mismo. Raramente persiste más de dos años, su tratamiento es reposo, alivio del dolor y evitar el peso sobre la zona ósea. El cuadro se resuelve pasado ese tiempo, sin secuelas para el niño.

Enfermedad
Enfermedad de Mano-Pie-Boca
¿Qué es la enfermedad mano-pie-boca?
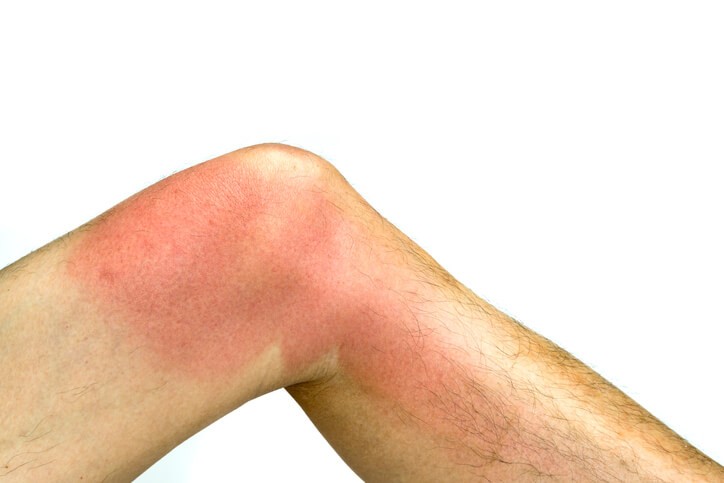
La enfermedad de manos, pies, boca es una infección de origen viral muy contagiosa , generalmente benigna, que es común en la infancia, afecta la cavidad oral y la región distal de las extremidades (manos y pies), que se caracteriza por la presencia de vesículas (pequeñas ampollas llenas de líquido en la piel) y llagas en la boca y una erupción cutánea en las manos y los pies.
Es más frecuentes en niños menores de 10 años, pero puede contagiarse a personas de todas las edades y en ambos sexos. Se extiende fácilmente a través del contacto con manos no lavadas, heces, saliva, mocos o el líquido de las ampollas . Su incidencia es mayor en los sitios donde hay poca higiene y sobrepoblación, normalmente se da en guarderías, centros de preescolar y otros lugares donde los niños comparten espacios reducidos y tienen contacto con objetos contaminados. Suele aparecer en los meses de verano y otoño y puede afectar a varios miembros de la familia. Es una enfermedad leve muy común, que desaparece espontáneamente después de algunos días.
Tipos de enfermedad mano-pie-boca
No se conocen tipos de la enfermedad mano pie boca.
Causas de la enfermedad mano-pie-boca
La causa más frecuente de la enfermedad de manos, pies y boca es la infección con el coxsackievirus A16, que pertenece al grupo de los enterovirus no polio. También existen otros tipos de enterovirus que lo pueden causar, lo que quiere decir que puede volver a repetirse.
Su transmisión es fundamentalmente fecal-oral , la ingestión oral es la principal fuente de infección por el coxsackievirus. La enfermedad se propaga por el contacto de persona a persona a través de los fluidos como: saliva, fluidos de las ampollas, heces, secreciones nasales y descargas de la garganta . También es posible que se transmitan con el contacto de objetos contaminados de los enfermos.
Síntomas de la enfermedad mano-pie-boca
La enfermedad mano pie boca tiene un periodo de incubación de 3 a 7 días , los síntomas que puede causar son: fiebre, dolor de garganta, cefalea, dolor abdominal, pérdida de apetito , lesiones dolorosas vesiculares (ampollas), de color rojo en la lengua, las encías y la cara interna de las mejillas, erupciones con ampollas pequeñas en las manos, los pies y en la zona donde se coloca el pañal que pueden estar sensibles o causar dolor si se presionan e irritabilidad en bebés y niños pequeños.
Tratamiento para la enfermedad-mano-pie-boca
No existe un tratamiento específico para la enfermedad de manos, pies y boca. Por lo general, los signos y síntomas duran entre siete y diez días. Para tratar los síntomas usan analgésicos-antitérmicos como paracetamol o ibuprofeno, para controlar la fiebre, el dolor y el malestar general causado por la enfermedad. También la hidratación, la ingesta de líquido es muy importante para evitar complicaciones. Un anestésico oral tópico puede ayudar a aliviar el dolor de las llagas en la boca.
Pruebas complementarias del tratamiento de la enfermedad mano-pie-boca
Para el diagnóstico y tratamiento se realiza un examen físico . Normalmente, se puede emitir sólo con los síntomas ya que son muy característicos, con solo ver las lesiones en la piel, ampollas y erosiones en las manos, los pies y la boca.
Factores desencadenantes de la enfermedad mano-pie-boca
El factor desencadenante principal de la enfermedad mano pie boca es el contacto con el virus coxsackievirus A16.
Factores de riesgo de la enfermedad mano-pie-boca
Los factores que aumentan el riesgo de la enfermedad mano pie boca incluyen:
La edad: la enfermedad de manos, pies y boca afecta principalmente a niños de menos de 10 años, principalmente niños menores de 5 años y lactantes.
Factor ambiental: los niños que se encuentran en centros de cuidado infantil son particularmente propensos a los brotes de la enfermedad de manos, pies y boca, debido a la propagación de infecciones en el contacto de persona a persona, y los niños pequeños son los más vulnerables.
Complicaciones de la enfermedad mano-pie-boca
La complicación más frecuente de la enfermedad de manos, pies y boca es:
La deshidratación: la enfermedad puede causar llagas en la boca y en la garganta, lo que produce dolor y dificultad para tragar.
Convulsiones.
Las complicaciones graves son poco frecuentes como son:
Onicomadesis: caídas de las uñas de las manos y los pies.
Encefalitis.
Meningitis aséptica.
Prevención de la enfermedad mano-pie-boca
Para prevenir la enfermedad mano pie boca es necesario:
Lavarse las manos frecuentemente con agua y jabón, en especial después de ir al baño o cambiar un pañal y antes de preparar alimentos y comer.
Desinfectar las áreas comunes.
Aislar a las personas que se puedan contagiar.
Evitar el contacto con personas que tengan esta enfermedad.
Especialidades a las que pertenece la enfermedad mano-pie-boca
La especialidad a la que pertenece la enfermedad mano pie boca es pediatría, la que se ocupa del estudio del crecimiento y el desarrollo de los niños hasta la adolescencia, así como del tratamiento de sus enfermedades.
Preguntas frecuentes
¿Cómo se contagia el virus mano-pie-boca?
Se contagia de persona a persona y se extiende fácilmente a través del contacto con manos no lavadas, heces, saliva, mocos o el líquido de las ampollas.
¿Cuánto tiempo dura la enfermedad mano-pie-boca?
La enfermedad mano pie boca dura de 3 a 7 días.
¿Qué es la enfermedad del beso?
La mononucleosis infecciosa o también conocida como la enfermedad del beso está provocada por un virus que se transmite a través de la saliva , se puede contraer al besar a alguien, aunque también cuando se queda expuesto a alguien que tose o estornuda, o al compartir un vaso o utensilio con alguien que tiene mononucleosis.
¿Qué es escarlatina infantil?
La escarlatina en niños, es una enfermedad exantemática causada por una bacteria , el estreptococo beta-hemolítico del grupo A, perteneciente a la misma familia que los gérmenes responsables de la amigdalitis. La bacteria se difunde a través del contacto directo con el moco o la saliva del niño infectado, con la saliva que se expulsa con la tos, con los estornudos o simplemente hablando, y penetra en el organismo a través de las mucosas de la nariz y de la boca.
¿Qué es un exantema viral?
El exantema vírico es una enfermedad producida por un virus que se manifiesta principalmente como una erupción rosacea en la piel . Es una enfermedad de carácter leve, provocada por un tipo de virus del herpes humano que provoca fiebre y erupciones similares a las del sarampión y la rubéola.
Enfermedad
Eritema Nodoso
¿Qué es un eritema nodoso?
El eritema nodoso constituye la forma de paniculitis más frecuente, es decir, aparición de nódulos inflamatorios redondeados que afectan al tejido celular subcutáneo , sobre todo en la región inferior de las piernas. Puede aparecer a cualquier edad de la vida, aunque tiene mayor prevalencia en adultos de 20-50 años, sobre todo en mujeres o en niños y a partir de los dos años en ambos sexos. La gravedad del proceso dependerá de si existe una enfermedad subyacente que lo produce y la importancia y posible evolución de la misma.
Tipos de eritema nodoso
Los tipos de eritemas nodosos son:
Eritema nodoso primario o idiopático : cuando no existe una enfermedad de base que lo origine.
Eritema nodoso secundario : cuando existe una patología que justifica su aparición.
Además, existen dos entidades consideradas variantes de la misma enfermedad (basadas en diferencias clínicas y de la alteración del tejido):
Eritema nodoso migrans : aparecen lesiones de localización asimétrica y que tienen una evolución más lenta.
Eritema nodoso crónico : las lesiones persisten meses o años de forma asintomática.
Causas del eritema nodoso
En la mitad de los casos no se encuentra una causa subyacente que justifique la aparición del eritema nodoso.
Dentro de las causas más frecuentes que pueden producir esta lesión dérmica están infecciones bacterianas o víricas (por Estreptococos, Tuberculosis, Salmonela, Herpes virus, virus de Epstein Barr… etc . ) también la Sarcoidosis , toma de medicamentos como anticonceptivos orales, salicilatos, antibióticos ( Cefalosporinas, Penicilinas, Tetraciclinas, Estreptomicina, Cotrimoxazol ), o el embarazo.
Otras enfermedades que de forma más infrecuente pueden producir el eritema nodoso son patologías de base inmunológica como la enfermedad de BeÇhet, enfermedad inflamatoria intestinal o el lupus eritematoso sistémico. Además, tumores como linfomas o leucemias de forma rara también lo pueden producir.
Síntomas del eritema nodoso
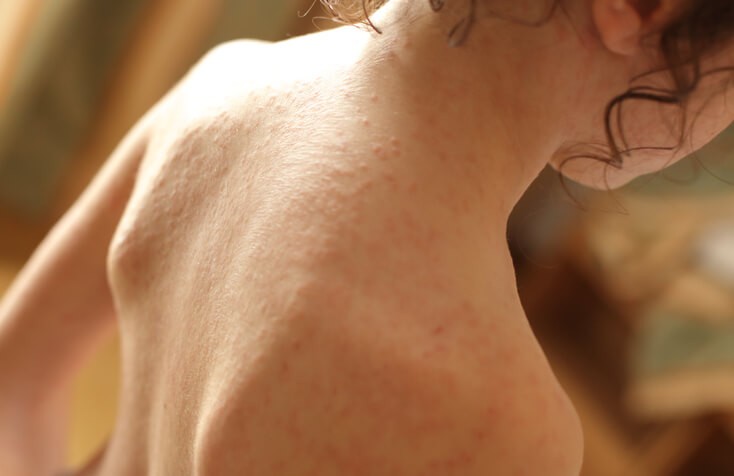
Aparecen de forma brusca lesiones redondeadas nodulosas , de aproximadamente 2-6 cm, inflamadas, rojas, ligeramente sobreelevadas, calientes y simétricas. Pueden evolucionar hacia una coloración violácea y aparecen de forma más frecuente en la zona anterior de las piernas, (espinillas). Curan en aproximadamente 3-6 semanas sin dejar cicatriz.
En ocasiones se asocia la aparición de fiebre, dolores articulares o inflamación de articulaciones , dolor de cabeza, irritación ocular y aparición de conjuntivitis y cansancio (astenia).
Tratamiento para el eritema nodoso
El tratamiento fundamental se basa en aquel dirigido a la situación causante asociada específica.
El tratamiento sintomático de los nódulos se basa en el reposo relativo, uso de fármacos como antiinflamatorios no esteroideos ( Ibuprofeno , ácido acetilsalicílico ( Aspirina ), Indometacina …etc.) En casos resistentes se puede utilizar yoduro potásico o corticoides sistémicos.
Pruebas complementarias del tratamiento de eritema nodoso
El diagnóstico del eritema nodoso es fundamentalmente clínico. Pueden solicitarse pruebas complementarias para diagnosticar las posibles enfermedades que lo producen:
Analítica de sangre : con determinación de hemograma, bioquímica con perfil hepático y función renal, reactantes de fase aguda como velocidad de sedimentación globular y proteína C reactiva.
Prueba de la tuberculina (Mantoux).
Test de embarazo .
Cultivo de exudado faríngeo (para diagnóstico de infección estreptocócica).
Radiografía de tórax
Factores desencadenantes de un eritema nodoso
El factor que desencadena la aparición del eritema nodoso es la aparición de una inflamación vascular, salida de glóbulos rojos y acúmulo de glóbulos blancos en el tejido subcutáneo, del que luego deriva la formación de los llamados granulomas, que son la base del nódulo que se forma bajo la piel.
Factores de riesgo del eritema nodoso
El factor de riesgo principal es padecimiento de todas aquellas enfermedades que secundariamente pueden desencadenar su aparición: enfermedades infecciosas bacterianas de vías respiratorias altas, tuberculosis, diarrea por Yersinia enterocolítica… etc. También enfermedades sistémicas como sarcoidosis, toma de medicamentos como sulfamidas, anticonceptivos orales…etc.
Complicaciones del eritema nodoso
Ulceración (en el caso de ser producidos por lepra).
Recurrencia.
Prevención del eritema nodoso
La mejor prevención es el adecuado tratamiento de las enfermedades de base que pueden desencadenar la aparición del eritema nodoso.
En un alto porcentaje esta alteración no se puede prevenir, ya que nunca se encuentra la causa que lo ha ocasionado.
Especialidades a las que pertenece el eritema nodoso
El diagnóstico y tratamiento inicial del eritema nodoso puede llevarse a cabo por el especialista en dermatología. Si existe una enfermedad subyacente se requerirá la intervención del especialista específico según las características de la misma (reumatólogo, especialista en enfermedades infecciosas, especialista en aparato digestivo…etc.)
Preguntas frecuentes:
¿Qué es la paniculitis septal?
La paniculitis septal es un tipo de manifestación de paniculitis en la que aparece una inflamación del tejido celular subcutáneo que respeta los lóbulos de grasa y afecta a las áreas periféricas a estos. Su manifestación típica es el eritema nodoso.
¿Qué es el eritema indurado de Bazin?
El eritema indurado de Bazin se considera un tipo de paniculitis, inflamación del tejido subcutáneo (tejido adiposo o graso debajo de la piel) producida por una alteración vascular inflamatoria (vasculitis ), que puede estar asociado al padecimiento de tuberculosis u otras enfermedades.
¿Qué es la sarcoidosis?
Es una enfermedad sistémica de causa desconocida, con afectación de los ganglios linfáticos y los pulmones sobre todo, como consecuencia de una respuesta inmunológica anómala con la formación de masas llamadas granulomas por acúmulo de células inflamatorias.

Enfermedad
Epididimitis
¿Qué es la epididimitis?
La epididimitis es un proceso inflamatorio o infeccioso del epidídimo, estructura tubular situada en la parte superior y posterior de los testículos donde se almacenan los espermatozoides, que frecuentemente se asocia a la afectación del testículo llamándose entonces orquiepididimitis.
Es el motivo más frecuente de consulta por dolor testicular en el adulto. Es una afectación que aparece en el varón adulto entre los 20 – 50 años de forma más frecuente.
Es una patología de gravedad moderada-grave por las posibles complicaciones que pueden desencadenarse con su padecimiento si no se trata o no evoluciona adecuadamente.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tipos de epididimitis
La epididimitis se clasifica según su curso evolutivo en agudas , con aparición evolución gradual en 1 – 2 días y no más de 6 semanas, o crónicas, persistente en el tiempo más de tres meses. También se clasifican según su orígen, por ser infecciosas (originadas por un germen) o por una inflamación sin patología infecciosa asociada.
Causas de la epididimitis
Causa infecciosa: En el varón sexualmente activo predominan organismos causantes de enfermedades de transmisión sexual ( chlamydia trachomatis ). En el anciano y el niño la bacteria más frecuentemente implicada es la echerichia coli. Algunas de las epididimitis crónicas son producidas por micobacteria tubercolusosis o la brucella sp.
Causa no infecciosa: Consumo del fármaco antiarrítmico amiodarona, padecimiento de enfermedades sistémicas como la enfermedad de BechÇhet (enfermedad reumática con inflamación de los vasos sanguíneos), por traumatismos o por lesiones después de cirugías como la vasectomía. También puede producirse por la irritación producida por reflujo de orina desde la uretra hasta el epidídimo.
Síntomas de la epididimitis
La epididimitis cursa con afectación normalmente unilateral (uno de los epidídimos) que produce dolor en el escroto , que en ocasiones se irradia hacia la ingle, febrícula o fiebre. Aparecen molestias uretrales y enrojecimiento o edema del escroto, a veces también hidrocele (acumulación de líquido en el escroto).
En los varones sexualemnte activos pueden coexistir síntomas de enfermedades de transmisión sexual (ETS), mientras que en los niños y ancianos suele haber una afectación genitourinaria previa (infecciones urinarias, prostatitis o sondaje urinario previo).
Las epididimitis crónicas pueden presentarse con escasos síntomas, manifestándose como un aumento del tamaño de la glándula que aparece indurada (endurecida). En ocasiones también aparece dolor y fiebre. Cuando la causa es una infección tuberculosa, es frecuente que se cronifique y que aparezca inflamación del escroto y edema y presencia de una fístula (comunicación anormal hacia el exterior de la piel).
Tratamiento para la epididimitis
Se recomienda el reposo con sujeción y elevación testicular . Se pautan tratamientos farmacológicos para controlar el dolor y la inflamación ( analéticos y antiinflamatorios ). En ocasiones, se puede pautar tratamiento con corticoides en dosis descendentes con el fin de evitar la obstrucción de los conductos del epidídimo (aunque su eficacia no está 100% demostrada).
En aquellos casos de origen infeccioso se establece tratamiento con antibiótico que se inicia antes de tener el resultado de los estudios diagnósticos, según la sospecha del origen de la infección. Se confirma con los cultivos realizados (determinación de la bacteria causante de la infección).
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Pruebas complementarias del tratamiento de la epididimitis
El diagnóstico se realiza principalmente por la clínica que presenta el paciente y la exploración física . Además, se pueden realizar pruebas diagnósticas para confirmar la causa como analítica de sangre, análisis de orina, cultivo de orina y del exudado uretral.
En aquellos casos en los que los cultivos son negativos, existe una mala evolución o una presentación crónica de la enfermedad, o si existen dudas diagnósticas para diferenciarlo con otras patologías como la torsión testicular, se realiza una ecografía doppler (prueba de imagen que valora el flujo sanguíneo).
Factores desencadenantes de la epididimitis
Los factores que desencadenan la epididimitis son las enfermedades de transmisión sexual y las patologías urológicas.
Factores de riesgo de la epididimitis
Los varones sexualmente activos que tiene múltiples parejas sexuales y no usan métodos de protección para evitar las enfermedades de transmisión sexual (preservativo), tienen mayor riesgo de padecer epididimitis. En caso de ancianos y niños el padecer alteraciones anatómicas urológicas o ser sometido a procesos invasivos como la introducción de una sonda urinaria, puede desencadenar la inflamación (por reflujo de orina, por ejemplo) o por aparición de una infección.
Por otro lado, realizar actividad física en la bicicleta puede producir traumatismos más importantes o repetitivos, u otro tipo de actividades que impliquen un sedentarismo importante (estar sentado durante largos periodos de tiempo).
Complicaciones de la epididimitis
Producción de un absceso (colección localizada y acúmulo de materia infecciosa con pus)
Infarto testicular (interrupción del flujo sanguíneo y muerte del tejido)
Dolor crónico
Infertilidad (por obstrucción de los conductos del epidídimo)
Sepsis (extensión de la infección al resto del organismo con una respuesta inflamatoria intensa y mala función multiorgánica)
Prevención de la epididimitis
Utilizar preservativo cuando se mantienen relaciones sexuales
Someterse a tratamiento antibiótico profiláctico indicado por el médico si la pareja presenta algún tipo de enfermedad de transmisión sexual
Mantener una adecuada higiene del área genital
Especialidades a las que pertenece la epididimitis
La epididimitis puede ser diagnosticado y tratado por el médico de atención primaria quien puede objetivar alguna complicación, mala evolución, o presencia de dudas diagnósticas. En este caso, derivará al especialista en urología.
Preguntas frecuentes:
¿Cuánto tiempo tarda en curar la epididimitis?
Dependiendo del origen de la epididimitis, de si existen complicaciones y el éxito del tratamiento, puede durar un par de semanas en los casos agudos. Cuando se cronifica el tiempo de evolución suele ser mayor a 3 meses.
¿Qué es la orquitis?
Es la inflamación aguda o crónica del testículo, habitualmente producida por una infección (por bacterias o virus).
¿Qué es la orquiepididimitis?
Es la asociación de una afectación conjunta del testículo y el epidídimo en la que se produce una inflamación de ambas estructuras anatómicas cuya causa puede ser una infección bacteriana (lo más habitual) o producida por otros patógenos, o no infecciosa (por anomalías anatómicas, traumatismos, etc.)
¿Qué es la torsión testicular?
Es la rotación del cordón espermático (estructura anatómica con forma cilíndrica que contiene vasos sanguíneos y linfáticos y el conducto que lleva los espermatozoides fuera del testículo), con supresión súbita del riego sanguíneo del testículo. Es una emergencia quirúrgica ya que si se mantiene durante más de 4 – 6 horas puede desencadenarse un infarto testicular (muerte del tejido) con pérdida del testículo.
¿Qué es una hernia testicular?
La hernia testicular o mejor denominada hernia inguinoescrotal es la salida de contenido intestinal hacia la bolsa escrotal. Es un tipo de hernia inguinal.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Enfermedad
Escarlatina
¿Qué es la escarlatina?
La escarlatina es una enfermedad producida por una bacteria cuando un paciente sufre amigdalitis estreptocócica , lo que provoca en el paciente una erupción en la piel de color rojo brillante, la cual se presenta en todo el cuerpo. Es también conocida por el nombre de fiebre escarlata , y es más frecuente en niños que en adultos. Se da en pacientes con amigdalitis estreptocócica. Se trata de una enfermedad de tipo leve que pertenece a la especialidad de enfermedades infecciosas.
Tipos de escarlatina
La escarlatina no se divide en diferentes tipos, ya que siempre es provocada por la bacteria Streptococcus del grupo A, conocida comúnmente como bacteria estreptococo.
Causas de la escarlatina
La causa principal por la cual se produce la escarlatina es debido a una infección bacteriana que expulsa una toxina, que a su vez provoca una erupción cutánea de tono rojizo generalizada por todo el cuerpo, así como otros síntomas.
Esta bacteria es la misma que provoca la amigdalitis estreptocócica.
Síntomas de la escarlatina
El principal síntoma de la escarlatina es la erupción de color rojo que se manifiesta por todo el cuerpo del paciente, teniendo un aspecto similar a una quemadura por el sol.
Otros síntomas son la llamada lengua de fresa , que provoca que se vea de color rojo e hinchada, con partes blancas. También se producen manchas en la cara marcando la zona de los labios con un anillo blanco.
El resto de síntomas destacados son fiebre, dolor de garganta, ganglios inflamados o dolores de cabeza, entre otros.
Tratamiento para la escarlatina
Al tratarse de una enfermedad bacteriana, el paciente será tratado con antibióticos para eliminar la infección, siendo muy importante completar el periodo indicado de toma del antibiótico para evitar que haya complicaciones por no eliminarse correctamente la bacteria.
También pueden recetarse al paciente cremas o medicamentos concretos para aplicar sobre las erupciones cutáneas y aliviar los síntomas, así como analgésicos para la fiebre y los dolores.
Pruebas complementarias del tratamiento de escarlatina
Para determinar si el paciente sufre escarlatina lo primero es realizar un examen físico , donde se le visualiza la garganta y las amígdalas.
Después, se evalúa si existe inflamación en los ganglios de la zona de la garganta, y por último se analizan las manchas rojizas de la piel por la erupción cutánea.
En algunos casos, el médico puede extraer una muestra de la parte de la faringe para realizar una analítica y ver si existe la presencia de las bacterias estreptocócicas.
Factores desencadenantes de la escarlatina
El principal factor desencadenante de la escarlatina o fiebre escarlata es la amigdalitis estreptocócica.
Factores de riesgo de la escarlatina
Esta enfermedad es más frecuente en niños que en adultos, sobre todo en edades comprendidas entre los 5 y los 15 años.
Al transmitirse por fluidos como la saliva, hay más riesgo de contagio entre familiares y amigos.
Complicaciones de la escarlatina
Fiebre reumática.
Infección de la bacteria en la piel, sangre, riñones… etc.
Anomalías en el sistema nervioso y articulaciones.
Prevención de la escarlatina
Mantener una correcta higiene, sobre todo lavando las manos antes de ingerir alimentos.
Evitar el uso compartido de cubiertos y/o alimentos.
Al toser o estornudar taparse la nariz y la boca.
Esterilizar los juguetes infantiles.
Especialidades a las que pertenece la escarlatina
La escarlatina es tratada por médicos de medicina general y los especialistas en enfermedades infecciosas.
Preguntas frecuentes
¿Es contagiosa la escarlatina?
Sí, se contagia a través de la saliva . Cuando entra en contacto la saliva de un paciente infectado con otra persona.
Desde los primeros síntomas ya se puede contagiar, y no es hasta las 48 horas siguientes de iniciar el tratamiento antibiótico cuando deja de ser una enfermedad infecciosa.
¿Qué personas tienen más riesgo de sufrir escarlatina?
La escarlatina se produce a raíz de una amigdalitis bacteriana que suele ser más frecuente en niños , y en personas que padecen amigdalitis frecuentes.
¿Cuánto tiempo dura la escarlatina?
Desde el contagio hasta que se supera la enfermedad, la escarlatina tiene una duración de entre 15 y 20 días.
¿Cuál es el periodo de incubación de la escarlatina?
El periodo de incubación se da entre los 2 y los 5 días previos a que aparezcan los primeros síntomas.
¿Puede haber escarlatina sin fiebre?
Sí. Aunque la fiebre es un síntoma característico del estreptococo que produce la escarlatina, en algunos casos puede no manifestarse.
Enfermedad
Enfermedad de Crohn
¿Qué es la enfermedad de Crohn?
La enfermedad de Crohn es una inflamación del tubo digestivo , también conocida como inflamación intestinal o síndrome de colon irritable. Se suele dar en pacientes con antecedentes genéticos en esta enfermedad, entre los 30 y los 40 años y pertenece a la especialidad de digestivo, el grado de la patología debe ser determinado por un especialista.
Tipos de enfermedad de Crohn
Existen diferentes tipos de enfermedad de Crohn según la parte del tubo digestivo a la que dañe, las 4 más frecuentes son:
Yeyunoileítis : afecta a la parte superior del intestino delgado, llamado yeyuno.
Ileítis : cuando afecta solo a la zona del íleon, una de las partes finales del intestino.
Ileocolitis : si la inflamación se produce en el colón y el íleon, zona final del intestino delgado.
Colitis de Crohn : solo se inflama el colon.
Causas de la enfermedad de Crohn
No existe una causa concreta conocida por la cual el paciente sufra la enfermedad de Crohn, no obstante, hay dos factores muy importantes:
La herencia genética : la enfermedad de Crohn se transmite por los genes, por lo que si existen antecedentes familiares con esta enfermedad el riesgo de padecerla es mayor.
Anomalías en el sistema inmunitario : en ocasiones el organismo ataca sus propias células, pudiendo atacar las del aparato digestivo.
Síntomas de la enfermedad de Crohn
Los síntomas van en función de cada paciente, pudiendo ser más o menos graves y afectando a una parte solo del intestino o a todo el conjunto.
Los más frecuentes son:
Sangrado en las heces.
Fístulas anales (perforaciones).
Diarrea o estreñimiento.
Dolor abdominal.
Fiebre.
Inflamación del hígado y a veces de otras partes del cuerpo.
Tratamiento para la enfermedad de Crohn
La enfermedad de Crohn suele tratarse con una medicación para reducir la inflamación del aparato digestivo, ya que a día de hoy no hay una cura total y cada paciente requiere una medicación distinta.
La medicación suele establecerse a partir de corticoesteroides para reducir la inflamación, y en algunos casos analgésicos y antibióticos . También hay tratamientos más agresivos, mediante medicamentos que atacan al sistema inmunitario para que no produzcan las sustancia que genera la inflamación.
En un último caso y si es muy grave, se requiere de cirugía , mediante la cual se extrae la parte dañada del aparato digestivo.
Sobre todo, es muy importante que el paciente adquiera unos buenos hábitos nutricionales , para evitar que los dolores y la enfermedad vayan a más.
Pruebas complementarias del tratamiento de la enfermedad de Crohn
La primera prueba a realizar es una exploración física por parte del médico. Después, se realizará una analítica de sangre y otra de heces en búsqueda de anomalías.
Para completar el diagnóstico se observará mediante técnicas de diagnóstico por imagen el interior del tubo digestivo, mediante colonoscopias (se introduce un cable fino y flexible con una cámara en el extremo para observar el interior), ecografía o resonancia magnética, entre otras pruebas similares.
Factores desencadenantes de la enfermedad de Crohn
A pesar de que se desconoce por qué los pacientes padecen la enfermedad de Crohn, hay dos factores que influyen, las anomalías en el sistema inmunitario y la herencia genética.
Pero, además, una mala alimentación y el estrés son dos desencadenantes muy frecuentes en este tipo de enfermedad.
Factores de riesgo de la enfermedad de Crohn
Los factores de riesgo que pueden hacer que las personas tengan mayor predisposición a padecer esta enfermedad son:
La herencia genética, debido a los antecedentes familiares.
La edad, ya que a pesar de que puede darse en cualquier etapa es más frecuente en gente joven.
Origen racial , al igual que con la edad, cualquier persona puede padecerlo, pero son más propensas las personas de raza blanca y con parentesco de origen judío.
Personas fumadoras.
Complicaciones de la enfermedad de Crohn
Fístulas anales.
Fístulas intestinales.
Úlceras.
Obstrucciones intestinales.
Cáncer de colon.
Prevención de la enfermedad de Crohn
No fumar tabaco.
Mantener una dieta equilibrada.
Evitar el estrés.
Acudir a revisiones médicas.
Consultar los antecedentes familiares.
Especialidades a las que pertenece la enfermedad de Crohn
La enfermedad de Crohn debe ser tratada por especialistas del aparato digestivo y/o la especialidad de gastroenterología.
Preguntas frecuentes
¿Qué es el Síndrome de Colon irritable?
Es una variación de la enfermedad de Crohn que afecta a la funcionalidad del colón. Es una enfermedad crónica que provoca molestias abdominales y diarreas o estreñimiento.
Puede controlarse con la medicación apropiada.
¿Qué dieta debo llevar cuando tengo la enfermedad de Crohn?
No es necesario seguir una dieta estricta, pero no se deben tomar alimentos demasiado picantes, con mucha sal o hacer comidas pesadas, y menos por la noche.
Simplemente mantener una dieta sana y equilibrada.
¿Qué es la distensión abdominal?
La distensión abdominal es un ensanchamiento de la zona de la tripa sin motivo aparente y que dura varios días. En el caso de la enfermedad de Crohn se debe a que los cambios en los ritmos intestinales provocan que las heces se acumulen y aumente el abdomen.
¿A quién afecta la enfermedad de Crohn?
No existe un cuadro médico claro sobre a quién puede afectar y a quién no. Sin embargo, tienen más predisposición aquellas personas que tienen antecedentes genéticos o anomalías en su sistema inmunitario.
¿Tiene cura la enfermedad de Crohn y cuál es el pronóstico?
A día de hoy no existe una cura total para la enfermedad de Crohn, pero con un correcto diagnóstico y tratamiento el paciente puede llevar una vida normal.

Enfermedad
Enfermedad de Hirschsprung
¿Qué es la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung, también conocida como megacolon congénito, es la obstrucción congénita del colon producida por alteraciones en la inervación de este, que dan lugar a una falta de relajación del mismo y puede presentarse al nacer o aparecer algo más tarde. Se da entre 1 y 5 de cada 10.000 nacidos vivos y, en el 80% de los casos, el defecto está tan solo en el recto. El 10% de los casos ocupan el recto y el sigma y, por último, el 10% restante altera también el colon. Puede producir una perforación intestinal que precise de cirugía de urgencia, por lo que es considerada una enfermedad de tipo grave.
Tipos de enfermedad de Hirschsprung
Enfermedad de Hirschsprung de segmento ultracorto : ocupa solo el esfínter interno o un pequeño segmento yusta-anal.
Enfermedad de Hirschsprung de segmento corto : no va más allá de unión del recto con el sigma.
Enfermedad de hirschsprung de segmento largo : si la alteración va más allá de la unión del recto con el sigma.
Causas de la enfermedad de Hirschsprung
La causa es la alteración de la inervación del intestino, que da lugar a que no se puedan empujar las heces hacia el exterior al no producirse la relajación del intestino, lo cual da lugar a una obstrucción por detrás de dicho nivel.
Síntomas de la enfermedad de Hirschsprung
El primer síntoma que suele aparecer es la dificultad para expulsar el meconio tras las 24 o 48 horas después del nacimiento. Otros síntomas serán heces explosivas y poco frecuentes, ictericia, falta de apetito, falta de ganancia de peso, vómitos y heces acuosas en los recién nacidos, y, en niños más mayores, puede aparecer falta de apetito, retraso del crecimiento y vientre hinchado.
Tratamiento para la enfermedad de Hirschsprung
Pueden ser necesarios enemas para vaciar el intestino, tras ello, hay que extirpar la parte de intestino anómalo, procediendo a realizar una anastomosis entre la parte sana del colon y el ano. Este procedimiento puede ser bien en un solo acto quirúrgico, bien en dos, siendo necesaria una colostomía (dar salida al recto a través del abdomen) durante un tiempo.
Pruebas complementarias del tratamiento de la enfermedad de Hirschsprung
Las pruebas complementarias serán manometría del ano, pruebas de imagen como radiología simple de abdomen o enema opaco, y además puede ser necesaria una biopsia anal para llegar al diagnóstico correcto.
Factores desencadenantes de la enfermedad de Hirschsprung
El factor desencadenante de la enfermedad de Hirschsprung es la falta de peristaltismo , que es el conjunto de movimientos de contracción del tubo digestivo que permiten la progresión de su contenido desde el estómago hacia el ano. Esto se produce por alteración en la relajación del colon, lo cual da lugar a una obstrucción a este nivel.
Factores de riesgo de la enfermedad de Hirschsprung
Entre los factores de riesgo está el tener un hermano con enfermedad de Hirschsprung , lo cual aumenta el riesgo, también el ser varón, ya que es más frecuente en varones, y padecer síndrome de Down , ya que en niños con esta patología aparece con mayor frecuencia que el resto de la población.
Complicaciones de la enfermedad de Hirschsprung
Enterocolitis (inflamación del intestino delgado y del colon).
Perforación intestinal.
Síndrome del intestino corto (pérdida anatómica o funcional de una parte del intestino delgado que ocasiona un cuadro clínico de graves alteraciones metabólicas y nutricionales).
Especialidades a las que pertenece la enfermedad de Hirschsprung
El niño será diagnosticado en general por un pediatra, y el tratamiento dependerá de un cirujano digestivo
Preguntas frecuentes
¿Debo tomar una dieta especial si tengo la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung no deja prácticamente secuelas tras la cirugía, las personas que la padecen pueden hacer una vida normal con dieta normal. Si el paciente presenta estreñimiento como secuela, deberá realizar una dieta rica en fibra con parte importante de frutas y verduras.
¿A quién afecta la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung afecta sobre todo a niños , dos veces más que a las niñas y, al ser una enfermedad congénita, se halla presente desde el nacimiento aunque en los casos más leves pueden tardar hasta seis meses en diagnosticarse.
¿Es hereditaria la enfermedad de Hirschsprung?
La enfermedad de Hirschsprung puede ser hereditaria, aunque haya casos aislados, también se pueden presentar varios casos en una misma familia. La herencia es compleja ya que se encuentran alteraciones hasta en 11 genes diferentes capaces de producir la enfermedad. Es más frecuente en pacientes con Síndrome de Down.

Enfermedad
Enfermedad de Lyme
¿Qué es la enfermedad de Lyme?
La enfermedad de Lyme es una infección bacteriana producida por la picadura de una garrapata que transmite la bacteria, es también conocida como borreliosis de Lyme o borreliosis. Se transmite por la picadura de una garrapata, sobre todo en países de Europa y Norteamérica, siendo más frecuentes de marzo a noviembre y en zonas boscosas. Pertenece a la especialidad de infectología, y es una enfermedad considerada de tipo leve.
Tipos de enfermedad de Lyme
No existen diferentes tipos de enfermedad de Lyme, pero sí se diferencian 4 tipos de garrapatas que pueden transmitir la enfermedad:
Borrelia afzelii.
Borrelia garinii.
Borrelia burgdorferi.
Borrelia mayonii.
Siendo las dos primeras las que afectan a Europa.
Causas de la enfermedad de Lyme
La enfermedad de Lyme tiene su origen en la picadura de una garrapata portadora de la bacteria Borrelia burgdorferi y Borrelia mayoni.
Estas bacterias entran en el organismo de las personas mediante la picadura de una garrapata, infectando su organismo al llegar la bacteria a la sangre del paciente.
Para que se transmita la bacteria, la garrapata debe estar en el cuerpo del paciente entre uno y dos días.
Síntomas de la enfermedad de Lyme
Tras la picadura de una garrapata es normal que la zona este inflamada y con un bulto rojo. Sin embargo, si días después aparecen estos síntomas el paciente debe acudir al médico:
Eritema migratorio : una erupción cutánea roja que en el centro está de un tono más claro o incluso blanco. Este puede aparecer en más partes del cuerpo.
Fiebre y/o escalofríos .
Malestar general .
Dolor de cabeza y fatiga .
Dolores en las articulaciones .
Alteraciones neurológicas .
Los dos últimos síntomas se dan en situaciones más graves, cuando la enfermedad está más avanzada y puede provocar mayores daños en la salud del paciente. Por ello es importante acudir al médico ante la presencia de los primeros síntomas.
Tratamiento para la enfermedad de Lyme
El principal tratamiento para hacer frente a la enfermedad de Lyme está basado en antibióticos , bien por vía oral durante unos 15 días aproximadamente, bien por vía intravenosa si la enfermedad afecta a la parte del sistema nervioso central.
Pruebas complementarias del tratamiento de la enfermedad de Lyme
Para detectar la enfermedad de Lyme se realiza primeramente una exploración física del paciente, observando si existe la presencia de eritemas migratorios, ya que estos son muy distintivos.
Otras dos pruebas a realizar son la enzimoinmunoanálisis de adsorción , por la cual se detecta si existen anticuerpos para la bacteria. En caso de dar positivo se realiza una segunda prueba para confirmar, llamada inmunotransferencia, y que detecta en este caso la existencia de proteínas contra la bacteria.
Factores desencadenantes de la enfermedad de Lyme
El principal factor desencadenante de esta enfermedad es la picadura de una garrapata.
No obstante, el no protegerse con la ropa adecuada en zonas donde estos insectos son abundantes o revisar a nuestras mascotas y jardines ante la búsqueda de su presencia, también pueden provocar que la contraigamos. Por lo que la prevención es muy importante en este caso.
Factores de riesgo de la enfermedad de Lyme
Existen diversos factores por los cuales puede incrementar el riesgo de contraer la enfermedad de Lyme:
Ir descalzo por zonas de pastos altos.
No revisar que las mascotas tengan garrapatas.
Estar al aire libre en zonas de jardín donde hayan garrapatas sin protección.
Complicaciones de la enfermedad de Lyme
Problemas cardíacos.
Alteraciones de los procesos cognitivos.
Parálisis.
Hinchazón de por vida de las articulaciones del cuerpo.
Neuropatías.
Prevención de la enfermedad de Lyme
Retirar cuanto antes la garrapata del cuerpo.
Revisar a las mascotas por si tienen alguna y, en caso de ser así, retirarlas.
Emplear repelentes en ropa y cuerpo.
Usar la ropa adecuada si se va a zonas de montaña o bosques para cubrir el cuerpo.
Mantener el jardín libre de garrapatas con insecticidas.
Especialidades a las que pertenece la enfermedad de Lyme
Es una enfermedad tratada por la medicina general y la especialidad de infectología.
Preguntas frecuentes
¿Cuál es el riesgo de contraer la enfermedad de Lyme?
El riesgo de contraer la enfermedad de Lyme tras una picadura de garrapata es de entre un 1% y un 3% , por lo que es un nivel de riesgo muy bajo.
¿Tiene cura la enfermedad de Lyme?
Si se diagnostica en las primeras etapas la enfermedad de Lyme es curable, y si los síntomas son más graves como dolores articulares, del sistema nervioso o el corazón, estos pueden quedarse crónicos, aunque en pocos casos sucede.
¿En qué parte del cuerpo es más probable que me pique una garrapata?
Suelen picar en las orejas, axilas, piernas y brazos.
¿Qué médico trata la enfermedad de Lyme?
El especialista en infectología y los médicos de medicina general o especialistas según el avance de la enfermedad.
¿Cuáles son las consecuencias de tener la enfermedad de Lyme?
Si padeces la enfermedad de Lyme deberás mantener un tratamiento a base de antibióticos durante 15 ó 20 días para eliminar la bacteria que la provoca del organismo.
Si no se trata la enfermedad, las consecuencias se agravarán, pudiendo provocar síntomas más graves como dolores articulares crónicos o problemas neurológicos.

Enfermedad
Endometriosis
Actualizado el 17/09/2021
La endometriosis es una enfermedad inflamatoria crónica que, debido a la amplia variedad de síntomas que provoca no resulta fácil de diagnosticar. Está asociada al dolor pélvico, que afecta en gran medida la calidad de vida de las pacientes. Otra de las características principales es la elevada tasa de infertilidad entre las mujeres que padecen endometriosis.
¿Qué es la endometriosis?
La endometriosis es una enfermedad caracterizada por el crecimiento de un tejido similar al revestimiento del útero o endometrio fuera de él, lo que puede provocar dolor e infertilidad. Provoca una reacción inflamatoria crónica que puede determinar la aparición de tejido cicatricial y fibrosis dentro de la pelvis y otras partes del cuerpo.
La endometriosis afecta al 10-15% de las mujeres en edad reproductiva y no está fuera de lo habitual que transcurra mucho tiempo entre la aparición de los síntomas y el diagnóstico. En el caso de mujeres con problemas de infertilidad o dolor pélvico crónico el porcentaje de mujeres con endometriosis puede llegar al 50%.
En la actualidad, no existe ningún tratamiento efectivo para curar la endometriosis, por lo que el objetivo es el control de los síntomas.
Tipos de endometriosis
En función de las diferentes lesiones que provoca la enfermedad se pueden diferencian distintos tipos de endometriosis:
Endometriosis superficial . Cuando las lesiones aparecen, principalmente, en el peritoneo de la pelvis.
Endometriosis quística . Cuando se producen quistes en el ovario (endometriomas).
Endometriosis profunda . Cuando las lesiones se producen en el tabique rectovaginal, la vejiga, los uréteres y el intestino.
También se pueden producir lesiones de endometriosis fuera de la pelvis (en la pleura, el diafragma o el ombligo), aunque es poco frecuente.
Causas
La endometriosis es una enfermedad compleja en la que inciden múltiples factores. Algunas situaciones que se apuntan como posibles causas incluyen:
Alteraciones del sistema inmunitario . Las células defensivas no reconocen las propias células endometriales y las atacan.
Exceso de estrógenos , que transforman las células embrionarias en endometriales.
Menstruación retrógrada . La sangre menstrual que lleva las células endometriales regresa a las trompas de Falopio en lugar de salir al exterior por la vagina. Como resultado, pueden depositarse células similares a las del endometrio fuera del útero, donde pueden implantarse y crecer.
Metaplasia celular . Es un proceso por el cual las células adoptan una forma distinta. Algunas células situadas fuera del útero se transforman en células similares al endometrio y comienzan a crecer.
Proliferación de células precursoras . Estas dan lugar a la enfermedad, que luego se propaga a través de los vasos sanguíneos y linfáticos.
Otros factores que pueden favorecer la aparición de las lesiones características de la endometriosis incluyen trastornos hormonales, factores genéticos y contaminantes ambientales.
Síntomas
Los síntomas de la endometriosis son muy variados. Suele cursar con fuertes dolores en la zona pélvica, sobre todo en fechas próximas o durante la menstruación.
Otros síntomas frecuentes incluyen sangrados muy abundantes durante el periodo, prácticas sexuales dolorosas, dolor al defecar y al orinar, dolor abdominal y de espalda, náuseas, diarrea, dolores y calambres pélvicos e infertilidad.
Los síntomas suelen mejorar después de la menopausia, pero en algunos casos el dolor puede persistir.
Por otro lado, no hay que olvidar que un porcentaje elevado de mujeres con endometriosis (entre el 15 y el 30%) son asintomáticas.
Tratamiento
La enfermedad no tiene cura. Sin embargo, posibilitar el conocimiento, diagnóstico y tratamiento tempranos podría ralentizar su evolución natural y reducir los síntomas a largo plazo.
En función de los síntomas y lesiones que presente la paciente el tratamiento puede ser farmacológico o quirúrgico. Los tratamientos más habituales incluyen los esteroides anticonceptivos, los antiinflamatorios no esteroideos y los analgésicos.
Los analgésicos son el primer recurso para minimizar el dolor. Si existe un desequilibrio en los niveles de estrógenos, se puede iniciar una terapia hormonal para reducirlos o aumentar los de progesterona. Algunos de estos tratamientos farmacológicos incluyen la píldora anticonceptiva oral combinada, los progestágenos y los análogos de la GnRH.
Sin embargo, ninguno de estos tratamientos elimina la enfermedad y suelen provocar efectos secundarios. Además, los síntomas de la endometriosis pueden reaparecer tras la interrupción del tratamiento.
Como última opción se puede llevar a cabo una intervención quirúrgica, bien por laparoscopia o bien una histerectomía. El tratamiento quirúrgico puede eliminar las lesiones, las adherencias y el tejido cicatricial de la endometriosis.
En cuanto a las opciones de tratamiento para la infertilidad asociada a la endometriosis se incluyen la extirpación quirúrgica laparoscópica de la endometriosis, la estimulación ovárica con inseminación intrauterina y la fecundación in vitro .
Pruebas diagnósticas
Tras analizar el historial clínico, para determinar si la paciente sufre de endometriosis se inicia primero una exploración física de la zona pélvica, donde el médico palpa el abdomen en busca de alteraciones como quistes o cicatrices tras el útero. No obstante, a no ser que los quistes sean de un tamaño considerable, no se detectarán anomalías.
Las siguientes pruebas que se realizan son una ecografía externa o una ecografía transvaginal. En última instancia se puede llevar a cabo una laparoscopia, un procedimiento quirúrgico a través del cual no solo se detecta la endometriosis, si no que se puede comenzar a tratar.
Factores de riesgo de la endometriosis
Existe una serie de circunstancias que se relacionan con un mayor riesgo de que una mujer pueda sufrir endometriosis:
Antecedentes familiares de endometriosis.
Acortamiento del periodo intermenstrual.
Menarquia muy temprana o menopausia tardía.
Un número reducido de hijos.
Nsaludso haber recurrido a la lactancia materna.
Estrés.
El ejercicio físico se asocia inversamente con el riesgo de endometriosis.
Endometriosis y cáncer
El riesgo de cáncer a partir de la endometriosis es muy bajo. En aquellas pacientes con endometriosis ovárica y transformación a un cáncer ovárico , el tipo de tumor frecuentemente encontrado es el carcinoma de células claras y el endometrioide.
Por otro lado, la endometriosis y el cáncer de ovario comparten factores de riesgo (por ejemplo, menarquia temprana, ovulación y menstruación incesantes y estrés crónico) y factores protectores (por ejemplo, la ligadura de trompas, la histerectomía y la actividad física).
Prevención
Dadas las características complejas de la endometriosis es complicado establecer medidas de prevención.
En cualquier caso, es recomendable tener presente los factores de riesgo, reparar en los síntomas más característicos de la enfermedad y realizar revisiones ginecológicas periódicas.
Si tienes dudas puedes chatear con un especialista en ginecología ahora.
Preguntas frecuentes
¿Qué es el endometrio o tejido endometrial?
El endometrio es el tejido mucoso que recubre el interior del útero. En él se implantará el óvulo fecundado y dará lugar a la placenta. Si no se produce el embarazo, el endometrio será expulsado con la menstruación.
¿Qué es la endometriosis ovárica?
La endometriosis ovárica se produce cuando el endometrio crece en los ovarios, formándose quistes de tipo benigno.
¿Qué es la adenomiosis?
La adenomiosis se produce cuando el endometrio se desarrolla e invade la capa muscular del útero (miometrio). Puede tener lugar por sí misma o junto con la endometriosis. Los síntomas son muy parecidos entre las dos enfermedades, aunque es importante diagnosticar bien la patología de cara a seleccionar el tratamiento óptimo.
¿Cómo se llama la operación de endometriosis?
En un primer momento la endometriosis se opera a través de una laparoscopia, por la cual se extraen los quistes o se realiza una limpieza uterina.
En algunos casos más graves se necesita extraer el útero. Si la extracción se realiza por la vagina recibe el nombre de histerectomía vaginal, y en caso de ser necesario extirpar los ovarios y las trompas de Falopio, la operación recibe el nombre de salpingo-ooforectomía .
¿Qué pasa si no se trata la endometriosis?
La progresión de las lesiones que causa la endometriosis es variable, pudiendo permanecer sin grandes cambios o extenderse por otros tejidos. En cualquier caso, es importante establecer el tratamiento más adecuado en cada caso.
¿Qué es la hiperplasia endometrial?
La hiperplasia endometrial consiste en un aumento del grosor del útero al haber un incremento de las glándulas endometriales por el exceso de estrógenos.
En algunos casos puede desencadenar en un cáncer de endometrio, pero generalmente los quistes son benignos. Se dan más frecuentemente en mujeres que se están acercando a la menopausia o en las que comienzan a tener sus primeras menstruaciones.
Bibliografía
Organización Mundial de la Salud. Endometriosis. 2021 .
Sociedad Española de Medicina Interna. Endometriosis. Consultado: 06/09/2021 .
Ministerio de Sanidad. Guía de atención a las mujeres con endometriosis en el Sistema Nacional de Salud (SNS). 2013 .
Chapron C, Marcellin L, Borghese B, Santulli P. Rethinking mechanisms, diagnosis and management of endometriosis. Nat Rev Endocrinol 2019; 15(11): 666-682. Doi: 10.1038/s41574-019-0245-z .

Enfermedad
Enfermedad de Kawasaki
¿Qué es la enfermedad de Kawasaki?
La enfermedad de Kawasaki también conocida como síndrome mucocutáneo ganglionar, es una vasculitis aguda (inflamación aguda de los vasos sanguíneos), multisistémica auto limitada y febril casi exclusiva de lactantes y niños . Es una enfermedad que afecta a la piel, la boca y los ganglios linfáticos.
Produce la inflamación de las paredes de las arterias medianas de todo el organismo y tiende a afectar las arterias coronarias que suministran sangre al músculo cardíaco. Afecta, principalmente, a los niños menores de 5 años. Es más frecuente en niños con antepasados de origen japonés o coreano , aunque se puede dar en todos los grupos étnicos. Predomina más en el sexo masculino y es la mayor causa de anomalías cardiacas adquirida en los países occidentales. Esta enfermedad es poco común, rara para esta época y potencialmente mortal para los niños.
Tipos de enfermedad de Kawasaki
No han identificado tipos de la enfermedad de Kawasaki.
Causas de la enfermedad de Kawasaki
La enfermedad de Kawasaki, es todavía desconocida para la ciencia, aunque fue descubierta hace 40 años no se ha encontrado ninguna causa específica que la produce. Se sospecha de una respuesta inmunológica inducida por cualquier agente infeccioso o un superantígeno bacteriano en niños genéticamente susceptibles.
Síntomas de la enfermedad de Kawasaki
Los síntomas de la enfermedad de Kawasaki incluyen:
Fiebre que frecuentemente es superior a los (39°C) y dura más de tres días.
Ojos demasiado inyectados de sangre o rojos (sin pus ni supuración).
Una erupción en la parte principal del cuerpo (tronco) y en la zona genital, sin apariencia de ampollas.
Labios rojos brillantes , con hendiduras o agrietados.
Mucosas rojas en la boca.
Ganglios linfáticos del cuello y quizá de otra zona, inflamados.
Palmas de las manos y plantas de los pies rojas e hinchadas.
Irritabilidad.
Inflamación y dolor articular , con frecuencia en ambos lados del cuerpo.
Diarrea, vómitos y dolor abdominal. Entre otros síntomas.
Tratamiento para la enfermedad de Kawasaki
El tratamiento debe iniciarse lo antes posible tras la aparición de la fiebre. Los objetivos del tratamiento inicial son bajar la fiebre, la inflamación y prevenir el daño cardíaco.
Generalmente, el tratamiento consiste en administrar gammaglobulinas G no modificadas (anticuerpos purificados) por vía intravenosa. Las gammaglobulinas son un componente de la sangre que ayuda a luchar contra las infecciones. Las dosis altas de aspirina pueden ayudar a tratar la inflamación.
La aspirina también puede aliviar el dolor y la inflamación articular y también reducir la fiebre.
El tratamiento de Kawasaki es una excepción rara a la norma de no administrar aspirina a los niños. Una vez que no haya más fiebre, es posible que el niño necesite tomar una dosis baja de aspirina durante al menos seis semanas o más.
Pruebas complementarias del tratamiento de la enfermedad de Kawasaki
No existe una prueba específica disponible para el diagnóstico y tratamiento de la enfermedad de Kawasaki. Pero sí algunas pruebas que pueden ayudar a diagnosticarla como son: análisis de orina, análisis de sangre, radiografía de tórax y cuello, ecocardiograma y electrocardiograma.
Factores desencadenantes de la enfermedad de Kawasaki
No se conocen factores desencadenantes de la enfermedad de Kawasaki.
Factores de riesgo de la enfermedad de Kawasaki
Los factores de riesgo de la enfermedad de Kawasaki incluyen:
La edad: Los niños menores de 5 años tienen más riesgo de contraer la enfermedad de Kawasaki.
El origen étnico: Los niños de ascendencia asiática o de las Islas del Pacífico, como los japoneses o coreanos, tienen niveles más altos de enfermedad de Kawasaki.
El sexo: Los niños tienen un poco más de posibilidades que las niñas de contraer la enfermedad de Kawasaki.
Complicaciones de la enfermedad de Kawasaki
Las complicaciones de la enfermedad de Kawasaki incluyen:
Aneurisma en las arterias coronarias.
Inflamación de los vasos sanguíneos, generalmente de las arterias coronarias que suministran sangre al corazón.
Problemas de válvula cardíaca.
Inflamación del músculo cardíaco (miocarditis).
Ataque cardíaco.
Prevención de la enfermedad de Kawasaki
La enfermedad de Kawasaki no se puede prevenir ya que no se conoce su causa.
Especialidades a las que pertenece la enfermedad de Kawasaki
La enfermedad de Kawasaki pertenece a la especialidad de cardiología pediátrica. La cardiología pediátrica se dedica al estudio, diagnóstico y tratamiento de las enfermedades del corazón en los niños.
Preguntas frecuentes:
¿Cómo se transmite la enfermedad de Kawasaki?
No se conocen formas de transmisión de la enfermedad de Kawasaki.
¿Es curable la enfermedad de Kawasaki?
Si, la enfermedad de Kawasaki es totalmente curable.
¿Cuales son las secuelas de la enfermedad de Kawasaki?
Las secuelas de la enfermedad de Kawasaki incluyen: arritmias (cambios en el latido cardíaco) y se pueden producir anomalías en el funcionamiento de algunas válvulas cardíacas.

Enfermedad
Encefalitis
¿Qué es la encefalitis?
La encefalitis es una enfermedad que da nombre a la inflamación del cerebro producida por una infección en el cuerpo del paciente. Es también conocida como inflamación cerebral o del cerebro, y suele ser producida por un virus. Además, está influenciada por diferentes factores como el clima, la zona geográfica y la vacunación, entre otros. Se trata de una enfermedad de la especialidad de neurología pero de carácter leve.
Tipos de encefalitis
La encefalitis es considerada como un síntoma que indica la presencia de otras enfermedades en el paciente, clasificándose en dos tipos:
Directa : en este caso el virus ha infectado directamente al cerebro, estando en una zona de él o más extendido. En muchas ocasiones se produce tras haber superado una enfermedad, indicando que el virus se ha vuelto a activar.
Indirecta : la encefalitis también puede ser un indicativo de que un virus ha infectado el cuerpo del paciente, y se produce como respuesta del sistema inmunitario para darlo a conocer, manifestándose incluso 3 semanas después de haber adquirido la infección.
Causas de la encefalitis
Generalmente se desconoce el foco por el cual el paciente ha desarrollado la encefalitis, pero en el 80% de los casos, proceden de una infección vírica.
Se puede transmitir vía fecal-oral, vía respiratoria o por transmisión sexual .
Síntomas de la encefalitis
Los síntomas de la encefalitis son generalmente leves, basándose en dolores de cabeza, fiebre, dolores musculares y fatiga , provocando un malestar general al paciente.
No obstante, en muchas ocasiones los síntomas pueden agravarse produciendo en el paciente temblores, alucinaciones, parálisis en zonas del cuerpo, náuseas e incluso convulsiones y pérdida del conocimiento.
Tratamiento para la encefalitis
Si la encefalitis no presenta gravedad, el paciente deberá mantener reposo absoluto, ingerir abundantes líquidos (sobre todo agua), y tomar antiinflamatorios para reducir la inflamación, los dolores y la fiebre.
En caso de que la encefalitis sea más grave,el paciente debe tomar antivirales para hacer frente al virus y poder recuperarse.
Pruebas complementarias del tratamiento para la encefalitis
De cara a iniciar el tratamiento para la encefalitis es necesario realizar una resonancia magnética (diagnóstico por imagen) de la cabeza del paciente, un encefalograma (registro de la actividad del cerebro mediante electrodos), y una analítica de sangre.
En caso necesario, si el paciente no responde al tratamiento y/o los síntomas empeoran, se pueden realizar también una punción lumbar de la médula espinar (extracción de líquido cefalorraquídeo para analizarlo), y una biopsia cerebral (extracción de una muestra de tejido del cerebro).
Factores desencadenantes de la encefalitis
La encefalitis suele estar producida por un virus y en algunos casos por bacterias.
Los principales virus por los que se transmite la encefalitis son el enterovirus, el virus del herpes, y virus transmitidos por las garrapatas o los mosquitos.
Factores de riesgo de la encefalitis
Los principales factores por los cuales la encefalitis puede pasar de ser leve a grave son:
La edad : la encefalitis puede desarrollarse provocando mayor gravedad en niños y en personas mayores.
El motivo de la infección : la encefalitis viral es menos grave que la vírica.
La salud : si el paciente tiene el sistema inmunológico débil tiene mayor riesgo de que se agrave la encefalitis.
Complicaciones de la encefalitis
En el caso de ser un síntoma de un virus o infección, que se manifieste tarde y la otra enfermedad esté muy avanzada.
Si los medios sanitarios no son correctos y el tratamiento se inicia tarde.
Parálisis corporal y/o cerebral por zonas.
Fatiga, sensación constante de cansancio.
Problemas en la visión, el habla y el oído.
Prevención de la encefalitis
Lavarse las manos antes de las comidas y después de ir al baño.
Cumplir con el calendario de vacunación.
Usar repelente para prevenir las picaduras de mosquitos.
Tener una correcta higiene.
Evitar compartir los cubiertos con otras personas.
Especialidades a las que pertenece la encefalitis
La encefalitis debe ser tratada por los especialistas en neurología y enfermedades infecciosas.
Preguntas frecuentes
¿Cuáles son las secuelas de la encefalitis?
Generalmente si la encefalitis no presenta complicaciones, en dos semanas el paciente estará recuperado sin lesiones.
Pero en algunos casos se produce daño cerebral , lo que puede desencadenar en problemas físicos (limitación de movimiento o parálisis), cognitivos (pérdida de memoria, lenguaje, atención) o emocionales (cambios de personalidad y comportamiento).
¿Es contagiosa la encefalitis?
La encefalitis no es contagiosa, pero el virus que la produce sí puede serlo.
¿Qué significa encefalitis viral?
Que la encefalitis está causada por un virus.
¿Por qué se produce la encefalitis?
Puede ser por la infección directa del cerebro ocasionada por un virus, o como respuesta del sistema inmune al haber un patógeno atacando a otra parte del cuerpo.
¿Cómo se detecta la encefalitis?
Primariamente el paciente presenta un cuadro clínico de dolores de cabeza, musculares y fiebre, e incluso en ocasiones síntomas más graves, como pérdida del conocimiento o convulsiones.
Tras un examen neurológico se realizan diferentes pruebas médicas, como la resonancia magnética, y se estudia el origen de la encefalitis para iniciar cuanto antes el tratamiento.

Enfermedad
Embarazo Ectópico
¿Qué es el embarazo ectópico?
El embarazo ectópico o ectociesis, hace referencia a todo aquel embarazo que anida fuera de la cavidad uterina . La incidencia de los embarazos ectópicos es del 1-2% de todas las gestaciones, observándose un incremento en las últimas décadas debido a la influencia sobre todo, de las técnicas de reproducción asistida y al uso de DIUs (Dispositivo Intra Uterino, que es un método anticonceptivo). Es una alteración grave, ya que puede comportar riesgos para la paciente y complicaciones importantes si no es diagnosticado y tratado a tiempo .
Tipos de embarazos
Según la localización pueden aparecer:
Embarazo ectópico en la trompa de Falopio (lo más frecuente).
Embarazo ectópico en el ovario.
Embarazo ectópico en el cuello del útero.
Embarazo ectópico en el abdomen.
Causas del embarazo ectópico
En ocasiones no se aprecia una causa aparente previa que haya desencadenado la anidación anómala del óvulo fecundado. En otras muchas circunstancias, la causa es una alteración en el funcionamiento de las trompas de Falopio debida a enfermedades inflamatorias, intervenciones quirúrgicas previas, por influencia de alteraciones congénitas en el funcionamiento de las trompas de falopio o la presencia de alteraciones producidas por tumores.
Síntomas del embarazo ectópico
En la fase inicial del embarazo la paciente se encuentra asintomática. Posteriormente son típicas otras manifestaciones como dolor abdominal en la parte inferior del abdomen, sobre todo del lado en donde se haya anidado el embrión. Cuando hay salida abundante de sangre hacia el peritoneo (membrana abdominal que envuelve los órganos), se produce un dolor intenso. Según la cantidad de sangre que se pierda hacia el peritoneo, se notará mareo , habrá hipotensión arterial e incluso la paciente puede entrar en shock.
La paciente percibe que tiene una falta en la menstruación que puede ser de más o menos duración. Aparece también una hemorragia vaginal que es irregular y no muy abundante. Otros síntomas que se pueden presentar son los propios de una gestación normal: náuseas vómitos, dolor en las mamas… En un 50% de los casos a la exploración se palpa una masa en el abdomen.
Tratamiento para el embarazo ectópico
Si se sospecha de embarazo ectópico, se ingresa a la paciente en el hospital para el control de su situación y evolución.
En ocasiones los embarazos ectópicos se resuelven espontáneamente, por eso existen circunstancias en las que se mantiene una actitud expectante si la paciente está asintomática, sin alteraciones de las constantes vitales, y se observa que las trompas de Falopio están íntegras con controles ecográficos y análisis de sangre frecuentes.
El tratamiento médico se realiza administrando por vía oral, intramuscular o inyectando directamente en el saco de gestación bajo control ecográfico, un fármaco quimioterápico llamado Metotrexato que impide el crecimiento del embrión y su destrucción, todo ello bajo control hospitalario con la paciente ingresada.
Si no hay éxito con el tratamiento médico, se realiza un tratamiento quirúrgico , siempre que sea posible, por medio de laparoscopia o por laparotomía (cirugía abierta del abdomen).
Pruebas complementarias del tratamiento del embarazo ectópico
Test de embarazo : si existen dudas, se determina analíticamente en sangre la presencia de un aumento de B- HCG (hormona gonadotropina coriónica humana).
Analítica de sangre con determinación de hemograma, coagulación, grupo sanguíneo y Rh.
Ecografía : preferentemente se realiza una ecografía transvaginal (introducción de un utensilio en forma de cono a través de la vagina que tiene una sonda para obtener las imágenes).
Laparoscopia diagnóstica : se realiza en casos de test de embarazo positivo con dudas diagnósticas por no visualizar ninguna imagen patológica en la ecografía. Se trata de la introducción, por medio de pequeñas incisiones en el abdomen, de un dispositivo fino con una cámara en su extremo con luz que sirve para visualizar de forma directa el abdomen y así localizar la masa gestacional.
Factores de riesgo y desencadenantes del embarazo ectópico
Padecer una enfermedad inflamatoria pélvica.
Simeterse a fecundación in vitro : se puede favorecer el embarazo ectópico por la transferencia del embrión con la introducción excesiva del catéter en la luz de la trompa de falopio y por la alteración de la disposición anatómica de esta, debido al sobrecrecimiento del ovárico, ocasionado por la estimulación hormonal previa que padece.
Antecedentes previos de cirugía pélvica de la trompa de falopio.
Tener adherencias (uniones anómalas) de la cicatrización de una cirugía pélvica previa.
Padecer endometriosis.
Utilizar como método anticonceptivo un DIU (dispositivo intrauterino).
Tener alguna alteración anatómica de las trompas de Falopio.
Haber padecido anteriormente un embarazo ectópico.
Elevada edad materna (mayor de 35 años).
El tabaquismo.
Complicaciones del embarazo ectópico
Rotura de la trompa de Falopio.
Evolución (excepcional) a un embarazo abdominal (si la placenta consigue un lugar de implantación), lo que conlleva en la mayoría de los casos aparición de malformaciones en el feto en desarrollo.
Si se produce un sangrado activo interno, la paciente puede llegar a tener un shock hipovolémico (con fallo multiorgánico y riesgo de muerte).
Infertilidad posterior.
Prevención del embarazo ectópico
En muchas ocasiones no hay manera de prevenir un embarazo ectópico. La prevención va destinada a evitar aquellos factores que pueden alterar el funcionamiento de la trompa de Falopio, como evitar los riesgos de padecer una enfermedad inflamatoria pélvica y las enfermedades de transmisión sexual: múltiples parejas sexuales, relaciones sin protección , etc.
Otro factor fundamental es acudir regularmente a revisiones de ginecología para así poder detectar a tiempo cualquier anormalidad o enfermedad que pueda desencadenar un embarazo ectópico (endometriosis, adherencias tras cirugías…etc.)
Especialidades a las que pertenece el embarazo ectópico
El especialista que diagnostica y trata el embarazo ectópico es el ginecólogo-obstetra.
Preguntas frecuentes
¿Cómo es de peligroso un embarazo ectópico?
Un embarazo ectópico puede llegar a ser causa de complicaciones muy graves para la paciente, incluso su muerte, aunque esto es algo poco frecuente. Depende de la localización del embarazo puede tener mayor o menor riesgo, pero siempre es una alteración que se debe tratar para evitar complicaciones muy graves.
¿Qué posibilidades hay de sufrir un embarazo ectópico?
La incidencia total de los embarazos ectópicos es del 1-2% de todas las gestaciones. Hay mayor posibilidad de sufrir un embarazo ectópico si se padecen factores de riesgo que puedan desencadenarlo.
¿Hay mujeres con más riesgo que otras de sufrir un embarazo ectópico?
Sí, aquellas que padecen factores de riesgo arriba detallados pueden padecer con mayor probabilidad un embarazo ectópico.
Tras un embarazo ectópico… ¿Podré tener otro embarazo normal?
Sí, todo depende de dónde se haya alojado el embarazo ectópico sufrido y del tratamiento que se haya tenido que llevar a cabo, siendo fundamental que las trompas de Falopio o al menos una de ellas, tenga un funcionamiento adecuado.
Si quieres conocer cuánto sabes sobre el embarazo, realiza nuestro test de embarazo . Con él descubrirás todos los consejos y cuidados que han de tener las mujeres embarazadas.

Enfermedad
Endocarditis
¿Qué es la endocarditis?
La endocarditis es una infección cardiaca , en concreto del endocardio, que es la parte que recubre el interior de las válvulas y de las cavidades del corazón . Es también conocida como infección de las válvulas del corazón o endocardio. Se produce por bacterias, gérmenes u hongos. Se trata de una patología perteneciente a la especialidad de cardiología y es de tipo grave.
Tipos de endocarditis
La endocarditis se clasifica según la velocidad a la que se desarrolle la enfermedad:
Aguda : cuando los patógenos tienen una actividad virulenta muy rápida y son muy agresivos. La enfermedad se desarrolla en cuestión de días.
Subaguda : en este caso los patógenos son menos agresivos y la enfermedad se desarrolla más pausadamente, en semanas o meses.
Causas de la endocarditis
La endocarditis es causada por la entrada en el cuerpo de gérmenes, bacterias u hongos que a través del torrente sanguíneo llegan a la cavidad del corazón y se adhieren a aquellas zonas del endocardio (revestimiento interno de las válvulas y cavidades del corazón), que están dañadas.
Suele producirse por la presencia de dichos organismos en el intestino, la piel, la boca o la garganta, debido a agentes externos como agujas mal esterilizadas o catéteres , entre otros.
Síntomas de endocarditis
La endocarditis es una enfermedad que puede aparecer bien de manera brusca, bien poco a poco.
En función de cada paciente y del modo de aparición de la enfermedad los síntomas son diferentes:
Fatiga constante.
Dolores musculares.
Fiebre y escalofríos.
Dolor en el pecho.
Pérdida de peso.
Manchas rojas en los dedos de manos y pies.
Tratamiento para la endocarditis
La endocarditis al ser una infección se trata primariamente con antibióticos , de forma que disminuyan los síntomas y se elimine el virus o bacteria que haya provocado la infección.
En caso de que la infección haya dañado en gravedad las válvulas se requerirá de cirugía bien para tratar directamente la infección o para sustituir la válvula dañada.
Pruebas complementarias del tratamiento de endocarditis
Para poder determinar concretamente la endocarditis, deben realizarse diferentes pruebas médicas:
Reconocimiento médico : en un primer momento el médico preguntará al paciente por los síntomas y le hará una primera exploración física.
Analítica : con el fin de ver si los niveles están bien o no, para ver si existe infección en el organismo.
Diagnóstico por imagen : se pueden realizar diferentes pruebas para obtener una imagen del corazón y ver si existe endocarditis. Entre ellas destaca el ecocardiograma (se observa el corazón mediante ondas sonoras), la radiografía de tórax o la resonancia magnética.
Electrocardiograma : medición de la actividad cardíaca mediante electrodos.
Factores desencadenantes de la endocarditis
La endocarditis se desarrolla por la llegada de un patógeno a la zona del corazón a través del torrente sanguíneo.
Dicho patógeno puede provenir de diferentes sitios del organismo, pero solo afecta al corazón, como bacterias alojadas en el intestino o la boca que penetran ante un alimento o una herida, respectivamente.
Factores de riesgo de la endocarditis
Las personas que padecen los siguientes aspectos tienen mayor riesgo de contraerla:
Prótesis cardíacas : las válvulas artificiales tienen mayor tendencia a acumular bacterias.
Antecedentes cardíacos : si el paciente ha padecido endocarditis con anterioridad.
Problemas cardíacos crónicos : si el paciente tiene alguna anomalía o alteración cardíaca, o si padece enfermedades que hayan dañado las válvulas del corazón.
Complicaciones de la endocarditis
Bloqueo de la arteria pulmonar (embolia pulmonar).
Daño cerebrovascular.
Agravamiento de problemas cardíacos.
Parálisis y/o convulsiones.
Abscesos en diferentes órganos (formación de bolas de pus).
Prevención de la endocarditis
Mantener una correcta higiene , sobre todo de la zona bucal, para evitar el acceso a organismos patógenos.
No realizar perforaciones en la piel, evitar hacerse piercings o tatuajes ; y en caso de que se los haga acuda a sitios especializados con material esterilizado.
Acudir a revisiones médicas.
Informarse de los antecedentes familiares por si existe riesgo de padecerla.
Ante cualquier síntoma acudir a un médico, cuanto antes se detecte e inicie el tratamiento menores serán los riesgos.
Especialidades a las que pertenece la endocarditis
La endocarditis debe ser tratada por especialistas de cardiología.
Preguntas frecuentes:
¿Qué es la endocarditis bacteriana en Odontología?
Es la endocarditis que se produce por la infección de un tipo de bacteria tras un procedimiento quirúrgico odontológico.
Por ello, las personas que padecen enfermedades cardíacas no tienen recomendado someterse a este tipo de intervenciones.
¿Qué son los nódulos de Osler?
Son lesiones de la piel que tienen un color púrpura y abultado que se localizan debajo de los dedos de pies y manos, siendo uno de los indicadores de endocarditis.
¿Qué es la endocarditis reumática?
Es un tipo de endocarditis que se forma tras padecer fiebre reumática (fiebre producida por la infección de bacterias estreptococos del grupo A).
¿Qué es la fiebre recurrente?
Es una infección que provoca fiebres elevadas y se transmite al cuerpo humano por garrapatas o piojos.
¿Qué es endocarditis subaguda?
La endocarditis que se desarrolla por patógenos poco agresivos y avanza despacio en cuestión de semanas o meses.

Enfermedad
Dispepsia
¿Qué es la dispepsia?
El término dispepsia hacer referencia a un conjunto de síntomas y signos complejos y heterogéneos originados en el tracto gastrointestinal superior. Una de las definiciones aceptadas puede ser la presencia de dolor o molestia abdominal persistente o recurrente, localizada en la parte superior del abdomen de al menos 3 meses de duración.
Es una alteración frecuente que puede afectar al 25-40% de la población general , más frecuentemente en mujeres.
Habitualmente no supone una patología grave, pero depende la causa de la producción de los síntomas, su gravedad será más o menos relevante.
Tipos de dispepsia
Una de las clasificaciones más aceptadas de la dispepsia es aquella que las divide en:
Dispepsia orgánica: las que producen síntomas dispépticos originados por diferentes enfermedades orgánicas (digestivas o no).
Dispepsia funcional: se trata de un trastorno funcional gastrointestinal en el que no existe influencia de toma de medicamentos, alcohol, tabaco…por parte del paciente, y en el que los estudios bioquímicos, endoscópicos y ecográficos no aportan evidencia de enfermedad orgánica que justifique los síntomas.
Causas de la dispepsia
Existen diversas patologías que se han relacionado con la producción de dispepsia orgánica, siendo las patologías más relevantes el reflujo gastroesofágico, cáncer de esófago, cáncer gástrico, enfermedad ulcerosa péptica, duodenitis erosiva, la esofagitis y la litiasis biliar . Dentro de las causas que se han relacionado con la dispepsia funcional están las gastroenteritis agudas, la infección por Helicobacter Pylori, la irritación química de la mucosa gastrointestinal por la ingesta de tabaco, alcohol, antiinflamatorios no esteroideos, reflujo gastroesofágico. También se ha relacionado con trastornos psicológicos y alteraciones de la motilidad gastrointestinal.
Síntomas de la dispepsia
Dentro de los síntomas que se describen en la dispepsia están epigastralgia (dolor en la parte superior central del abdomen, “en la boca del estómago”), ardor de estómago, hinchazón abdominal después de las comidas, saciedad precoz, sensación nauseosa y vómitos, eructos. Algunos autores incluyen síntomas de quemazón o pirosis y regurgitación de la comida, aunque estos síntomas son más típicos de el reflujo gastroesofágico.
Son síntomas y signos de alarma de un posible origen orgánico grave de la dispepsia la pérdida de peso significativa no intencionada, presentar vómitos persistentes, disfagia (dificultad para tragar), hematemesis (vómitos de sangre), melenas (presencia de sangre en las heces), tener anemia con falta de hierro o presentar una masa abdominal palpable.
Tratamiento para la dispepsia
En el caso de la dispepsia funcional, el tratamiento se basará en aquel específico de la patología que origina los síntomas dispépticos.
El tratamiento se basa en establecer una serie de medidas generales como disminuir el grado de estrés, normalizar el ritmo sueño-vigilia, seguir horarios fijos de comidas, eliminar determinados alimentos de la dieta como las bebidas gaseosas, alimentos flatulentos o grasas, el alcohol, tabaco, cafeína, fármacos antiinflamatorios, etc. Realizar ejercicio físico, perder peso e instaurar medidas antirreflujo gastroesofágico (no irse a dormir justo después de comer, no comer comidas muy picantes, etc.)
En caso de detección de infección por Helicobacter pylori se aconseja su tratamiento con antibióticos e inhibidores de la bomba de protones (omeprazol).
En pacientes que no presentan signos de alarma o cuando se ha descartado una causa de dispepsia orgánica mediante pruebas diagnósticas, se instaura inicialmente un tratamiento de prueba durante unas 4 semanas con antisecretores como el omeprazol o la ranitidina. Si hay mejoría se retira la medicación y si existen recaídas se pauta una dosis los más baja posible que logre controlar los síntomas.
Otros de los fármacos utilizados en ocasiones son los procinéticos como la domperidona ( Motilium )
Pruebas complementarias del tratamiento de la dispepsia
La evaluación inicial para el diagnóstico de la dispepsia es una adecuada anamnesis (interrogatorio que realiza el médico para evaluar lo que le pasa al enfermo) y una adecuada exploración física.
Se le podrá realizar al paciente una analítica de sangre para descartar alteraciones como anemia o disfunciones del hígado o el páncreas.
En muchos de los pacientes que presentan estos síntomas se les indicará la realización de una endoscopia digestiva alta (visión del interior del esófago, estómago y duodeno con la introducción de un tubo flexible que se introduce por la boca que tiene una cámara con luz).
Otra de las pruebas que se pueden realizar es la prueba del aliento o test de detección del Helicobacter Pylori , para descartar la infección por esta bacteria como posible causa de la dispepsia.
Factores de riesgo de la dispepsia
Tomas frecuentes de fármacos antiinflamatorios no esteroideos como ibuprofeno, (ácido acetilsalicílico (aspirina), etc.
Consumo de alcohol, tabaco, café, etc.
Infección por Helicobacter Pylori.
Padecer enfermedades gastrointestinales como úlcera gástrica, pancreatitis, esofagitis, hernia de hiato, etc.
Complicaciones de la dispepsia
En el caso de las dispepsias orgánicas las complicaciones vendrán derivadas de las patologías que originan la dispepsia, y derivan en trastornos más o menos graves (complicaciones de un tumor esofágico o pancreático, una úlcera péptica, etc.).
En el caso de las dispepsias funcionales no hay una complicación propiamente dicha salvo la incomodidad de presentar la sintomatología de forma intermitente y los efectos secundarios que se puedan dar de los tratamientos pautados o las pruebas diagnósticas iniciales realizadas. Hacer un diagnóstico temprano puede retrasar en el futuro un posible diagnóstico de otra patología en la que se solapen los síntomas debido a que se lo “achaquen” a la dispepsia funcional diagnosticada previamente.
Prevención de la dispepsia
Evitar comidas con alto contenido graso, picantes, etc. Eliminar las bebidas gaseosas.
No tomar café ni alcohol, así como tabaco o cualquier otra droga.
Realizar comidas con adecuada masticación e intentar llevar unos ritmos de comida habituales establecidos, con 5 comidas al día.
Evitar el consumo continuado de antiinflamatorios no esteroideos.
Especialidades a las que pertenece la dispepsia
La dispepsia será evaluada y tratada inicialmente por el médico de atención primaria. Si el paciente no responde al tratamiento o detectan alteraciones importantes en las pruebas diagnóstica o sospecha de la posible gravedad de la enfermedad remitirá al paciente a consultas del especialista en gastroenterología o digestivo.
Preguntas frecuentes
¿Qué es la dispepsia gastrointestinal?
Se puede definir la dispepsia gastrointestinal como la presencia en la zona superior del abdomen de dolor o molestias, sensación de ardor, náuseas, o vómitos o cualquier otro síntoma que se considere originado en el tracto gastrointestinal superior.
¿Qué es la dispepsia flatulenta?
No hay una entidad en sí misma denominada dispepsia flatulenta. Dentro de los síntomas que definen la dispepsia se recoge la sensación de hinchazón abdominal y en ocasiones el aumento de la expulsión de gases, mediante eructos o flatulencias.
¿Es lo mismo dispepsia que indigestión estomacal?
Dentro de las posibles causas de la dispepsia funcional se ha descrito la gastroenteritis aguda. El término indigestión estomacal es una definición popular que puede hacer referencia al padecimiento de la gastroenteritis, por lo que se puede decir que pueden tener relación.
¿Por qué se produce la acidez de estómago?
La acidez de estómago se produce por el paso de contenido gástrico de forma ascendente hacia el esófago por incompetencia o relajación inadecuada del esfínter esofágico inferior (“puerta de entrada al estómago”), lo que supone un ascenso de los jugos gástricos ácidos del estómago que provocan la sensación de quemazón en el esófago.
¿Qué comer para evitar la acidez de estómago?
Los alimentos recomendados para disminuir la acidez son las cocciones sencillas con uso de la plancha, grill, el horno, alimentos hervidos etc. Comer pasta, arroz, patata, pan blanco. Introducción de abundantes verduras cocidas y sin piel, frutas cocidas, en compota y en conserva. Consumo de carnes magras , pescados, clara de huevo, quesos y lácteos desnatados. Beber agua y bebidas sin cafeína ni gas.
 Savia
Savia